Clear Sky Science · de
Integrierte virtuelle Durchmusterung, ADMET-Profilierung und Molekulardynamik-Simulationen neuartiger natürlicher HDAC6-Inhibitoren mit dem Potenzial, den Abbau der Skelettmuskulatur zu mildern
Warum es wichtig ist, unsere Muskeln zu schützen
Skelettmuskulatur dient nicht nur zum Heben von Gewichten oder Laufen; sie ist der größte Protein-Reservoir des Körpers, ein wichtiger Treiber des Stoffwechsels und unverzichtbar für alltägliche Bewegungen. Wenn Muskeln durch Alter, Krankheit oder Inaktivität zurückgehen, verlieren Menschen Kraft, Selbstständigkeit und Lebensqualität. Diese Studie untersucht einen rechnergestützten Ansatz zur Entdeckung neuer Wirkstoffkandidaten aus natürlichen Substanzen, die diesen Muskelschwund verlangsamen oder verhindern könnten, indem sie einen zentralen molekularen Schalter in Muskelzellen anvisieren.
Ein problematisches Molekül bei Muskelschwäche
Innerhalb von Muskelfasern steuert ein Protein namens HDAC6 die Organisation des inneren Gerüsts und den Abbau anderer Proteine. Unter normalen Bedingungen trägt es zur gesunden Muskelpflege bei. Wird die HDAC6-Aktivität jedoch übermäßig, destabilisiert das die Mikrotubuli, die Form und die neuromuskulären Verbindungen der Muskeln erhalten. Diese Störung begünstigt Proteinschäden und das Schrumpfen des Muskels. Tierstudien haben gezeigt, dass die Blockade von HDAC6 die Muskelgröße erhalten und die Funktion verbessern kann, weshalb es ein attraktives Wirkstoffziel gegen Muskelatrophie ist.
Auf der Suche nach neuen Wirkstoffideen in der Natur
Viele vorhandene HDAC6-Blocker wurden synthetisch entworfen und können unerwünschte Nebenwirkungen haben oder nicht spezifisch genug sein. Die Autoren wandten sich stattdessen der chemischen Vielfalt der Natur zu, mit der Überlegung, dass Naturstoffe oft Strukturen aufweisen, die sanft und zugleich effektiv mit menschlichen Proteinen interagieren. Sie nutzten die Sammlung SuperNatural 3.0, die nahezu eine halbe Million verschiedener Naturverbindungen enthält, und stellten die einfache Frage: Welche dieser Moleküle könnten sich in die aktive Rinne von HDAC6 einfügen, sie so abschalten und gleichzeitig als vielversprechende Arzneimittel erscheinen? 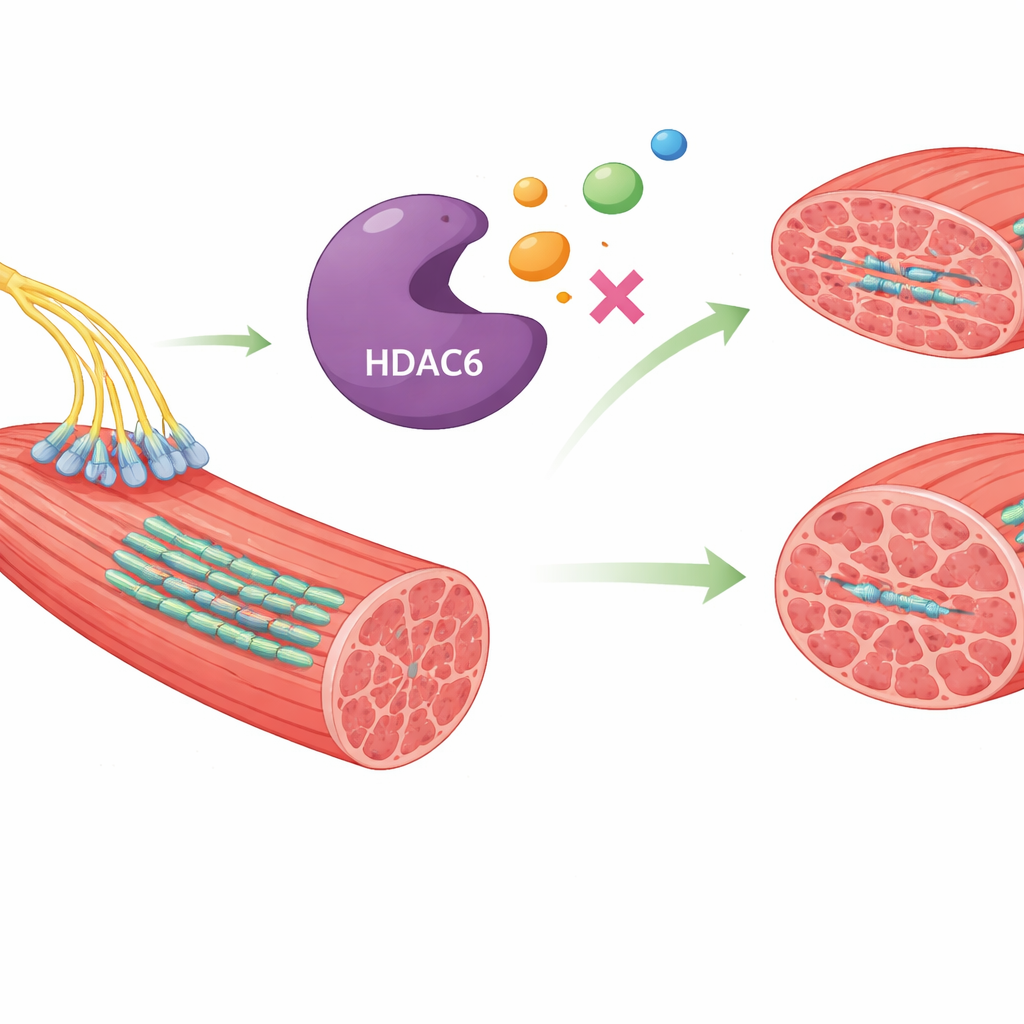
Hochgeschwindigkeits-Computerscreening von Hunderttausenden Molekülen
Um das zu beantworten, verwendete das Team eine integrierte Pipeline für virtuelles Screening. Zuerst bereiteten sie ein detailliertes dreidimensionales Modell des katalytischen Tunnels von HDAC6 vor, basierend auf einer experimentellen Struktur des Enzyms, die an einen bekannten Inhibitor gebunden ist. Anschließend dockten sie mit spezialisierter Software 449.058 Naturverbindungen in diesen Tunnel und bewerteten, wie eng und günstig sich jedes einzelne einfügte. Aus diesem riesigen Anfangspool schnitten 146 Moleküle besser ab als das Referenzmedikament Trichostatin A. Die Forscher wendeten dann eine Reihe von Filtern an, die dem entsprechen, worauf Arzneimittelentwickler achten: richtige Größe und Polarität, Aufnahmefähigkeit über den Darm, akzeptable Löslichkeit, begrenzte vorhergesagte Toxizität und realistische Aussichten auf chemische Synthese. Nach diesen Schritten blieben zwei herausragende Kandidaten übrig, bezeichnet als SN0000021 und SN0000043.
Testen von Stabilität und Verhalten in einer virtuellen Zelle
Eine gute Docking-Orientierung reicht nicht aus; potenzielle Wirkstoffe müssen unter der ständigen Bewegung realer biologischer Systeme gebunden bleiben. Um das zu prüfen, führte das Team lange Molekulardynamik-Simulationen durch, gewissermaßen hochauflösende Filme der HDAC6–Verbindungskomplexe über 200 Milliardenstel Sekunden. Sie überwachten, wie stark das Proteingerüst schwankte, wie tief sich jedes Molekül im Tunnel befand, wie exponiert es dem umgebenden Wasser war und wie eng der Komplex verpackt blieb. Beide Naturverbindungen bildeten stabile, langanhaltende Wechselwirkungen mit Schlüsselaminosäuren, die für die Steuerung der HDAC6-Aktivität bekannt sind. Sie zeigten geringere Fluktuationen und dichtere Packung als der Referenzinhibitor, was auf eine robustere Anpassung hindeutet. Fortgeschrittene Energie-Berechnungen, die abschätzen, wie günstig die Bindung aus thermodynamischer Sicht ist, bestätigten zusätzlich, dass diese beiden Moleküle wahrscheinlich stärker binden als das Kontrollmedikament. 
Von Computertreffern zu zukünftigen muskelschützenden Medikamenten
Für Nichtfachleute ist die Kernaussage klar: Mit allein rechnerischen Mitteln durchkämmten die Forschenden einen enormen Katalog natürlicher Substanzen und identifizierten zwei, die besonders gut geeignet scheinen, sich an HDAC6 zu binden und dessen Aktivität zu unterdrücken — ein Protein, das mit Muskelschwund verbunden ist. Diese Kandidaten binden nicht nur in Simulationen fest, sondern zeigen auch vorteilhafte vorhergesagte Absorptions-, Verteilungs- und Sicherheitsprofile, was sie zu vielversprechenden Ausgangspunkten für neue Arzneien macht. Die Arbeit beweist noch nicht, dass diese Moleküle reale Muskeln schützen; dafür sind Laborversuche mit dem gereinigten Enzym, Zelltests und Tiermodelle nötig. Die Studie liefert jedoch eine überzeugende Roadmap dafür, wie digitales Screening von Naturstoffen potenzielle Therapien zum Schutz der Skelettmuskulatur vor Degeneration aufspüren kann.
Zitation: Ahmad, K., Ahmad, S.S. & Choi, I. Integrated virtual screening, ADMET profiling, and molecular dynamics simulations of novel natural HDAC6 inhibitors with the potential to ameliorate skeletal muscle degeneration. Sci Rep 16, 7840 (2026). https://doi.org/10.1038/s41598-026-39066-6
Schlüsselwörter: Skelettmuskelatrophie, HDAC6-Hemmung, Entdeckung von Medikamenten aus Naturstoffen, virtuelles Screening, Muskuläre Regeneration