Clear Sky Science · de
Das casr-Gen von Zebrafischen beeinflusst Herzstruktur und -funktion
Warum Fischherzen für die menschliche Gesundheit wichtig sind
Unser Herz ist auf Calcium, ein einfaches Mineral, angewiesen, um richtig zu schlagen. Wenn die Calciumsignale gestört sind, kann das zu Herzversagen oder anderen schweren Erkrankungen führen. In dieser Studie nutzen die Forschenden winzige Zebrafische — durchsichtige Süßwasserfische, die oft im Labor verwendet werden —, um zu untersuchen, wie ein calcium-sensierender Schalter in Zellen die Herzstärke und das Überleben beeinflusst. Durch das Abschalten eines einzelnen Gens, das Zellen hilft, Calcium zu erkennen, entdeckten sie eine Kaskade von Problemen beim Herzschlag, in der Körperform und sogar in der luftgefüllten Schwimmblase der Fische. Ihre Arbeit zeigt außerdem, dass der genetische Gesamtzustand eines Tiers die Folgen einer schädlichen Mutation deutlich abschwächen oder verschärfen kann — eine Erkenntnis mit klaren Parallelen zur Humanmedizin.
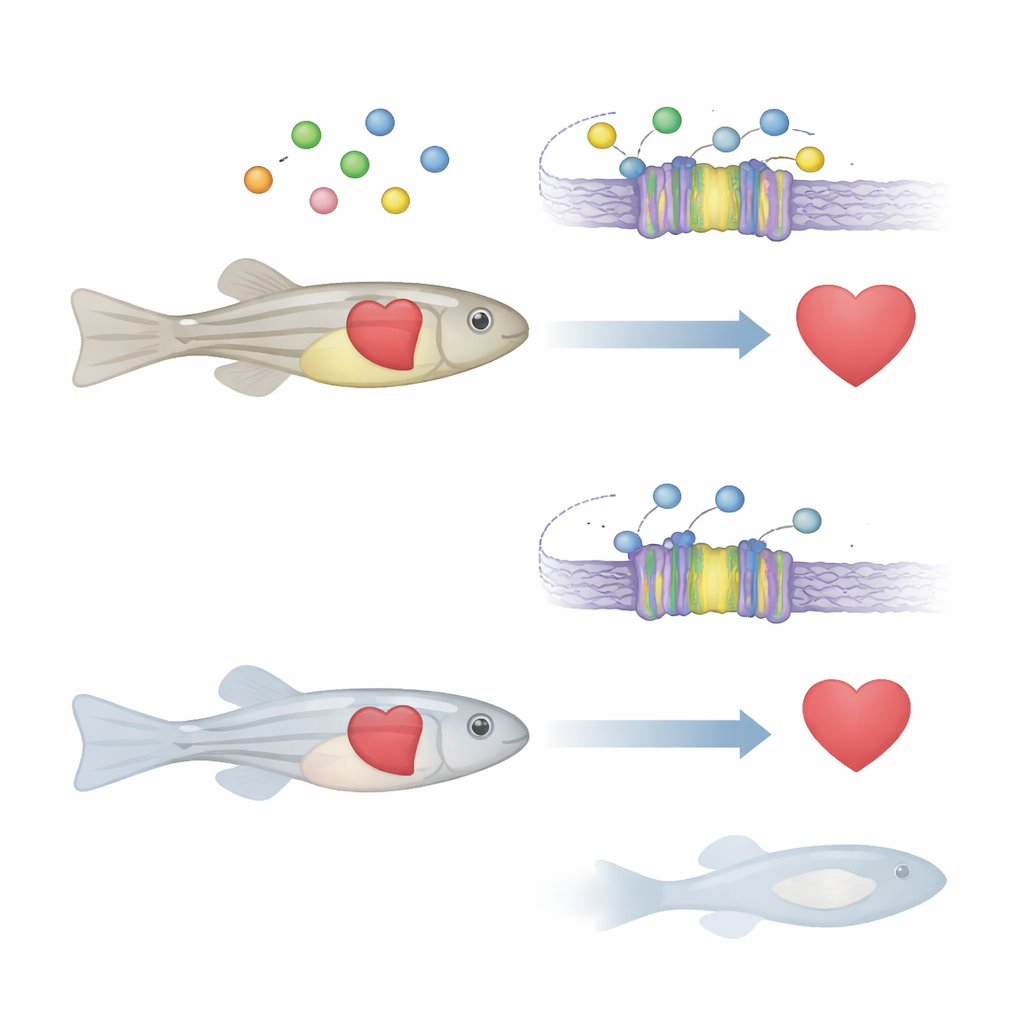
Ein zellulärer "Thermostat" für Calcium
Calcium innerhalb und außerhalb von Zellen fungiert als universelles Signal, das Muskelbewegung, Hormonfreisetzung und sogar die Aktivierung bestimmter Gene steuert. Viele Organe sind auf ein Protein angewiesen, den calcium-sensitiven Rezeptor, der wie ein Thermostat für Calciumwerte wirkt. Wenn sich das Calcium außerhalb der Zelle ändert, passt dieser Rezeptor die Hormonfreisetzung und andere Prozesse an, um das Gleichgewicht wiederherzustellen. Beim Menschen sind Defekte dieses Rezeptors bereits mit Knochen- und Mineralstoffwechselstörungen verknüpft, und er gilt als möglicher Mitspieler bei Herzerkrankungen und einigen Krebsarten. Wie genau dieser Calciumsensor jedoch die Herzentwicklung und -funktion in einem ganzen Organismus beeinflusst, war lange unklar.
Was passiert, wenn der Calciumsensor ausgeschaltet wird
Das Team konzentrierte sich auf die Zebrafisch-Version dieses Gens, genannt casr, die eng mit dem menschlichen Gegenstück verwandt ist. Mit modernen Geneditierungswerkzeugen erzeugten sie Zebrafische, bei denen beide Kopien von casr deaktiviert wurden. Zuerst wirkten die jungen Fische fast normal. Doch etwa fünf Tage nach der Befruchtung konnten viele Mutanten ihre Schwimmblase nicht aufblasen, ein kleines gasgefülltes Organ, das den Auftrieb steuert. Diese Fische sanken auf den Boden, schwammen schlecht, entwickelten bald eine Wirbelsäulenkrümmung und starben alle bis zur zweiten Lebenswoche. Diese äußerlichen Anzeichen deuteten auf schwerwiegende interne Probleme hin, die mehr als ein Organsystem betrafen.
Ein schwächeres, kleineres und langsameres Herz
Schnellaufnahmen und Bildanalyse schlagender Herzen zeigten, wie stark das Fehlen des Calciumsensors die Herzleistung beeinträchtigte. Bei normalen Zebrafischlarven füllt sich die Herzkammer (Ventrikel) und entleert sich in einem kräftigen, rhythmischen Muster. Bei den Mutanten war der Ventrikel beim Füllen deutlich kleiner, das Herz schlug langsamer und jeder Schlag förderte weniger Blut. Messgrößen dafür, wie stark sich der Herzmuskel verkürzt und wie sehr sich die Pumpkammerfläche bei jedem Schlag verändert, waren beide reduziert — ein Hinweis auf geschwächte Kontraktion. Das gesamte Herzzeitvolumen — das pro Minute beförderte Blutvolumen — sank deutlich. Auf Genebene veränderten sich hunderte Transkripte, und wichtige Netzwerke, die die Calciumhandhabung und die Mechanik der Muskelkontraktion steuern, waren herunterreguliert, womit ein Zusammenhang zwischen der Genveränderung und sowohl molekularem als auch mechanischem Herzversagen hergestellt wurde.
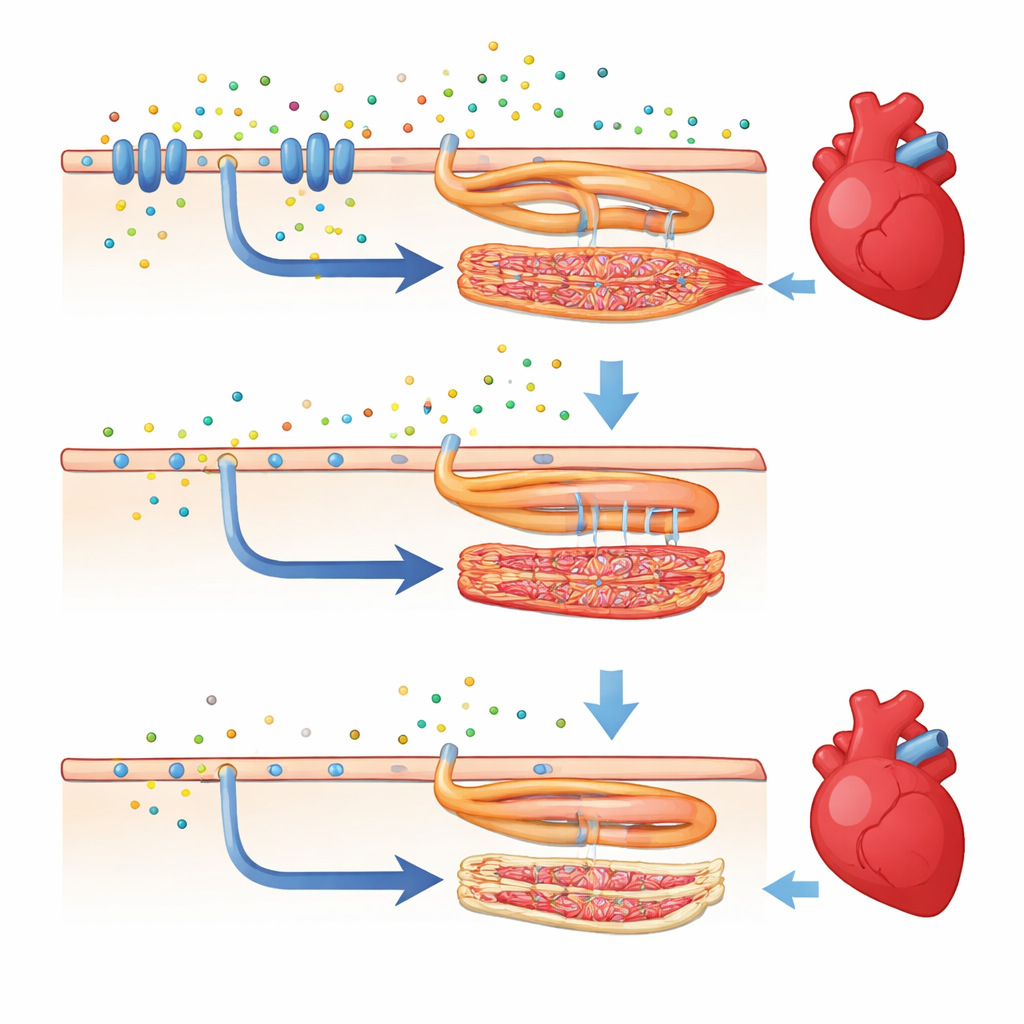
Wie Hintergrundgene ein krankes Herz retten können
Überraschenderweise verhielt sich dieselbe casr-Mutation in einer anderen häufigen Zebrafisch-Linie, bekannt als TL (Tupfel long-fin), ganz anders. Als der Gen-Knockout in diesen neuen genetischen Hintergrund überführt wurde, konnten die Fische ihre Schwimmblasen aufblasen, bis ins Erwachsenenalter überleben und zeigten eine deutlich bessere Herzfunktion. Ihre Herzen waren zwar noch teilweise beeinträchtigt — die Herzfrequenz blieb niedriger als normal —, doch die Maße dafür, wie kraftvoll der Ventrikel kontrahierte und wie viel Blut pro Minute gepumpt wurde, kamen fast an gesunde Fische heran. In diesen „geretteten“ Tieren kehrten viele der Gene, die mit Calcium-Signalen und Herzmuskelkontraktion verknüpft sind, auf mittlere Werte zurück, höher als in der ursprünglich kranken Linie. Das zeigt, dass andere Gene im Genom die Folgen einer schädlichen Veränderung abpuffern oder verstärken können.
Signale, die Herzen und Auftrieb formen
Über das Herz hinaus störte der Verlust des Calciumsensors auch wichtige wachstumssteuernde Systeme im Embryo. Gene der Wnt- und Hedgehog-Signalwege — bekannte Architekten der Organbildung — waren in den Mutanten heruntergeregelt. Diese Veränderungen tragen wahrscheinlich zur ausgefallenen Inflation der Schwimmblase bei, was wiederum das Überleben verschlechtern kann, weil sich Nahrungsaufnahme und Fortbewegung erschweren. Marker für die Differenzierung von Herzmuskelzellen waren ebenfalls vermindert und die Ventrikel kleiner, was darauf hindeutet, dass der Calciumsensor die Wachstums- und Reifungsprozesse von Herzmuskelzellen mitsteuert.
Was das für das Verständnis von Krankheitsrisiken bedeutet
Insgesamt zeigt diese Arbeit, dass der calcium-sensitiven Rezeptor ein entscheidender Wächter sowohl der Herzfunktion als auch der richtigen Organentwicklung bei Zebrafischen ist. Geht dieser Sensor verloren, versagen Calciumsignale, der Herzmuskel kontrahiert schwach, die Schwimmblase bleibt funktionslos und die Tiere sterben jung. Gleichzeitig unterstreicht die dramatische Rettung in einem anderen genetischen Stamm eine zentrale Botschaft: Der Rest des Genoms kann erheblich beeinflussen, wie gefährlich eine bestimmte Mutation tatsächlich ist. Für die menschliche Gesundheit betont dies, warum Menschen mit ähnlichen riskanten Genvarianten sehr unterschiedliche Krankheitsverläufe erleben können und warum das Verständnis sowohl der Kernkrankheitsgene als auch ihres genetischen Hintergrunds für Vorhersage und Behandlung von Herzerkrankungen unerlässlich ist.
Zitation: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Schlüsselwörter: Calcium-Signalisierung, Herzentwicklung, Zebrafischmodell, genetischer Hintergrund, Herzfunktion