Clear Sky Science · de
Zugkraftübertragung durch bioaktives Matrixhydrogel fördert epithelialen Kollektivmigration vermittelt durch Integrin
Wie Zellen gemeinsam ziehen, um zu heilen
Wenn Sie Ihre Haut schneiden oder ein Organ beschädigen, müssen Zellschichten koordiniert wandern, um die Wunde zu verschließen. Diese Studie stellt eine auf den ersten Blick einfache Frage: Wenn Zellen zusammenkriechen, zerren sie dann nur aneinander, oder „sprechen“ sie auch über das weiche Material unter ihnen miteinander? Durch die Nachbildung einer realistischen, gelartigen Umgebung im Labor zeigen die Autorinnen und Autoren, dass Zellen mechanische Kräfte durch diese weiche Matrix senden können, um die Gruppenbewegung zu lenken. Damit wird eine verborgene Kommunikationsebene sichtbar, die für Wundheilung, Gewebereparatur und sogar die Ausbreitung von Krebs entscheidend sein könnte.
Ein weicher Untergrund, der Kraft überträgt
In unserem Körper liegen viele Zellen auf einem weichen, proteinreichen Gerüst und nicht auf etwas Starrem wie Glas oder Plastik. Um dies nachzuahmen, kultivierten die Forschenden Nierenepithelzellen als zusammenhängende Schicht auf einem bioaktiven Hydrogel aus Matrigel und Kollagen, zwei gängigen Komponenten des natürlichen Gewebes. Sie erzeugten dann in der Mitte des Gels eine kleine freie Zone, ähnlich einer winzigen Wunde, und beobachteten, wie die Zellschicht nach innen marschierte, um die Lücke zu schließen. Um die Aktivität eines wichtigen Signalwegs in den Zellen zu verfolgen, nutzten sie einen fluoreszenten Biosensor, der die Aktivität von ERK meldet — einem Protein, das häufig auf mechanische Reize reagiert. Dieses System erlaubte es ihnen, in Echtzeit zu sehen, wie mechanische Kräfte im weichen Gel mit Zellbewegung und innerer Signalgebung zusammenhängen. 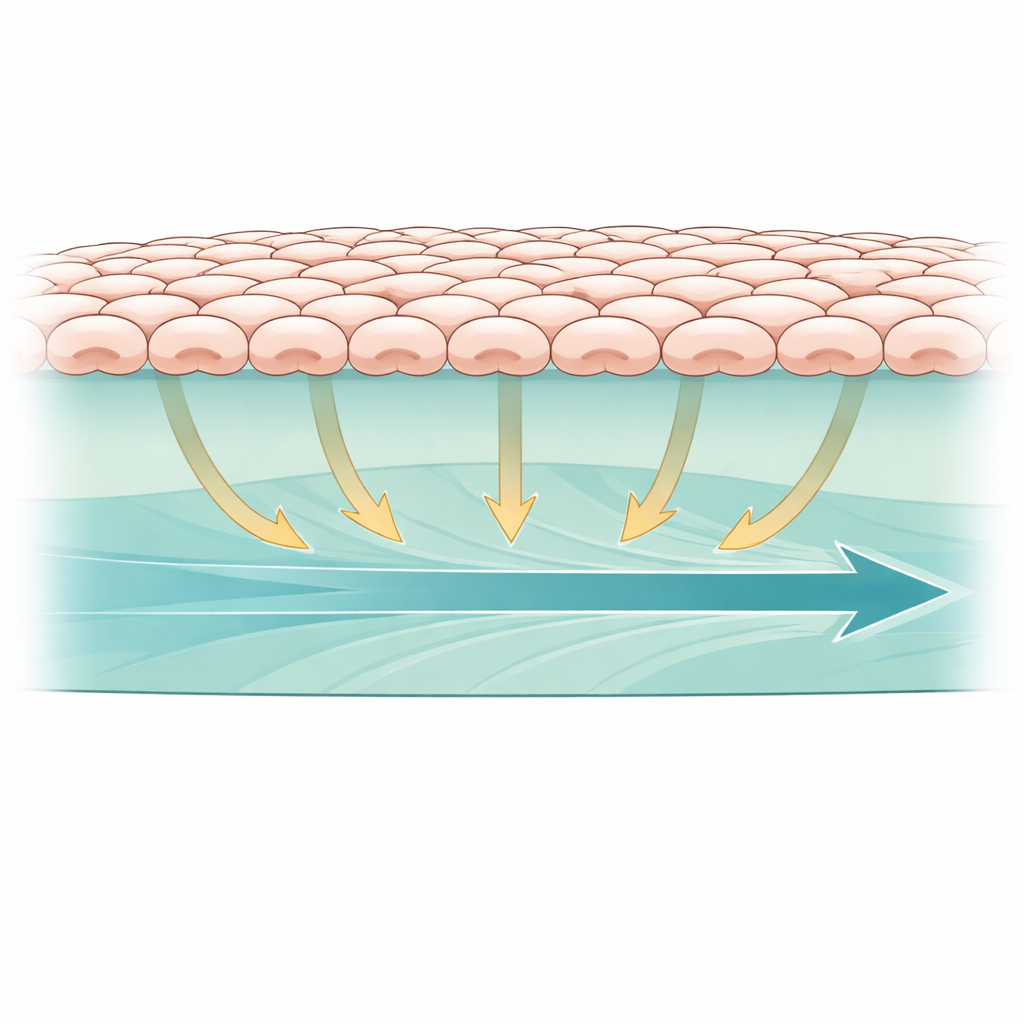
Den Boden beobachten, wie er sich unter den Zellen bewegt
Um zu prüfen, ob das Gel tatsächlich Kräfte trägt und überträgt, mischte das Team winzige magnetische Kügelchen in das Material und verfolgte deren Bewegung während der Zellmigration. Auf dem normalen Gel, das sowohl Matrigel als auch Kollagen enthielt, rutschten die Kügelchen langsam vorwärts in dieselbe Richtung wie die vorrückende Zellschicht, was darauf hindeutet, dass die Zellen die Matrix packen und mitziehen. Auf Geln, die nur aus Matrigel bestanden, bewegten sich die Kügelchen langsamer, was auf eine schwächere Kraftübertragung schließen lässt. Wurde das Gel chemisch mit Glutaraldehyd quervernetzt, um das Netzwerk zu versteifen und „zu verriegeln“, verschoben sich die Kügelchen kaum noch. Unter diesen verriegelten Bedingungen hafteten die Zellen zwar weiterhin, ihr kollektives Vorrücken verlangsamte sich jedoch drastisch, und das ERK-Signal wurde schwächer und weniger am Vorderrand konzentriert — ein Hinweis darauf, dass starke Matrixtraktion mit schnellerer, gezielterer Gruppenbewegung verbunden ist.
Innere Motoren und Ionenkanäle treiben die Bewegung an
Die Autorinnen und Autoren untersuchten als Nächstes, was innerhalb der Zellen diese Zugkräfte erzeugt und wie diese Aktivität wahrgenommen wird. Sie setzten Wirkstoffe ein, um die myosinabhängige Kontraktion zu blockieren — denselben molekularen Mechanismus, der Muskelkraft antreibt. Wenn die Kontraktion gehemmt war, sank die ERK-Aktivität und die Zellschicht rückte langsamer vor, was zur Idee passt, dass internes Ziehen nötig ist, um Spannung in die Matrix zu übertragen. Außerdem störten sie verschiedene Typen von Kalziumkanälen in der Zellmembran und dem intrazellulären Kalziumspeicher. Das Blockieren dieser Ionenwege dämpfte ERK-Aktivität und verlangsamte die kollektive Migration, was auf eine Kaskade hindeutet, in der mechanisches Ziehen an der Matrix in Kalzium- und ERK-Signale umgewandelt wird, die helfen, die Gruppe gemeinsam in Bewegung zu halten.
Die Richtung durch Oberflächenverankerungen lenken
Ein besonders auffälliges Ergebnis ergab sich beim Anvisieren von Integrinen, den Oberflächenmolekülen, die wie winzige Anker Zellen mit ihrer Umgebung verbinden. Als die Forschenden einen wichtigen Integrinuntertyp blockierten, bewegte sich die Schicht nicht mehr als kohärente Front vorwärts, obwohl einzelne Zellen weiterhin lokal nahezu normal wackeln konnten. Gleichzeitig kamen die Kügelchenbewegungen im Gel praktisch zum Stillstand, was zeigt, dass Integrine für die Übertragung von Kraft aus den kontrahierenden Zellen in die Matrix unerlässlich sind. Im Gegensatz dazu reduzierte das Blockieren von Piezo1-ähnlichen mechanosensitiven Kanälen, die Zellen helfen, physikalischen Druck zu spüren, sowohl das Tempo der Migration als auch die im Gel sichtbare Traktion. Zusammengenommen zeichnen diese Ergebnisse das Bild, dass Kontraktion Kraft erzeugt, Integrine sie an die Matrix übertragen und mechanosensitive Kanäle sowie ERK-Signalgebung diese Kraft interpretieren, um Richtung und Effizienz der kollektiven Bewegung zu koordinieren. 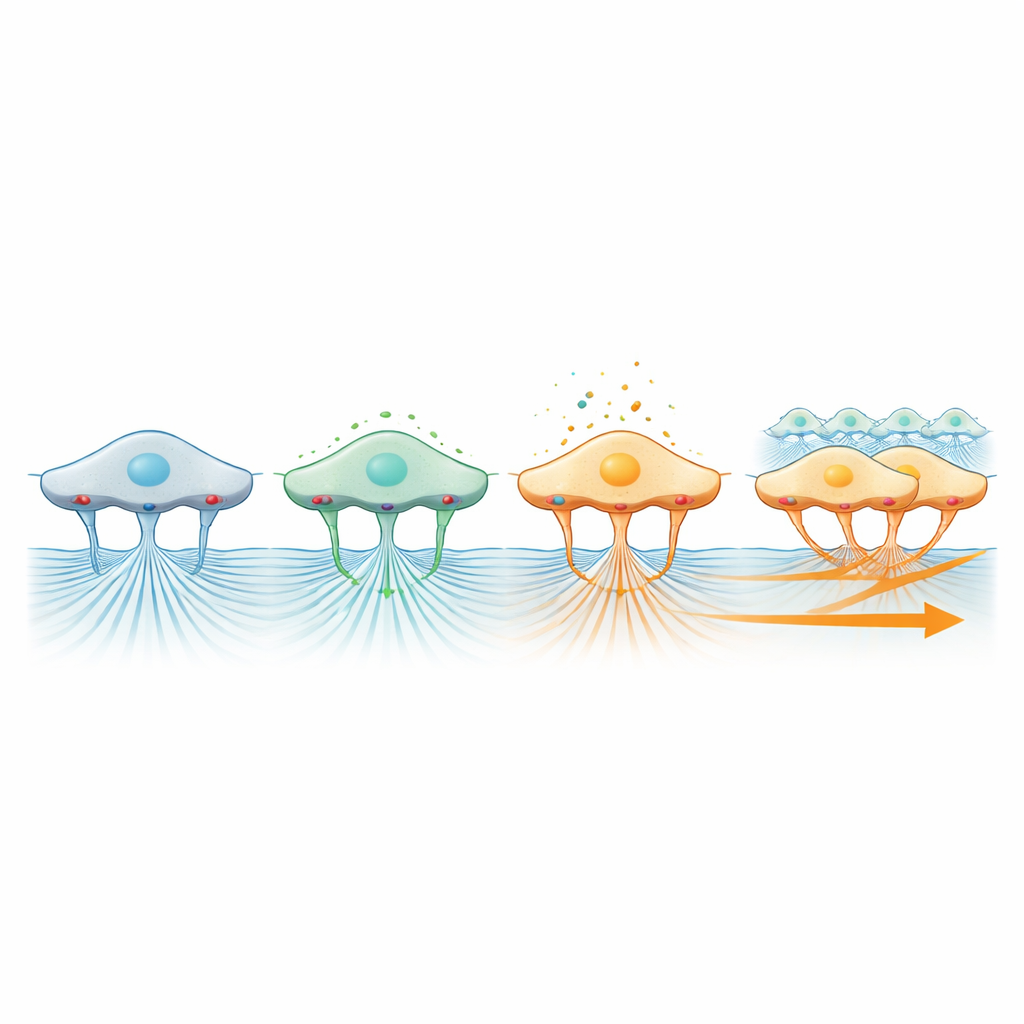
Warum das für Heilung und Krankheit wichtig ist
Kurz gesagt, diese Arbeit zeigt, dass Zellschichten nicht nur aneinander ziehen; sie ziehen auch an dem weichen Material darunter und durch dieses hindurch und nutzen es wie eine mechanische Telefonleitung. Die Kontraktionen der Zellschicht senden Spannung durch die Matrix, und diese Spannung — wahrgenommen über Integrine und Ionenkanäle und ausgelesen durch ERK-Aktivität — hilft der Gruppe, schnell und einheitlich voranzukommen. Wenn die Matrix chemisch verriegelt ist, sodass Kräfte nicht weitergeleitet werden können, oder wenn wichtige Oberflächenanker und Sensoren blockiert sind, stockt der kollektive Marsch. Diese Einsichten vertiefen unser Verständnis davon, wie Wunden schließen, wie Gewebe seine Struktur erhält und wie invasive Zellgruppen, etwa bei Krebs und Fibrose, mechanische Wege in ihrer Umgebung ausnutzen könnten, um sich auszubreiten.
Zitation: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
Schlüsselwörter: kollektive Zellmigration, mechanische Signalübertragung, extrazelluläre Matrix, Integrin, Wundheilung