Clear Sky Science · de
In-silico-Identifizierung inhalierbarer niedermolekularer IL-33/ST2-Antagonisten für schwere Typ‑2‑hohe Asthma‑Endotypen
Warum das für das Atmen wichtig ist
Für Millionen Menschen mit schwerem Asthma reichen selbst moderne Inhalatoren und fortschrittliche Injektionen oft nicht aus: Sie bleiben kurzatmig und sind weiterhin Gefahr schwerer Anfälle ausgesetzt. Diese Studie untersucht, ob bekannte, tablettenähnliche Wirkstoffe so umgestaltet werden könnten, dass sie als inhalative Behandlungen wirken und eines der früh aktivierten „Alarm“-Signale in den Lungen blockieren. Allein mithilfe von Computersimulationen suchten die Forschenden nach niedermolekularen Verbindungen, die an einen Schlüsselrezeptor binden könnten, der bei schwerem, allergisch getriebenem Asthma eine Rolle spielt – als Grundlage für spätere Laboruntersuchungen, nicht als sofort einsatzfähiges Medikament.
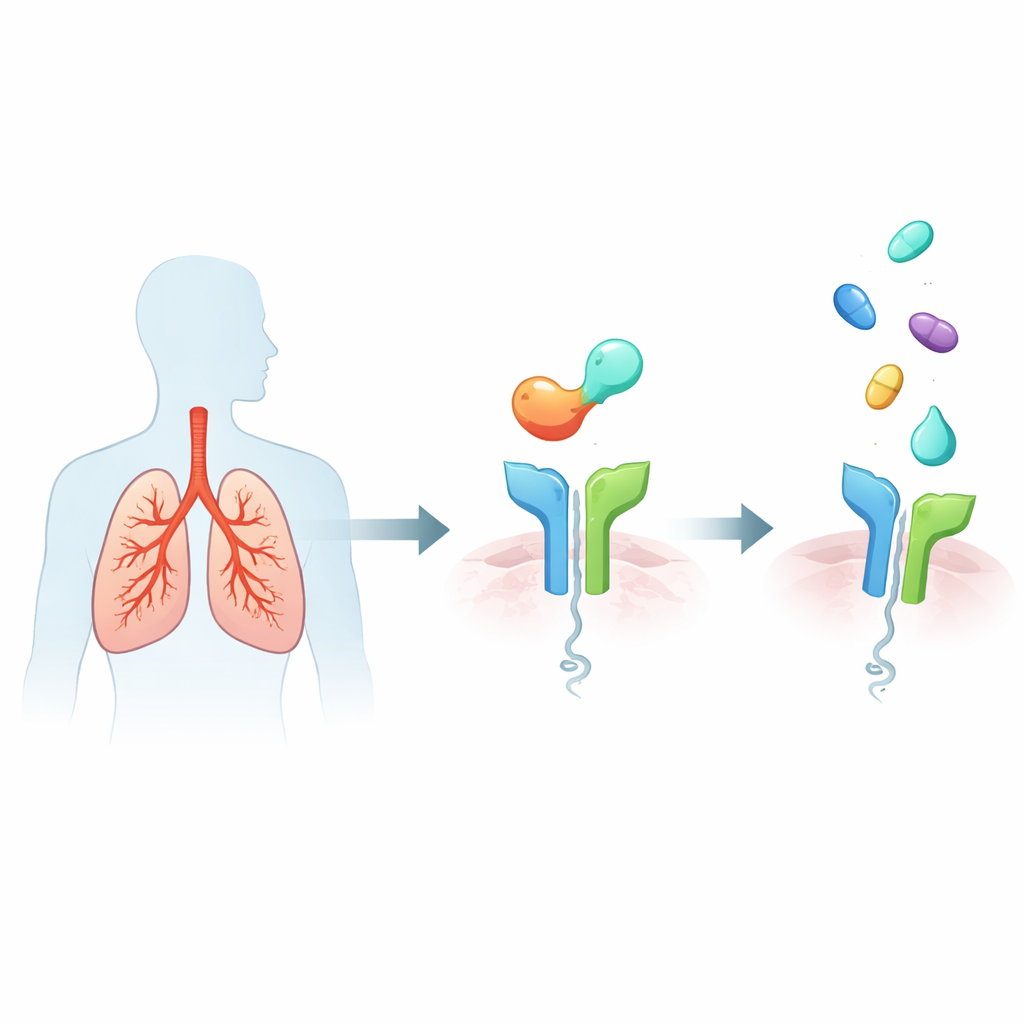
Das Alarmsystem in asthmatischen Lungen
Schweres Typ‑2‑hohes Asthma zeichnet sich durch eine überaktive Immunantwort aus, die die Atemwege mit Schleim und Entzündungszellen füllt, die Atemwege verengt und langfristig die Lungenstruktur schädigt. Ein wichtiger Auslöser ist das Protein IL‑33, das von gestressten Epithelzellen freigesetzt wird. IL‑33 bindet an einen Rezeptor namens ST2 auf verschiedenen Immunzellen, die daraufhin potente Botenstoffe ausschütten, welche typische Asthmasymptome wie Keuchen, Schübe und langfristige Umbauvorgänge der Atemwege vorantreiben. Da erhöhte IL‑33/ST2‑Aktivität mit stärkeren Symptomen und häufigeren Anfällen verbunden ist, hat sich ST2 als attraktives, upstream Ziel herauskristallisiert: Blockiert man ST2, könnte man viele der nachgeschalteten Entzündungssignale gleichzeitig dämpfen.
Von Antikörpern zu Alltags‑Wirkstoffen
Mehrere aktuelle Therapien für schweres Asthma verwenden injizierbare Antikörper, die entzündliche Proteine im Blut neutralisieren oder deren Rezeptoren blockieren. Diese biologischen Arzneimittel sind zwar für manche wirksam, jedoch teuer, müssen injiziert werden und richten sich meist gegen weiter downstream liegende Signale. Hingegen könnten niedermolekulare Wirkstoffe – eher wie traditionelle Tabletten oder Inhalatoren – großtechnisch hergestellt, leicht gelagert und möglicherweise direkt in die Lunge verabreicht werden. Die Schwierigkeit besteht darin, dass ST2 IL‑33 über eine breite Protein‑Protein‑Schnittstelle bindet, die für kleine Moleküle schwerer zu stören ist als eine tiefe Tasche an einem Enzym. Die Autorinnen und Autoren nutzten daher hochauflösende Strukturdaten des ST2–IL‑33‑Komplexes und moderne in‑silico‑Werkzeuge, um zu prüfen, ob bekannte entzündungshemmende Wirkstoffe unerwartet Teile dieser Schnittstelle greifen könnten.
Die Rezeptoroberfläche per Computer absuchen
Mithilfe der Kristallstruktur des menschlichen ST2 in komplex mit IL‑33 entfernte das Team zunächst IL‑33, um die Bindungsoberfläche des Rezeptors freizulegen, und verwendete ein Taschenfindungsprogramm, um die vielversprechendste Region für ein kleines Molekül zu identifizieren. Anschließend wählten sie zehn klinisch relevante niedermolekulare Verbindungen aus, die bereits bei Asthma oder verwandten Immunerkrankungen eingesetzt werden – etwa die Leukotrien‑Blocker Zafirlukast und Montelukast, thalidomid‑verwandte immunmodulierende Substanzen und JAK‑Inhibitoren – sowie ein zuvor berichtetes ST2‑fokussiertes Molekül als Referenz. Mit virtueller Docking‑Software platzierte man jede Verbindung tausendfach auf der ST2‑Oberfläche, und die besten Posen wurden nach vorhergesagter Bindungsstärke bewertet. Zafirlukast ergab sich als höchstrangiges Gerüst und übertraf leicht Montelukast sowie den bekannten ST2‑gerichteten Vergleichsstoff.
Ein Leitmolekül auf dem Bildschirm optimieren
Da Zafirlukast das vielversprechendste Verhältnis von vorhergesagter Bindung und allgemein wirkstoffähnlichem Verhalten zeigte, nutzten die Autorinnen und Autoren ein KI‑gestütztes Designtool, um eine modifizierte Version dieses Moleküls zu erstellen. Ziel war es, die Bindung an ST2 zu erhalten und gleichzeitig das vorhergesagte Sicherheitsprofil zu verbessern. Der neu gestaltete Analoga hatte einen sehr ähnlichen Docking‑Score und wurde in silico als weniger toxisch vorhergesagt. Detaillierte Kontaktkarten zeigten, dass sowohl das Ausgangs‑ als auch das modifizierte Molekül mehrere der gleichen ST2‑Aminosäuren berühren, die normalerweise IL‑33 kontaktieren, was darauf hindeutet, dass sie funktionell wichtige Bereiche der Schnittstelle besetzen. Ausgedehnte molekulardynamische Simulationen – eine halbe Mikrosekunde virtueller Bewegung in Wasser und Salz – zeigten, dass Rezeptor und Ligand flexibel blieben, wobei das kleine Molekül verschiedene Positionen entlang der Oberfläche einnahm, statt starr einzuschließen. Berechnungen der Wechselwirkungsenergien über die Zeit deuteten auf eine bedeutsame, aber dynamische Assoziation hin, konsistent mit einem Molekül, das eine relativ flache Protein‑Protein‑Oberfläche erkundet.
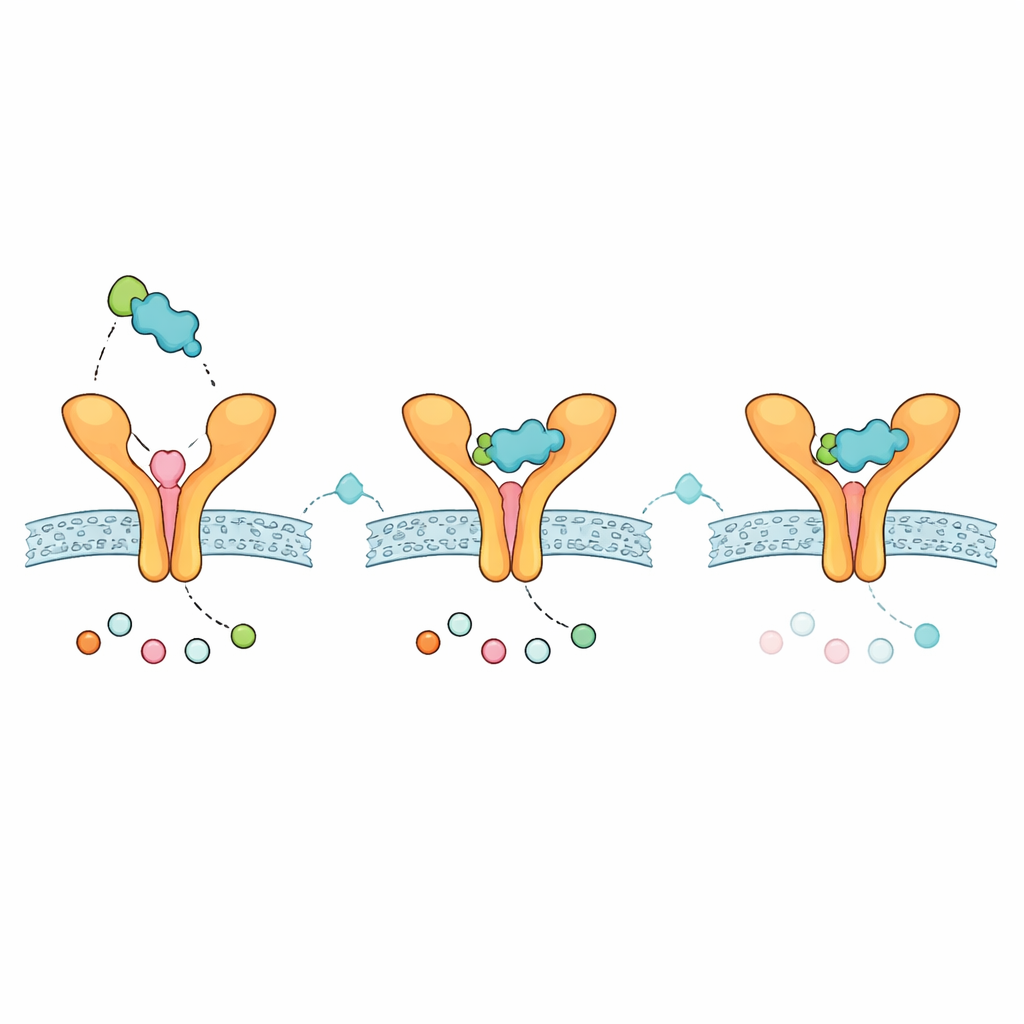
Hinweise darauf, wie ein zukünftiger Inhalator sich verhalten könnte
Um zu prüfen, ob das modifizierte Zafirlukast plausibel als Arzneimittel fungieren könnte, führten die Forschenden gängige rechnerische Prüfungen zu Absorption, Verteilung, Metabolismus, Ausscheidung und Toxizität durch. Der Analoga erfüllte übliche Regeln zur oral‑en Wirkstoffähnlichkeit, wies moderate Größe und Lipophilie auf und wurde voraussichtlich nicht ins Gehirn gelangen – Eigenschaften, die für eine lungenspezifische Behandlung mit begrenzten systemischen Nebenwirkungen günstig sein könnten. Schätzungen zur Löslichkeit variierten je nach Modell, was darauf hindeutet, dass eine sorgfältige Formulierung insbesondere für nicht‑orale Verabreichungswege wie Inhalation erforderlich wäre. Weiterhin wurde vorhergesagt, dass die Verbindung mit bestimmten Leberenzymen interagiert, was auf potenzielle Arzneimittel‑Wechselwirkungen hinweist, die berücksichtigt werden müssten, falls sie zusammen mit anderen Medikamenten eingesetzt würde.
Was diese Arbeit tatsächlich zeigt
Anstatt ein neues Asthmamedikament zu liefern, demonstriert diese Studie eine schrittweise computergestützte Strategie, um niedermolekulare Verbindungen zu finden und zu verfeinern, die das IL‑33/ST2‑Alarmsystem an der Oberfläche von Atemwegszellen stören könnten. Sie stellt Zafirlukast und ein KI‑optimiertes Verwandtes als plausible Ausgangspunkte für Laboruntersuchungen vor und zeigt, dass beide Schlüsselbereiche der ST2‑Schnittstelle besetzen und insgesamt akzeptable vorhergesagte Sicherheits‑ und Wirkstoff‑Eigenschaften besitzen. Alle Befunde sind jedoch virtuell: Die Arbeit beweist nicht, dass diese Moleküle IL‑33 tatsächlich an der Bindung an ST2 hindern, entzündliche Signale dämpfen oder Patientinnen und Patienten das Atmen erleichtern. Diese Fragen erfordern biochemische Tests, Zellstudien, Tiermodelle und schließlich klinische Studien. Bis dahin liefert die Studie eine rechnerische Roadmap und eine kurze Liste von Kandidaten‑Gerüsten für Wissenschaftlerinnen und Wissenschaftler, die den körpereigenen Asthma‑Alarmschalter in ein praktikables, inhalierbares Arzneimittelziel verwandeln möchten.
Zitation: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Schlüsselwörter: schweres Asthma, IL-33 ST2‑Signalweg, niedermolekulare Antagonisten, in‑silico Wirkstoffdesign, inhalative Therapeutika