Clear Sky Science · de
Analyse des Mechanismus und des prognostischen Werts von PRKCQ-AS1 bei der Hemmung des Fortschreitens von Lungenadenokarzinom durch Regulation des PD-1/PD-L1-Signalwegs
Warum dieses verborgene Molekül wichtig ist
Das Lungenadenokarzinom ist die häufigste Form von Lungenkrebs, und selbst mit moderner Immuntherapie erleiden zu viele Patienten Rückfälle oder sprechen nicht auf die Behandlung an. Diese Studie konzentriert sich auf ein wenig bekanntes RNA-Molekül, PRKCQ-AS1, das keine Proteine kodiert, aber möglicherweise still beeinflusst, ob Lungentumoren ungehindert wachsen oder vom Immunsystem unter Kontrolle gehalten werden. Das Verständnis dieses unsichtbaren Akteurs könnte neue Möglichkeiten für frühere Prognosen und eine gezieltere Nutzung der Immuntherapie eröffnen.
Ein leises Signal in Lungentumoren
Die Forscher begannen damit, eine große öffentliche Krebsdatenbank auszuwerten, um zu sehen, wie viel PRKCQ-AS1 in Tumorproben von Hunderten von Menschen mit Lungenadenokarzinom vorhanden ist. Sie stellten fest, dass diese RNA in Tumorgewebe durchgehend niedriger ist als im normalen Lungengewebe und dass ihre Konzentration mit dem Fortschreiten der Tumoren in spätere Stadien weiter abnimmt. Patienten, deren Tumoren weniger von dieser RNA aufwiesen, hatten über die Zeit hinweg tendenziell schlechtere Verläufe, was darauf hindeutet, dass PRKCQ-AS1 eher wie eine natürliche Bremse für den Krebs wirkt als wie Treibstoff. Das Team bestätigte dieses Muster anschließend in echten Patientenproben aus der Klinik und stärkte damit die Idee, dass PRKCQ-AS1 als nützlicher Warnhinweis für aggressivere Erkrankungen dienen könnte.
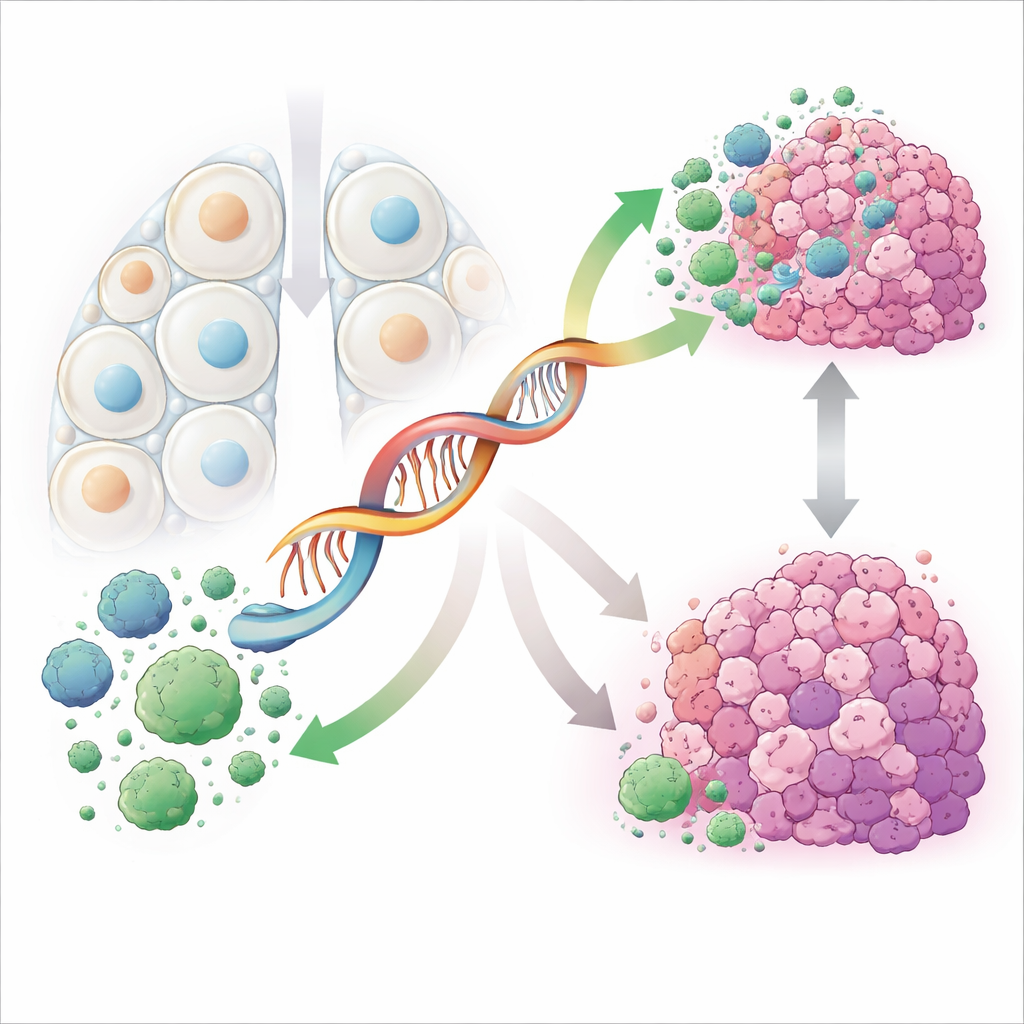
Untersuchung, wie das Molekül das Verhalten von Krebszellen prägt
Um von Datenbankmustern zur Biologie vorzudringen, arbeiteten die Wissenschaftler mit im Labor kultivierten Lungenadenokarzinomzellen. Sie erhöhten oder verringerten künstlich die PRKCQ-AS1-Spiegel und beobachteten, wie die Zellen reagierten. Bei Reduktion dieser RNA teilten sich die Krebszellen schneller, bewegten sich leichter über künstliche Barrieren und drangen aggressiver durch Membranen. Gleichzeitig unterzogen sich weniger Zellen dem programmierten Zelltod, dem Selbstzerstörungsprozess, der normalerweise beschädigte Zellen in Schach hält. Eine Erhöhung von PRKCQ-AS1 hatte den gegenteiligen Effekt: Das Wachstum verlangsamte sich, Bewegung und Invasion nahmen ab und mehr Zellen starben. Zusammen zeigen diese Experimente, dass PRKCQ-AS1 direkt mehrere charakteristische Verhaltensweisen bremst, die Lungentumoren gefährlich machen.
Verbindungen zu den Abwehrkräften des Körpers
Die Studie untersuchte außerdem, wie diese RNA die weitere Umgebung des Tumors beeinflussen könnte, insbesondere die Immunzellen, die nach abnormalem Gewebe Ausschau halten. Mithilfe computergestützter Werkzeuge erstellten die Autoren eine regulatorische Karte, die PRKCQ-AS1 mit anderen RNA-Molekülen und Genen verbindet, die an Krebs und Immunantworten beteiligt sind. Sie fanden, dass Gene, die mit dieser RNA assoziiert sind, in Signalwegen gebündelt sind, die mit Immunantworten und Zellkommunikation zu tun haben. In Patientendaten wiesen Tumoren mit höheren PRKCQ-AS1-Leveln tendenziell höhere Mengen bestimmter nützlicher Immunzellen auf, einschließlich zytotoxischer T-Zellen, die Krebszellen direkt zerstören können. Tumoren mit weniger PRKCQ-AS1 zeigten eine andere Zusammensetzung von Immunzellen, die möglicherweise weniger effektiv oder sogar erschöpft sind, was darauf hindeutet, dass diese RNA mitbestimmt, wie einladend oder feindlich die Tumorumgebung gegenüber den Abwehrkräften des Körpers ist.
Kontrolle eines wichtigen Immun-Checkpoints
Einer der mächtigsten Mechanismen, die Tumoren zu ihrem Überleben einsetzen, ist das PD-1/PD-L1-Checkpoint-System, das wie eine molekulare Tarnung wirkt und Immunzellen signalisiert, sich zurückzuhalten. Moderne Immuntherapeutika wirken, indem sie dieses Signal blockieren. Die Autoren entdeckten eine starke Verbindung zwischen PRKCQ-AS1 und diesem Checkpoint. In Patientenproben und in kultivierten Zellen ging ein niedriger PRKCQ-AS1-Spiegel einher mit höheren Werten von PD-1 und PD-L1, während eine Steigerung der RNA diese Checkpoint‑Signale senkte. Das legt nahe, dass Tumorzellen bei reichlich vorhandenem PRKCQ-AS1 weniger „Nicht angreifen“-Signale auf ihrer Oberfläche zeigen und so für Immunzellen sichtbarer werden. Bei geringem PRKCQ-AS1 ist der Checkpoint aktiver, wodurch Tumoren sich leichter vor der Immunabwehr verbergen und weiter wachsen können.
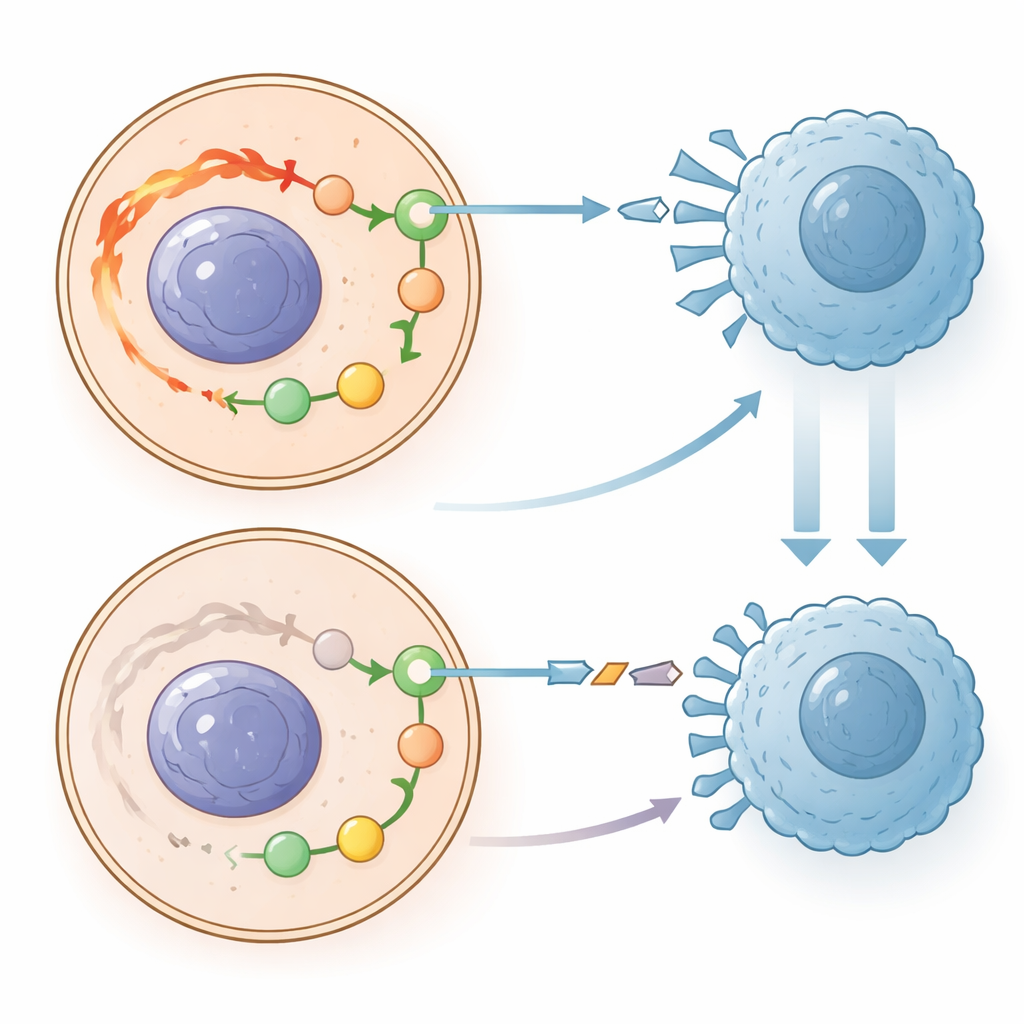
Was das für die künftige Versorgung bedeuten könnte
Obgleich diese Arbeit noch auf Zellmodellen und einer relativ kleinen klinischen Kohorte beruht, deutet sie darauf hin, dass PRKCQ-AS1 im Lungenadenokarzinom als natürlicher Tumorsuppressor wirkt. Indem diese nicht‑kodierende RNA das Krebszellwachstum hemmt und einen wichtigen Mechanismus der Immunflucht dämpft, könnte sie sowohl das Fortschreiten der Tumoren als auch das Ansprechen auf Immuntherapien beeinflussen. Künftig könnte die Messung von PRKCQ-AS1 Ärzten helfen, die Prognose eines Patienten besser einzuschätzen, und Therapien, die ihre Aktivität wiederherstellen oder nachahmen, könnten Immunbehandlungen wirksamer machen. Vorerst fügt diese Studie ein wichtiges Puzzleteil dazu, warum manche Lungenkrebserkrankungen sich der körpereigenen Abwehr entziehen — und bietet einen neuen molekularen Ansatzpunkt, um sie anzugehen.
Zitation: Wu, M., Wang, Y., He, G. et al. Analysis of the mechanism and prognostic value of PRKCQ-AS1 in inhibiting the progression of lung adenocarcinoma via regulating the PD-1/PD-L1 pathway. Sci Rep 16, 9782 (2026). https://doi.org/10.1038/s41598-026-39024-2
Schlüsselwörter: Lungenadenokarzinom, Immun-Checkpoint, lange nicht-kodierende RNA, Tumormikroumgebung, PD-1 PD-L1