Clear Sky Science · de
MUC14 unterdrückt Lungenadenokarzinom über Integrin α8β6/PI3K/AKT/MAPK und moduliert Cisplatin‑Antwort und Immunität
Warum diese Studie zum Lungenkrebs wichtig ist
Das Lungenadenokarzinom ist die häufigste Form von Lungenkrebs und wird oft mit dem Chemotherapeutikum Cisplatin behandelt. Leider entwickeln viele Tumoren Resistenzen gegen dieses Medikament, und die Langzeitüberlebenschancen bleiben gering. Diese Studie entdeckt ein wenig bekanntes zelloberflächenständiges Protein, MUC14, das offenbar als natürlicher Bremsmechanismus gegen Lungentumoren wirkt. Das Verständnis der Funktionsweise von MUC14 könnte neue Wege eröffnen, Chemotherapie wirksamer zu machen und das Immunsystem besser Tumorzellen erkennen und angreifen zu lassen.
Ein schützendes Protein, das offen sichtbar ist
MUC14, auch Endomucin genannt, sitzt auf der Zelloberfläche und gehört zu einer Familie zuckerbeschichteter Proteine, den Mucinen. Durch die Auswertung großer öffentlicher Krebsdatenbanken und die Untersuchung von Patientenproben fanden die Forschenden heraus, dass Lungenadenokarzinom‑Tumoren in der Regel deutlich weniger MUC14 produzieren als angrenzendes normales Gewebe. Patientinnen und Patienten, deren Tumoren höhere MUC14‑Spiegel aufwiesen, lebten länger und hatten ein langsameres Fortschreiten der Krankheit als solche mit niedrigen Werten. Über viele Krebsarten hinweg zeigte sich eine Tendenz zur Unterdrückung von MUC14, was darauf hindeutet, dass es häufiger als Tumor‑Blocker denn als Tumor‑Förderer wirkt. 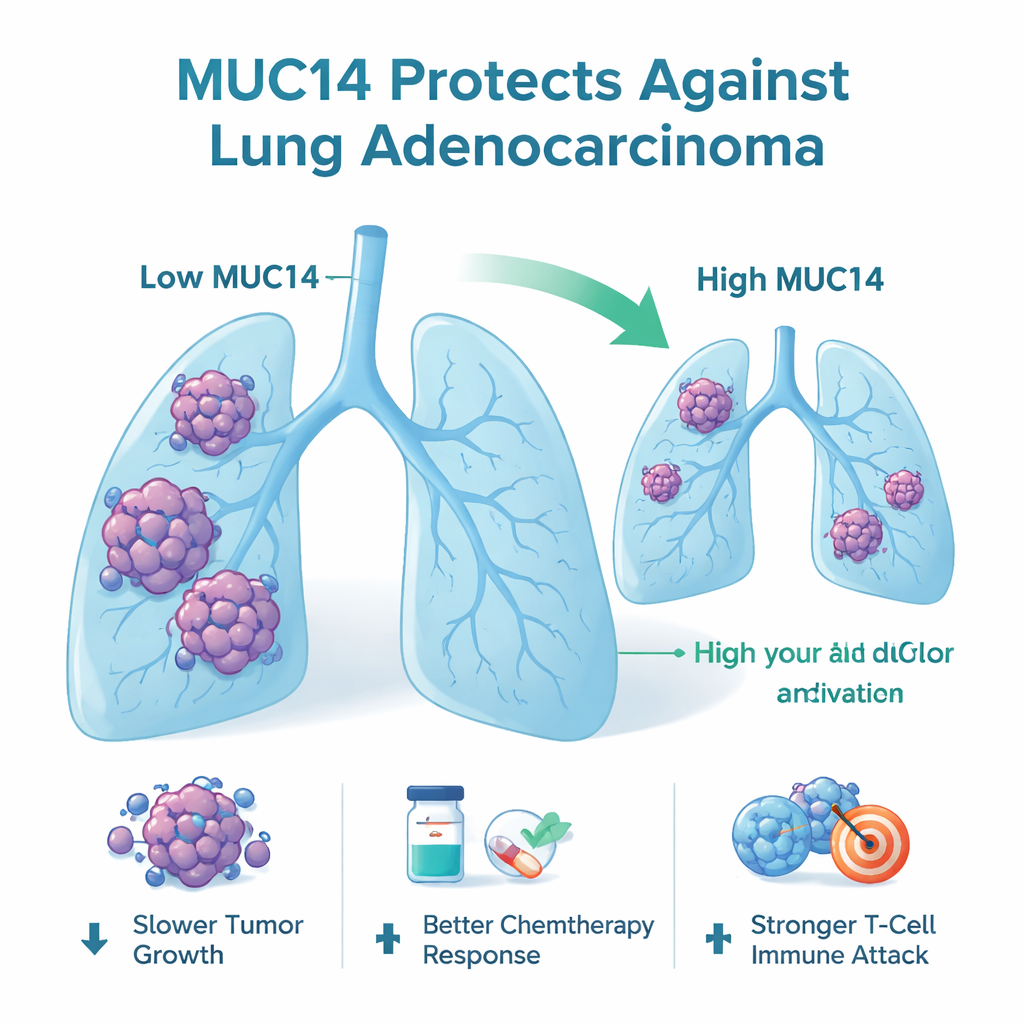
Krebszellen bremsen und Tumoren verkleinern
Um herauszufinden, was MUC14 tatsächlich bewirkt, manipulierte das Team dessen Expression in Lungenkrebs‑Zelllinien. Wenn sie die Zellen zwangen, zusätzliches MUC14 zu produzieren, teilten sich die Zellen langsamer, zeigten weniger Migration und hatten eine geringere Invasionsfähigkeit durch ein Gel, das Gewebe imitiert. Sie hafteten schlechter an wichtigen Gerüstmolekülen und bildeten weniger und kleinere Kolonien. In Mäusen bildeten Krebszellen, die so verändert waren, dass sie vermehrt MUC14 produzierten, kleinere Unterhauttumoren und führten nach Injektion in den Blutkreislauf zu weniger Lungenmetastasen. Wurde MUC14 hingegen mit kleinen interferierenden RNAs herunterreguliert, trat das Gegenteil ein: Die Zellen wuchsen schneller, bewegten sich mehr, hafteten besser und bildeten mehr Kolonien — alles Anzeichen für aggressiveres Krebsverhalten.
Wachstumssignale an der Zelloberfläche kappen
Die Autoren fragten dann, wie MUC14 diese starken Effekte vermittelt. Sie konzentrierten sich auf Integrine, eine Familie von Rezeptorproteinen, die Zellen an ihre Umgebung verankern und Wachstums‑ und Überlebenssignale in die Zelle hinein weiterleiten. Daten aus Hunderten von Lungentumoren zeigten eine starke Verbindung zwischen MUC14 und zwei Integrin‑Bausteinen, α8 und β6, die an der Zelloberfläche zusammenwirken. Mit einer lichtbasierten Technik, die Proteine in Abständen von Milliardsteln Metern zueinander nachweist, bestätigten die Forschenden, dass MUC14 und der α8β6‑Integrinkomplex nebeneinander in der Zellmembran sitzen. Zusätzliches MUC14 störte das Zusammenklumpen dieser Integrine und dämpfte zwei zentrale Wachstumswege, die sie normalerweise speisen: PI3K/AKT und MAPK/ERK. Bei reduziertem MUC14 wurden diese Signalwege aktiver, was erklärt, warum Krebszellen leichter wachsen und sich ausbreiten konnten. 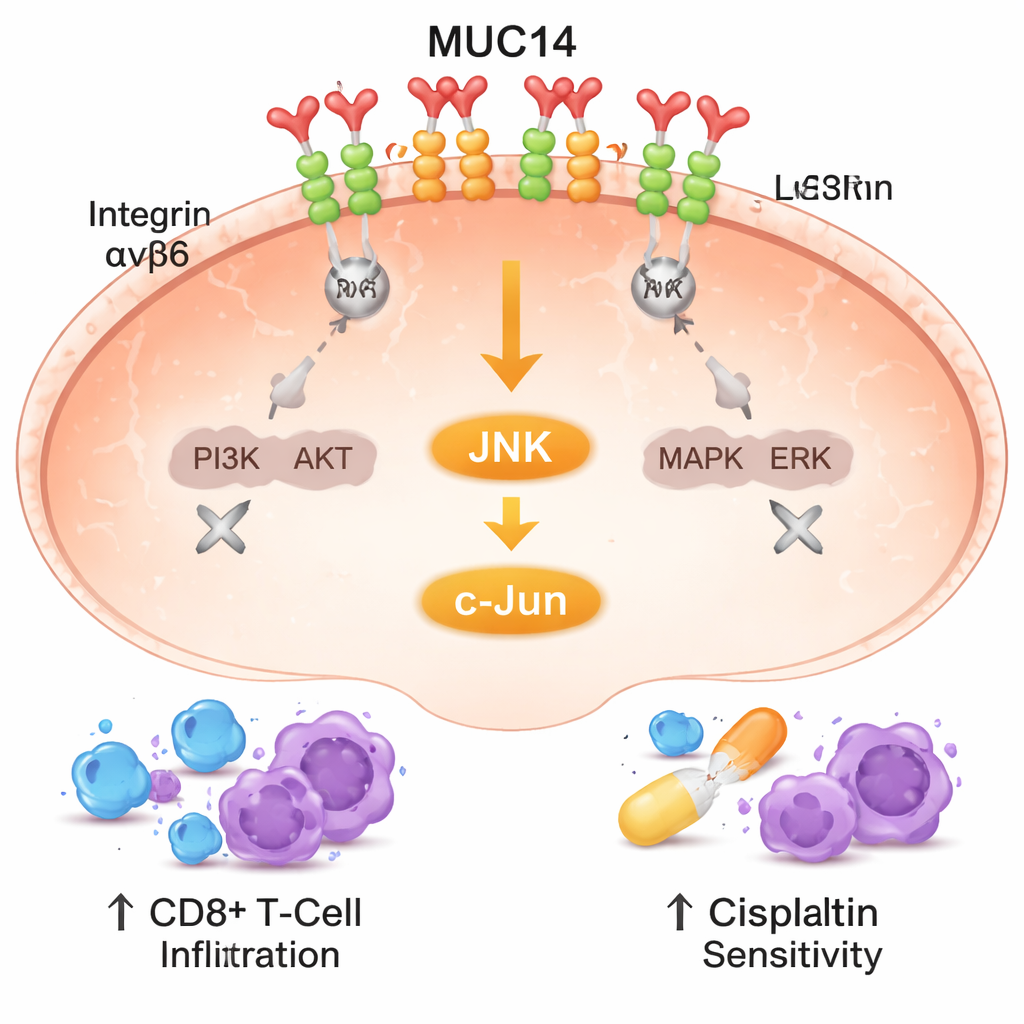
Immunsystem und Chemotherapie zusammen stärken
Der Krankheitsverlauf wird nicht nur von den Tumorzellen selbst, sondern auch von den angrenzenden Immunzellen beeinflusst. Durch die Analyse von Immunprofil‑Datenbanken und die Anfärbung menschlicher Tumorschnitte fanden die Forschenden heraus, dass Tumoren mit höheren MUC14‑Spiegeln mehr CD3+ und CD8+ T‑Zellen aufwiesen — Immunzellen, die Tumorzellen direkt abtöten können — in unmittelbarer Nähe zu MUC14‑positiven Tumorregionen. Das deutet darauf hin, dass MUC14 eine günstigere Umgebung für immunologische Angriffe schafft. Außerdem untersuchten die Forschenden Cisplatin, ein Standardmedikament beim Lungenadenokarzinom. In Zellkultur benötigten Tumoren mit zusätzlichem MUC14 deutlich geringere Cisplatin‑Dosen zur Hemmung, während Zellen ohne MUC14 resistenter gegenüber dem Medikament wurden. Wichtig ist, dass MUC14 die Zellen nicht einfach anfälliger für spontanen Zelltod machte; vielmehr verstärkte es die Wirkung von Cisplatin, teils durch Aktivierung eines Stresswegs, bekannt als JNK/c‑Jun, der durch DNA‑Schäden ausgelöst wird.
Auf dem Weg zu klügeren Kombinationen in der Lungenkrebsbehandlung
Kurz gesagt zeichnet diese Arbeit MUC14 als eingebautes Abwehrsystem gegen Lungenadenokarzinom. Wenn es vorhanden ist, blockiert es zentrale Wachstums‑Schaltstellen an der Zelloberfläche, verlangsamt die Tumorausbreitung, zieht krebsbekämpfende T‑Zellen an und verstärkt die Wirkung von Cisplatin, ohne in Tierversuchen zusätzlichen Organschaden zu verursachen. Geht es verloren, werden Tumoren widerstandsfähiger, beweglicher und weniger ansprechbar auf Standardtherapien. Die Ergebnisse legen nahe, dass die Messung von MUC14 Prognose und Therapieansprechen vorhersagen könnte und dass künftige Therapien, die MUC14‑Aktivität erhöhen oder ihre Wirkung auf die Integrin‑Signalgebung nachahmen, es Ärzten ermöglichen könnten, Chemotherapie und Immuntherapie bei Patientinnen und Patienten mit fortgeschrittenem Lungenkrebs wirkungsvoller zu kombinieren.
Zitation: Li, X., Li, M., Huang, S. et al. MUC14 suppresses lung adenocarcinoma via integrin α8β6/PI3K/AKT/MAPK modulating cisplatin response and immunity. Sci Rep 16, 7784 (2026). https://doi.org/10.1038/s41598-026-39019-z
Schlüsselwörter: Lungenadenokarzinom, MUC14, Cisplatinresistenz, Integrin‑Signalgebung, Tumorimmunität