Clear Sky Science · de
Aus Bienenpollen abgeleitetes Peptid mit dualer DPP‑IV‑Hemmung und Modulation des Glukosetransports
Warum Bienenpollen für den Blutzucker relevant sein könnte
Typ‑2‑Diabetes wird oft als Problem zu viel Zuckers und zu wenig Insulin dargestellt, doch im Hintergrund steuert ein Geflecht aus Enzymen und Transportern, wie unser Körper Glukose verarbeitet. Diese Studie untersucht eine faszinierende Idee: dass Bienenpollen, ein natürliches „Superfood“, eine Quelle winziger Proteinfragmente (Peptide) sein könnte, die sowohl Hormonsignale schützen, welche den Blutzucker regulieren, als auch die Aufnahme von Zucker aus dem Darm feinjustieren. Die Arbeit konzentriert sich auf ein solches Peptid, AA‑7 genannt, und fragt, ob es eines Tages sichere, ernährungsbasierte Strategien zur Unterstützung der Diabeteskontrolle inspirieren könnte.
Vom Bienenstock zur Laborbank
Bienenpollen ist ein Gemisch aus Pflanzenpollen und bienenabhängigen Bestandteilen, reich an Proteinen, Vitaminen und anderen Nährstoffen. Um die menschliche Verdauung nachzuahmen, behandelten die Forscher die Bienenpollenproteine mit zwei Verdauungsenzymen, Pepsin und Pankreatin, ähnlich denen im Magen und Dünndarm. Dieser Prozess zerlegte große Proteine in viele kleinere Stücke, einige nur wenige Aminosäuren lang. Anschließend trennten sie diese Fragmente nach Größe und chemischen Eigenschaften und testeten jede Fraktion auf ihre Fähigkeit, ein Enzym namens DPP‑IV zu blockieren, das normalerweise Hormone aufspaltet und inaktiviert, die die Insulinausschüttung anregen. Eine Fraktion sehr kleiner, relativ fettliebender (hydrophober) Peptide fiel durch starke DPP‑IV‑hemmende Aktivität besonders auf. 
Ein herausragendes Peptid finden
Mithilfe hochauflösender Massenspektrometrie identifizierte das Team ein sieben Aminosäuren langes Peptid mit der Sequenz Ala‑Thr‑His‑Ala‑Leu‑Leu‑Ala, das sie AA‑7 nannten. Sie synthetisierten dieses Peptid, um es isoliert zu testen. In Enzymtests hemmte AA‑7 DPP‑IV im Mikromolarbereich, etwas schwächer als ein gängiges Labormedikament, aber vergleichbar mit oder besser als viele in der Fachliteratur berichtete nahrungsbedingte Peptide. Durch Untersuchung der Reaktionsgeschwindigkeit bei unterschiedlichen Peptid‑ und Substratkonzentrationen zeigten sie, dass AA‑7 als kompetitiver Inhibitor wirkt: Es besetzt die gleiche aktive Tasche von DPP‑IV wie die natürlichen Substrate und behindert sie, ohne das Enzym zu zerstören.
Peptid‑Enzym‑Interaktionen auf atomarer Ebene
Um zu verstehen, warum AA‑7 wirkt, nutzten die Forscher Computersimulationen, um das Peptid in ein dreidimensionales Modell von DPP‑IV zu docken, und führten anschließend Molekulardynamik‑Simulationen über die Zeit durch. Die Modelle deuteten darauf hin, dass AA‑7 sich in die katalytische Tasche des Enzyms einbettet und Kontakt zu Schlüsselaminosäuren hat, die bereits als wichtig für die Aktivität von DPP‑IV bekannt sind. Die Bindung wurde als mindestens ebenso stabil wie die eines Referenzinhibitors vorhergesagt. Weitere Computeranalysen zu Absorption, Verteilung, Metabolismus und Toxizität (ADMET) gaben einen realistischen Hinweis: AA‑7 ist wahrscheinlich sicher, wird aber in seiner unveränderten Form nicht effizient durch die Darmwand aufgenommen—eine häufige Beschränkung kleiner Peptide. Das macht deutlich, dass Lieferstrategien oder strukturelle Modifikationen nötig wären, falls AA‑7 oder darauf basierende Moleküle beim Menschen eingesetzt werden sollen.
Die Regulierung der Zuckeraufnahme im Darm
Die Studie blieb nicht bei Reaktionen im Reagenzglas stehen. Das Team setzte kultivierte menschliche Darmzellen (Caco‑2‑Zellen) AA‑7 aus und maß sowohl die Glukoseaufnahme als auch die Aktivität der Gene, die für zwei hauptsächliche intestinale Glukosetransporter kodieren, SGLT1 und GLUT2. Bei nicht toxischen Dosen veränderte AA‑7 die Geschwindigkeit, mit der eine fluoreszente Form von Glukose in die Zellen gelangte, wobei die Effekte dosis‑ und zeitabhängig waren. Es veränderte auch die Expression von SGLT1‑ und GLUT2‑Genen unterschiedlich über kurze (30 Minuten) und längere (24 Stunden) Zeiträume. Computer‑Docking deutete darauf hin, dass AA‑7 mit strukturellen Regionen dieser Transporter interagieren kann, wobei diese Modelle eher Hypesen als endgültige Beweise darstellen. Zusammen deuten die Zell‑ und Modellierungsdaten darauf hin, dass AA‑7 mehr tut als nur DPP‑IV zu blockieren—es beeinflusst auch die Mechanismen, die Zucker aus dem Darm ins Blut transportieren. 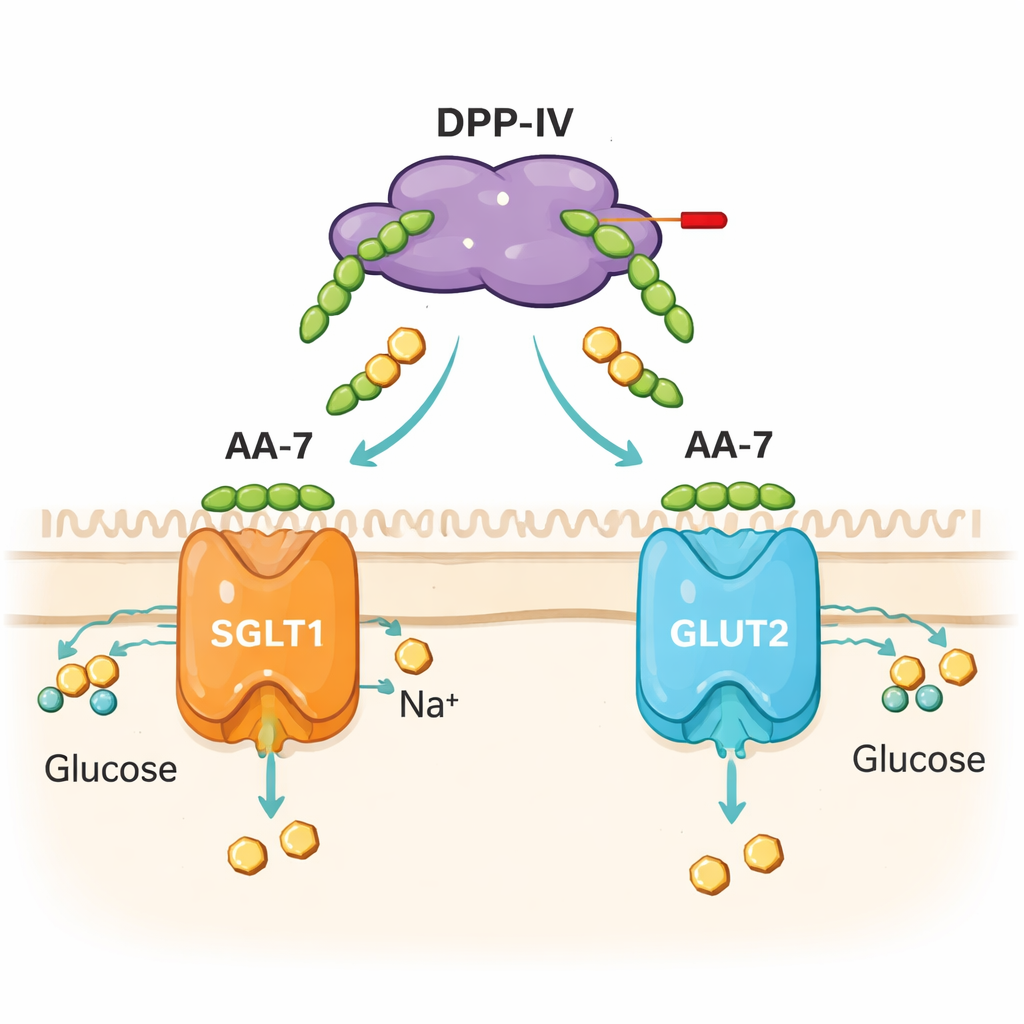
Was das für zukünftige Lebensmittel bedeuten könnte
Für Nicht‑Fachleute lautet die Kernaussage, dass das Bienenpollenpeptid AA‑7 offenbar auf zwei Ebenen relevant für Typ‑2‑Diabetes wirkt: Es verlangsamt ein Schlüsselenzym, das insulinstimulierende Hormone abbaut, und es beeinflusst, wie Darmzellen Glukose aufnehmen. Für sich genommen ist AA‑7 nicht bereit, ein Medikament oder Nahrungsergänzungsmittel zu sein, unter anderem weil es möglicherweise nicht effizient aufgenommen wird. Es weist jedoch auf Bienenpollen—und vielleicht auf andere proteinreiche Lebensmittel—als Reservoirs kleiner, multitaskingfähiger Peptide hin, die neue funktionelle Lebensmittel oder peptidbasierte Therapien inspirieren könnten. Mit weiterer Forschung an Tieren und Menschen und besseren Wegen, solche Peptide zu liefern, könnte ein derart dual wirkendes Molekül Teil eines nuancierteren, an der Ernährung orientierten Ansatzes zur Blutzuckerregulation werden.
Zitation: Mongkolnkrajang, U., Kuptawach, K., Sangtanoo, P. et al. Bee pollen-derived peptide with dual DPP-IV Inhibition and glucose transport modulation. Sci Rep 16, 7616 (2026). https://doi.org/10.1038/s41598-026-39009-1
Schlüsselwörter: Bienenpollen‑Peptide, DPP‑IV‑Hemmung, Glukosetransport, Typ‑2‑Diabetes, funktionelle Lebensmittel