Clear Sky Science · de
Strukturgestützte Modellierung enthüllt die molekulare Grundlage für die neuartige Aktivität von CYP153A6 gegenüber Toluen-Derivaten
Schwierige chemische Aufgaben an die Natur abgeben
Chemiker und die Industrie sind auf Reaktionen angewiesen, die Sauerstoff in hartnäckige Kohlenstoff–Wasserstoff-Bindungen einfügen — etwa um Schadstoffe abzubauen oder Ausgangsstoffe für Arzneimittel und Duftstoffe herzustellen. Das sauber, ohne aggressive Chemikalien oder Schwermetallabfälle zu bewerkstelligen, ist schwierig. Diese Studie betrachtet einen natürlichen Katalysator, ein Enzym namens CYP153A6 aus einem Bodenbakterium, und stellt eine einfache Frage mit großen Folgen: Lässt sich dieses Enzym so lenken, dass es Toluen‑ähnliche Chemikalien — gängige Bestandteile von Treibstoffen und Lösungsmitteln — selektiv in nützlichere und umweltfreundlichere Produkte umwandelt?
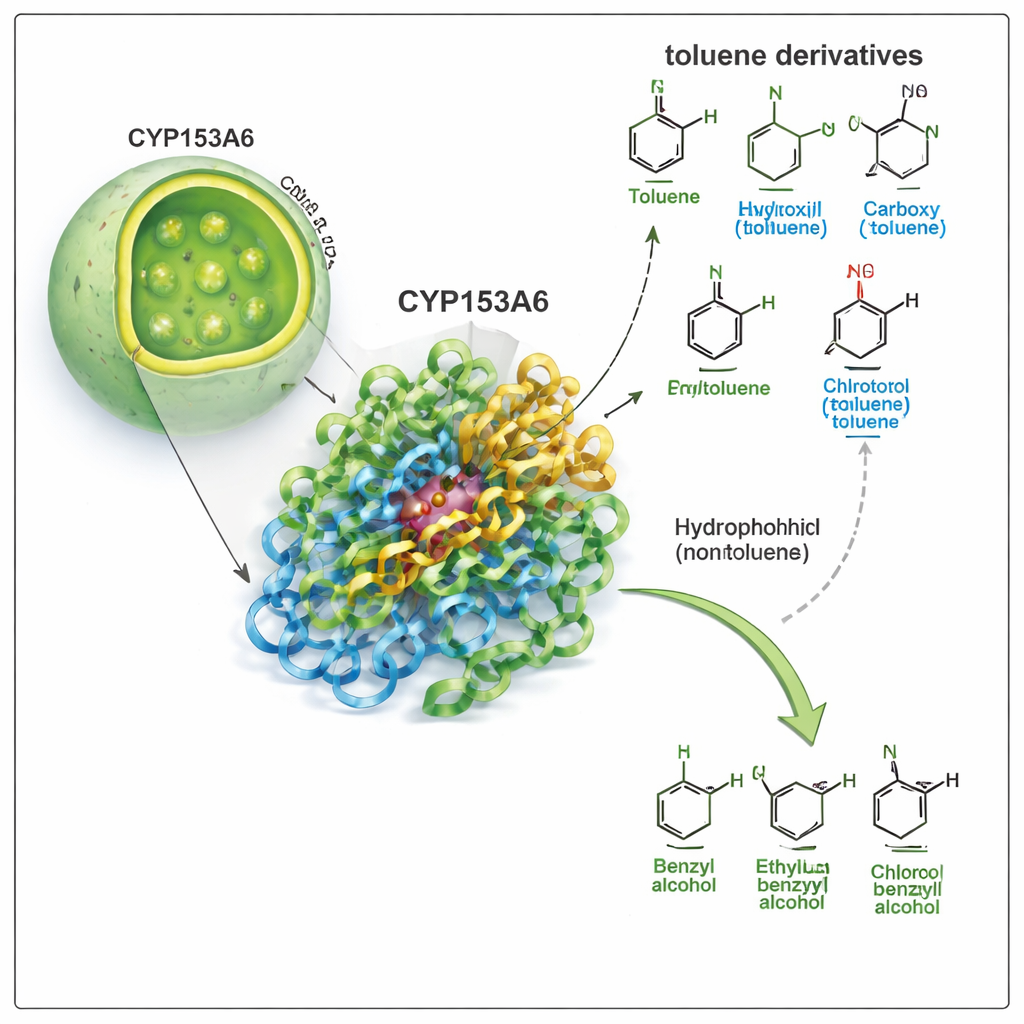
Ein Enzym, das eine einzige Stelle auswählt
CYP153A6 gehört zur großen Familie der Cytochrom‑P450‑Enzyme, den vielseitigen Oxidationsspezialisten der Natur. Im Unterschied zu vielen industriellen Katalysatoren arbeitet dieses Enzym im Wasser, bei moderaten Temperaturen, und greift sehr spezifische Positionen an einem Molekül an. Frühere Arbeiten zeigten, dass CYP153A6 Sauerstoff an die Enden einfacher Kohlenwasserstoffketten und an bestimmte pflanzliche Duftstoffe anfügt. Hier fragen die Autoren, ob es auch die „benzyliche“ Position — die kleine Seitenkette an einem Benzolring — bei Toluol und verwandten Verbindungen angreifen kann. Diese Umwandlung macht Toluen‑Derivate zu Benzylalkoholen, wertvollen Bausteinen für Pharmazeutika, Aromen und Feinchemikalien.
Ausprobieren, welche Moleküle das Enzym mag
Das Team führte zunächst Biotransformations‑Experimente mit gentechnisch veränderten E. coli-Zellen durch, die CYP153A6 produzieren, sowohl als intakte Zellen als auch als zellfreie Extrakte. Sie setzten das Enzym einer Reihe von Toluen‑Derivaten aus, variierten die Gruppe am aromatischen Ring (beispielsweise Methyl, Chlor, Methoxy, Hydroxyl oder Nitro) und deren Stellung (para, meta oder ortho). Das Enzym arbeitete sehr gut an apolaren oder nur wenig polaren Verbindungen wie p‑Cymen, p‑Xylol, p‑Methylanisol und p‑Chlortoluol und verwandelte konsistent die benzyliche Methylgruppe in ein Benzylalkohol. Auffällig ignorierte es stärker polare Moleküle wie p‑Cresol, p‑Methylbenzylalkohol und p‑Nitrotoluol vollständig, obwohl diese strukturell ähnlich sind. Dieses Muster deutete darauf hin, dass die Taschenstruktur des Enzyms stark hydrophob ist und polare Gruppen benachteiligt.
Eine 3D‑Karte der molekularen Maschine erstellen
Da die dreidimensionale Struktur von CYP153A6 experimentell nicht bestimmt war, bauten die Forscher ein hochwertiges Computermodell auf Grundlage eines eng verwandten P450, dessen Struktur bekannt ist. Sie validierten das Modell durch Überprüfung der Geometrie und durch lange Molekulardynamik‑Simulationen, um zu sehen, ob das Protein über die Zeit stabil bleibt — was der Fall war. Die Simulationen zeigten ein verborgenes aktives Zentrum, das durch enge Tunnel mit dem Außenbereich verbunden ist, durch die Substrate eintreten und Produkte entweichen. Diese Tunnel werden von flexiblen Schleifen an der Proteinoberfläche geformt und verschlossen, was erklärt, wie das Enzym hydrophobe Moleküle bis zum reaktiven Häm‑Eisen führen kann, während Wasser und oxidierte Produkte entweichen können.
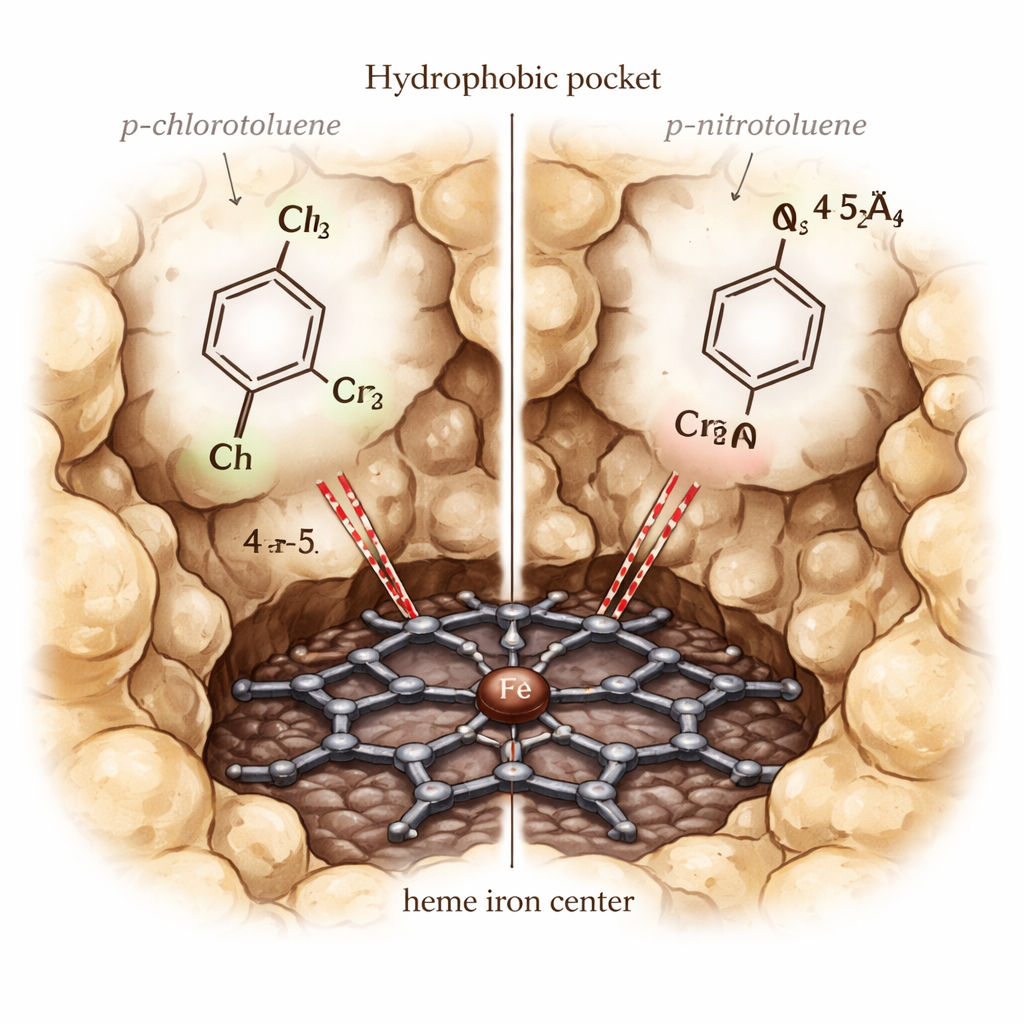
Zusehen, wie Moleküle andocken, sich bewegen und reagieren
Mit dem Modell in der Hand simulierten die Autoren, wie verschiedene Toluen‑Derivate in CYP153A6 binden. Sie verwendeten einen Ansatz namens Ensemble‑Docking, bei dem viele leicht unterschiedliche Proteinformen und mehrere Elektronenzustände des Häm‑Eisens getestet wurden, um herauszufinden, welche Konfigurationen echte Substrate von Nicht‑Substraten unterscheiden. Das erfolgreichste Szenario nutzte das Eisen im ruhenden ferrischen Zustand und keine zusätzlichen Wassermoleküle in der Tasche und bevorzugte korrekt die bekannten Substrate. Folgesimulationen verfolgten Bild für Bild, wie jedes Molekül relativ zum Häm lag. Gute Substrate wie p‑Cymen und p‑Xylol blieben nahe am Eisen mit der benzylichen Methylgruppe in dessen Richtung, und ihre vorhergesagten Bindungsenergien waren stark günstig. Schlechte Substrate drifteten eher weg, nahmen ungünstige Orientierungen ein oder wechselwirkten ungünstig mit den überwiegend öligen Seitenketten, die die Tasche auskleiden.
Warum ein fast identischer Stoff reagiert und ein anderer nicht
Ein Rätsel fiel besonders auf: p‑Chlortoluol wird von CYP153A6 effizient oxidiert, während p‑Nitrotoluol dies nicht wird, obwohl beide in die Tasche passen und in den Simulationen ähnlich stark binden. Zur Aufklärung führten die Autoren detailliertere Quant‑Mechanik/Molekül‑Mechanik‑(QM/MM)‑Berechnungen im hochreaktiven „Compound I“‑Zustand des Enzyms durch. Diese Rechnungen zeigten, dass die Nitrogruppe so viel Elektronendichte vom benzylichen Kohlenstoff wegzieht, dass dessen Oxidation trotz günstiger Geometrie sehr schwer wird. Im Gegensatz dazu erlaubt die Chlorsubstitution eine bessere elektronische Kopplung zwischen Häm und Substrat, sichtbar in höherer Spin‑Dichte am aromatischen Ring und an der Methylgruppe sowie in einer reaktiveren Ausrichtung für den kritischen Wasserstoff‑Abstraktionsschritt.
Was das für sauberere Chemie bedeutet
Alltagsnah ausgedrückt verhält sich CYP153A6 wie ein winziger, öliger Handschuh, der bestimmte kraftstoffähnliche Moleküle so hält, dass an einer genau definierten Stelle Sauerstoff eingeführt werden kann — wodurch sie wasserlöslicher, nützlicher und letztlich besser abbaubar werden. Die Studie zeigt, dass das Enzym unpolare Substituenten bevorzugt und dass sowohl Form als auch Elektronenfluss darüber entscheiden, ob ein bestimmtes Toluen‑Derivat umgesetzt wird. Indem sie klären, wie CYP153A6 diese Moleküle erkennt und aktiviert, liefert die Arbeit eine Blaupause für das Engineering verbesserter Varianten, die helfen könnten, aromatische Schadstoffe abzubauen oder komplexe Chemikalien nachhaltiger herzustellen.
Zitation: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Schlüsselwörter: Biokatalyse, Cytochrom P450, Toluol-Hydroxylierung, Enzymtechnologie, grüne Chemie