Clear Sky Science · de
Transplastomische Biofabrik zur Produktion von funktionellem menschlichem α‑Laktalbumin für ernährungs- und therapeutische Anwendungen
Pflanzen zu Milchproteinproduzenten machen
Moderne Ernährungsweisen sind stark von Milchproteinen abhängig, doch die weltweite Viehhaltung bringt Umweltkosten und ethische Fragen mit sich. Diese Studie untersucht einen ganz anderen Weg zur Herstellung eines wichtigen menschlichen Milchproteins — indem man Pflanzenblättern beibringt, es zu produzieren. Die Arbeit zeigt, dass Tabakpflanzen so umprogrammiert werden können, dass sie menschliches α‑Laktalbumin herstellen, ein Protein, das für die Säuglingsernährung wichtig ist und potenziell krebshemmende Eigenschaften besitzt. Das eröffnet einen Weg zu tierfreien Zutaten für Babynahrung und neuen, krebsbekämpfenden Lebensmittelkomponenten.
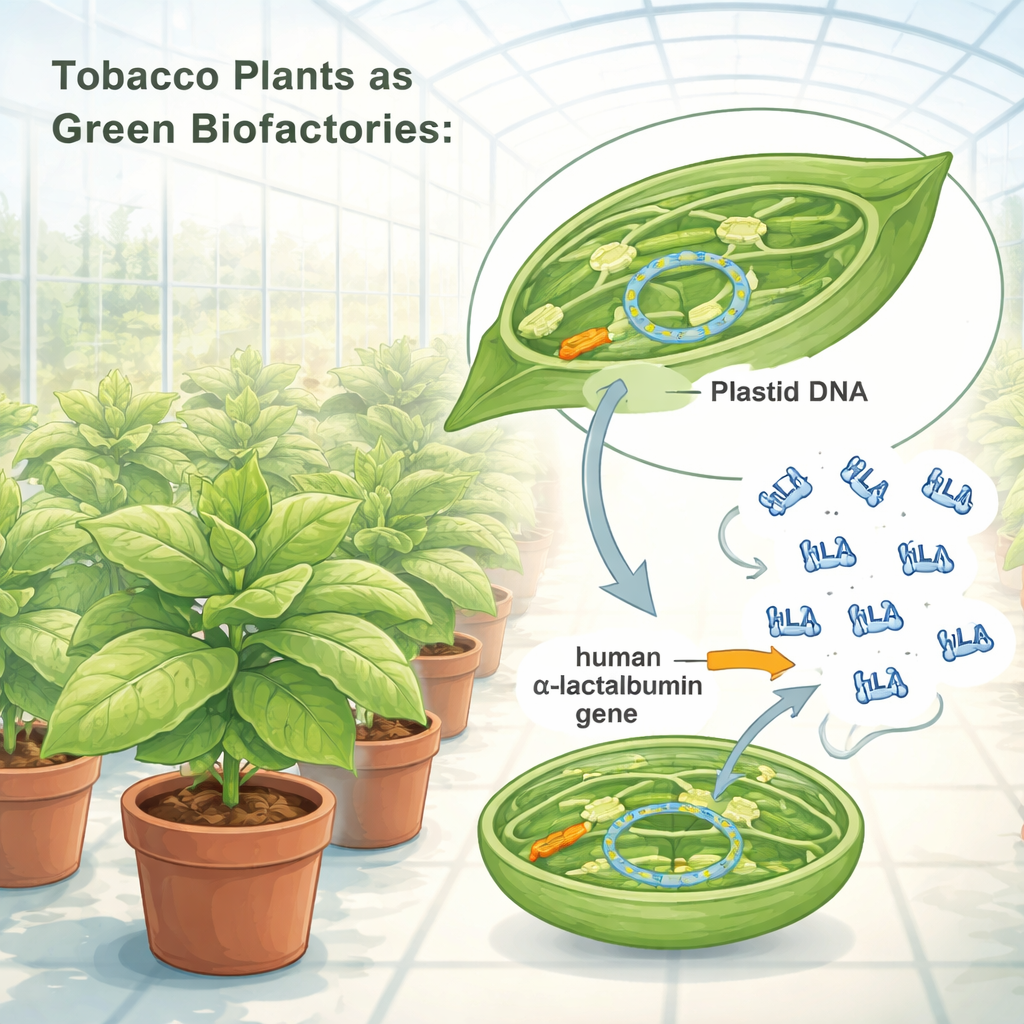
Warum dieses Milchprotein wichtig ist
Muttermilch ist mehr als nur Nahrung; sie ist ein fein abgestimmter Cocktail aus Proteinen, Fetten und Zuckern, der sich an die Bedürfnisse des Säuglings anpasst. Eines ihrer wichtigsten Proteine ist α‑Laktalbumin, das bei der Bildung von Laktose hilft, dem Hauptzucker in Milch und einer entscheidenden Energiequelle für Babys. α‑Laktalbumin ist reich an essentiellen Aminosäuren, einschließlich Tryptophan, einem Baustein für das im Gehirn wirkende "Wohlfühl"-Molekül Serotonin, und wurde mit besserer Stressresilienz sowie möglichem Schutz vor bestimmten Krebsarten in Verbindung gebracht. Da es leicht verdaulich ist, einen milden Geschmack hat und über einen weiten Säurebereich stabil bleibt, wird es häufig in Säuglingsanfangsnahrung und Ernährungsdrinks verwendet — und die Nachfrage steigt.
Das Problem der traditionellen Milchproduktion
Die Abhängigkeit von Kühen zur Bereitstellung von Milchproteinen hat Nachteile. Nutztiere verursachen einen erheblichen Anteil der globalen Treibhausgasemissionen, und große Milchbetriebe benötigen enorme Flächen, Wasser und Futter. Hinzu kommen Bedenken, dass Hormone, Antibiotika und Krankheitserreger über die Milch eingeführt werden können. Diese Probleme haben das Interesse an "zellularer Landwirtschaft" geweckt, bei der Milchproteine von Mikroben oder kultivierten Zellen statt von Tieren hergestellt werden. Viele dieser Systeme sind jedoch noch teuer, schwer skalierbar oder produzieren Proteine, die nicht ganz identisch mit den menschlichen Versionen sind. Pflanzen, insbesondere ihre Chloroplasten in den Blättern — die winzigen grünen Fabriken der Photosynthese — bieten eine vielversprechende Alternativplattform.
Umprogrammierung von Chloroplasten zu Biofabriken
Die Forschenden gestalteten die genetischen Anweisungen für menschliches α‑Laktalbumin so um, dass Tabakchloroplasten sie effektiv lesen können. Sie setzten dieses optimierte Gen in die Chloroplasten-DNA ein, mithilfe einer "Genkassette", die aus starken pflanzlichen Regulations‑Elementen besteht und wie kraftvolle Ein-/Ausschalter wirkt. Mittels Partikelbeschuss wurde diese Kassette in Tabakblattzellen eingebracht, danach wurden Pflanzenkeimlinge ausgewählt, deren Chloroplasten das neue Gen vollständig übernommen hatten. Genetische Tests bestätigten, dass alle Kopien der Chloroplasten‑DNA in diesen Pflanzen nun den Bauplan für das menschliche Protein trugen. Die veränderten Pflanzen wuchsen im Gewächshaus normal, produzierten Samen und zeigten keine sichtbaren Einbußen bei Größe, Form oder Fruchtbarkeit, was darauf hindeutet, dass die zusätzliche Proteinbelastung die Pflanzengesundheit nicht beeinträchtigte.
Nachweis, dass das pflanzengefertigte Protein funktioniert
Als Nächstes prüfte das Team, ob das pflanzengefertigte α‑Laktalbumin wie das echte menschliche Protein wirkt. Sie extrahierten lösliche Proteine aus den Blättern, reinigten das α‑Laktalbumin und untersuchten seine Struktur mit einer Technik, die Auskunft über die Faltung von Proteinen gibt. Der Spektral‑"Fingerabdruck" des pflanzlichen Proteins überlappte nahezu mit dem des kommerziellen menschlichen α‑Laktalbumins, was auf eine ähnliche Faltung hindeutet. Funktionell aktivierte das pflanzengefertigte Protein die laktosesynthesiserende Enzymaktivität fast ebenso gut wie die native Version und trieb die Laktosebildung mit etwa 93 % der Rate des Standardproteins voran. Bemerkenswert war, dass α‑Laktalbumin auf etwa 23 % des gesamten löslichen Proteins in den Blättern akkumulierte — einer der höchsten berichteten Werte für menschliche Proteine, die in Pflanzenchloroplasten hergestellt wurden — was darauf hindeutet, dass dieses System industriell relevante Ausbeuten liefern kann.
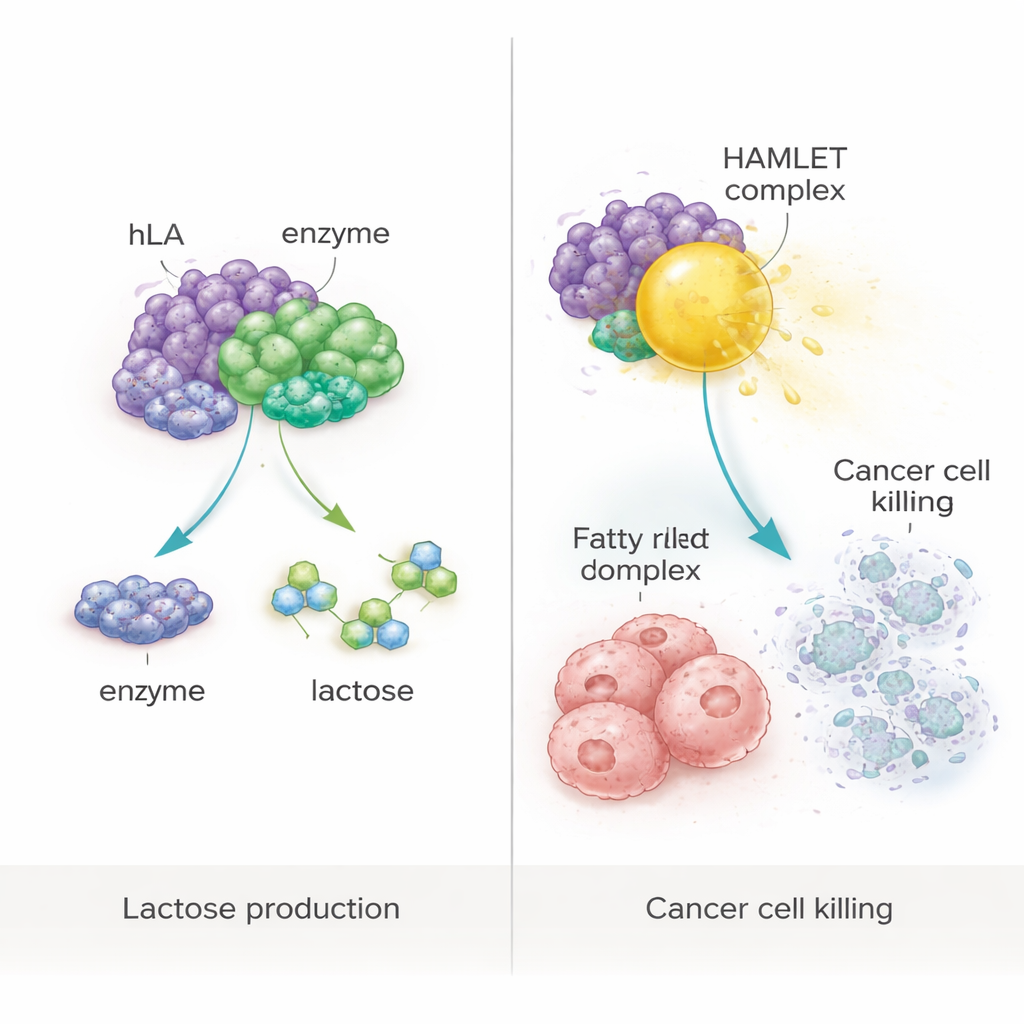
Von Ernährung zu krebsbekämpfenden Komplexen
Die Studie prüfte auch eine ambitioniertere Idee: das pflanzengefertigte Protein als Baustein für einen bekannten anti‑tumoralen Komplex namens HAMLET zu verwenden, der entsteht, wenn α‑Laktalbumin fest an Ölsäure bindet, eine häufige Fettsäure. Durch schonendes Erhitzen des gereinigten pflanzlichen Proteins mit Ölsäure unter kontrollierten Bedingungen erzeugten die Forschenden einen HAMLET‑ähnlichen Komplex. Bei Anwendung auf menschliche Darmkrebs‑ (WiDr) und Brustkrebs‑ (MCF‑7) Zelllinien im Kulturversuch reduzierte dieser Komplex die Zellüberlebensraten dramatisch auf unter 10 %. Folgeanalysen zeigten, dass die meisten betroffenen Zellen Apoptose durchliefen, eine Form des programmierten Zelltods, und nicht ein ungehemmtes Aufplatzen. Wichtig ist, dass weder das Protein allein, die Fettsäure allein noch Extrakte aus unveränderten Pflanzen eine signifikante Zellsterblichkeit auslösten, was bestätigt, dass die krebsvernichtende Wirkung vom spezifischen Komplex abhängt.
Was das für zukünftige Lebensmittel und Medikamente bedeuten könnte
In der Summe zeigt die Arbeit, dass Pflanzenchloroplasten zuverlässig große Mengen eines menschlichen Milchproteins produzieren können, das sowohl ernährungsrelevant als auch therapeutisch aktiv ist. Für Laien bedeutet das, dass zukünftige Säuglingsnahrungen, funktionelle Lebensmittel oder Nahrungsergänzungen eines Tages mit in Blättern gezüchteten Proteinen statt von Kühen gewonnen werden könnten, wodurch die Umweltbelastung sinkt und die Produkte näher an der menschlichen Biologie liegen. Gleichzeitig lässt sich dasselbe pflanzlich gewonnene Protein im Labor in einen zielgerichteten anti‑tumoralen Komplex umwandeln, was auf pflanzenbasierte Produktionsketten für erschwingliche Biotherapeutika hindeutet. Zwar sind weitere Untersuchungen nötig, um Sicherheit und Wirksamkeit in Tieren und Menschen zu bestätigen — und um die Technologie auf essbare Nutzpflanzen zu übertragen — doch die Studie bietet einen überzeugenden Ausblick darauf, wie Pflanzen als Mini‑Fabriken für die nächste Generation von Ernährung und Medizin dienen könnten.
Zitation: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Schlüsselwörter: in Pflanzen hergestellte Milchproteine, Chloroplasten-Biofabrik, menschliches Alpha-Laktalbumin, nachhaltige Milchalternativen, HAMLET-Krebstherapie