Clear Sky Science · de
Integrin αv trägt zur Regulierung der Steifigkeit vaskulärer glatter Muskelzellen bei
Warum die „Federkraft" der Arterien wichtig ist
Mit dem Alter oder bei Bluthochdruck verlieren unsere großen Arterien nach und nach ihre natürliche Elastizität und werden steifer. Diese Veränderung zwingt das Herz zu stärkerer Arbeit und erhöht das Risiko für Herzinfarkte, Schlaganfälle und andere Herz-Kreislauf-Erkrankungen. Wissenschaftler wissen seit Langem, dass die in den Gefäßwänden enthaltenen Materialien — Proteine wie Elastin und Kollagen — die Steifigkeit beeinflussen. Diese Studie stellt eine subtilere Frage: Können die Muskelzellen in den Gefäßwänden selbst steifer werden, und trägt eine kleine Familie von Oberflächenrezeptoren, genannt Integrin αv, dazu bei, diese Zellen und damit unsere Arterien flexibler zu halten?
Die Muskelzellen, die den Blutfluss formen
Große Arterien sind nicht nur passive Rohre. Ihre mittlere Schicht ist dicht mit vaskulären glatten Muskelzellen gefüllt, die sich zusammenziehen und entspannen können, um Blutfluss und Druck fein zu regulieren. Diese Zellen sind an ein umgebendes Gerüst, die extrazelluläre Matrix, verankert. Die Forscher konzentrierten sich auf eine Gruppe von Verankerungsmolekülen, Integrin αv, die die Zelloberfläche durchspannt und das innere Gerüst der Zelle physikalisch mit diesem äußeren Gerüst verbindet. Frühere Arbeiten deuteten darauf hin, dass Integrin αv an Vernarbung und Umbau von Blutgefäßen beteiligt ist, doch es war unklar, ob es auch steuert, wie steif die Muskelzellen selbst werden — besonders unter dem Stress von Hormonen wie Angiotensin II, die den Blutdruck erhöhen und Fibrose fördern.
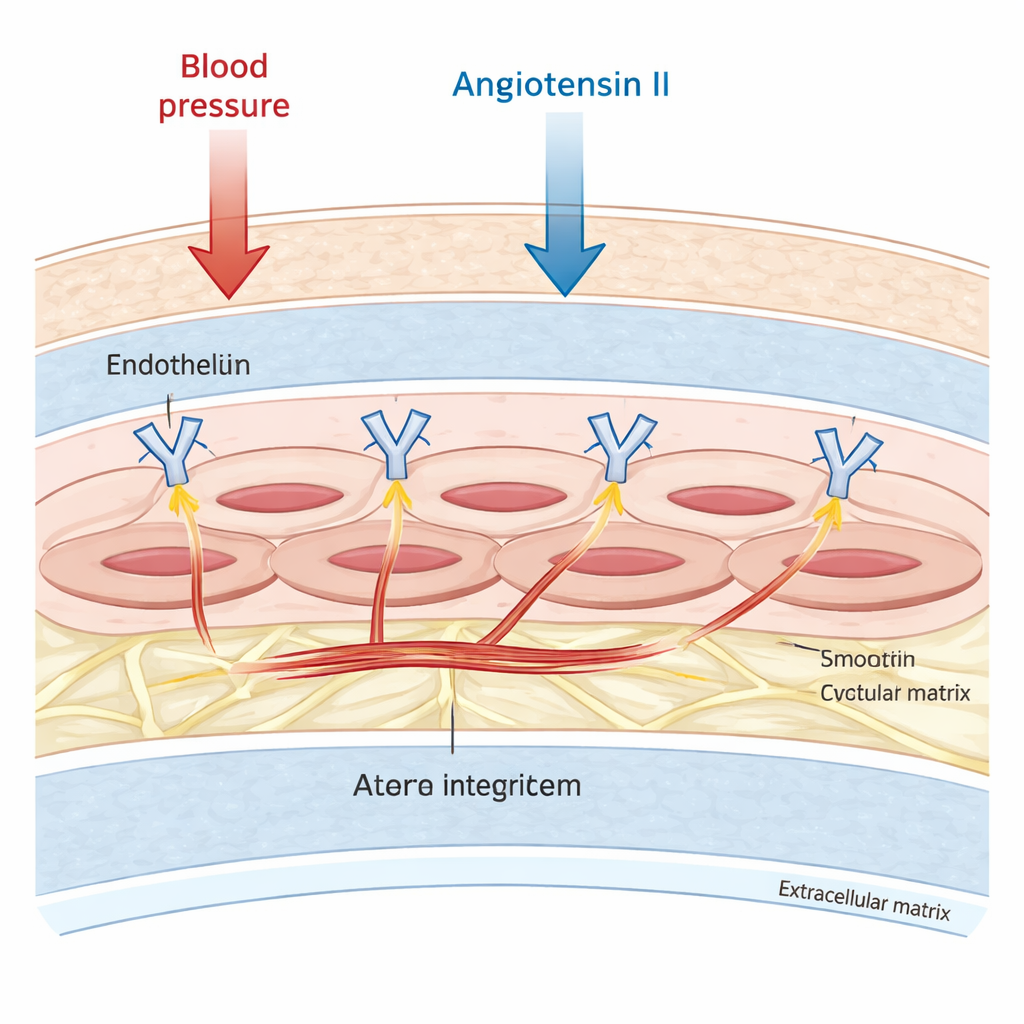
Steifigkeit Zelle für Zelle messen
Um dies zu untersuchen, verwendete das Team in vitro gezüchtete Maus-glatte Muskelzellen und Mäuse, denen Integrin αv spezifisch in ihren vaskulären Muskelzellen fehlte. Sie prüften die Zellsteifigkeit mit der Rasterkraftmikroskopie, einer Technik, bei der eine ultrafeine Spitze die Zelloberfläche sanft eindellt und aufzeichnet, welche Kraft nötig ist. Zellen ohne Integrin αv waren unter ruhigen Bedingungen mehr als doppelt so steif wie Kontrollzellen. Nach zweitägiger Behandlung mit Angiotensin II wurden diese defizitären Zellen nochmals etwa dreimal so steif, während sich normale Zellen kaum veränderten. Da ihre Messungen sehr flache Eindellungen nutzten, bauten die Autoren ein detailliertes Computermodell einer glatten Muskelzelle und simulierten tiefere Eindrücke. Die Simulationen zeigten, dass flache Tests den Beitrag der äußeren Schale und der kortikalen Region der Zelle betonen und weiterhin im Bereich der Werte der steifen Mutanten lagen, was die biologischen Befunde stützte.
Ein umgestaltetes inneres Gerüst
Der nächste Schritt war der Blick ins Zellinnere. Mit fluoreszierenden Farbstoffen und Mikroskopie untersuchten die Forscher Aktin, ein zentrales Filament, das das interne Gerüst der Zelle bildet. Kontrollmuskelzellen zeigten ein relativ diffus verteiltes Aktinnetz, selbst nach Angiotensin-II-Behandlung. Dagegen bildeten Zellen ohne Integrin αv dicke Stressfasern, die die Zelle durchkreuzten, und nach Hormonexposition einen intensiven Aktinring direkt unter der Zellmembran, bekannt als kortikales Aktin. Ein quantitatives Maß dafür, wie viel Aktin sich am Zellrand ansammelte, bestätigte, dass diese kortikale Schicht nur in den integrin-defizienten Zellen stark angereichert war. Diese Zellen entwickelten außerdem ungewöhnlich lange Adhäsionsstrukturen, mit denen sie an der umgebenden Matrix Halt finden — konsistent mit einem Übergang zu stärker spannungstragenden, fibrillären Adhäsionen, die die Zelle in einem starren Zustand verhaken können.
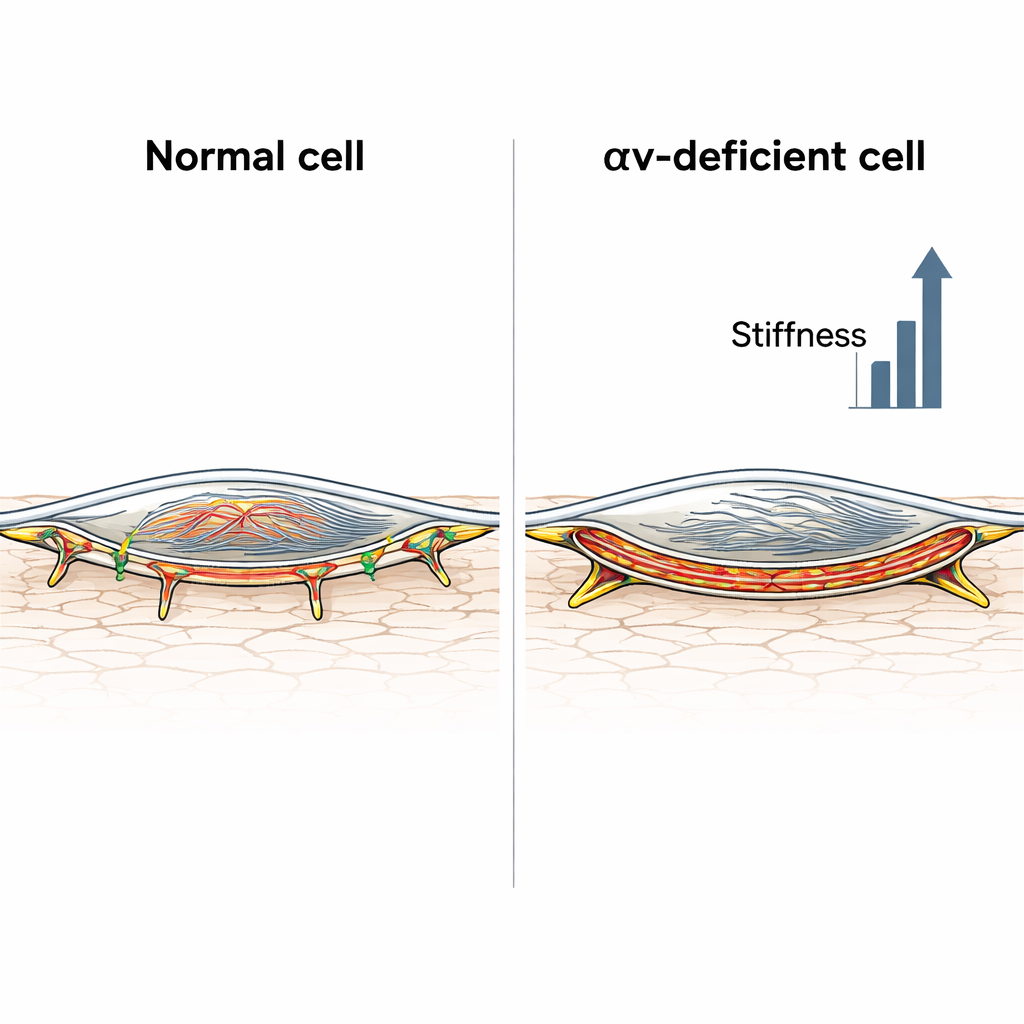
Wenn die Wand gleich aussieht, sich aber anders verhält
Da Arterien mehr sind als nur ihre Muskelzellen, maßen die Wissenschaftler auch die mechanischen Eigenschaften der Karotisarterien bei lebenden Mäusen mit und ohne Integrin αv in ihren vaskulären Muskelzellen sowie mit oder ohne chronische Angiotensin-II-Infusion. Überraschenderweise waren der gesamte arterielle Druck und die Wandsteifigkeit — bestimmt aus ultraschallbasierten Druck-Durchmesser-Kurven — bei beiden Mauslinien ähnlich, sowohl im Ausgangszustand als auch nach der Hormonbehandlung. Dennoch unterschied sich die mikroskopische Zusammensetzung der Wand. Unter Angiotensin II zeigten Kontrollmäuse weniger Elastin und mehr Kollagen, klassische Anzeichen einer steiferen Matrix, während integrin-defiziente Mäuse vergleichsweise weniger Kollagenveränderung, aber deutlich steifere Muskelzellen aufwiesen. Anders gesagt: Bei normalen Mäusen übernahm die Matrix den größten Teil der Versteifung; bei integrin-defizienten Mäusen wurden die Muskelzellen selbst so starr, dass sie die moderateren Matrixveränderungen effektiv ausglichen.
Was das für alternde Arterien bedeutet
Für Laien ist die Kernbotschaft: Arterielle Steifigkeit hängt nicht nur von verschlissenen elastischen Fasern ab; sie hängt auch davon ab, wie die Muskelzellen in der Wand ihre kleinen inneren „Kabel" organisieren. Integrin αv hilft normalerweise, diese Zellen davor zu bewahren, bei Belastung durch Hormone wie Angiotensin II zu starr zu werden. Geht diese Kontrolle verloren, ordnen die Zellen ihr Aktin-Zytoskelett neu — besonders im Kortex direkt unter der Membran — und verhaken sich in einem steiferen Zustand, der zur Versteifung der Arterie beitragen kann, selbst ohne dramatische Veränderungen des umgebenden Materials. Diese Einsicht weist auf neue therapeutische Ideen hin: Medikamente, die das kortikale Aktinnetz sanft lockern oder umorganisieren, oder die integrin-gekoppelte Signalwege modulieren, könnten eines Tages blutdrucksenzende Therapien ergänzen, um die „Federkraft" alternder Arterien direkter wiederherzustellen.
Zitation: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Schlüsselwörter: arterielle Steifigkeit, vaskuläre glatte Muskelzellen, Integrin alpha v, Aktin-Zytoskelett, Angiotensin II