Clear Sky Science · de
Autofluoreszenz- und Fourier-Transformations-Infrarot-Analysen verfolgen diätetische Fluorophore und enthüllen Plastikkontamination im Darm von Mückenlarven
Warum diese Mückenstudie wichtig ist
Mücken sind berüchtigt für die Übertragung von Krankheiten, doch bevor sie überhaupt zustechen, verbringen sie Tage als winzige Larven, die in mit Wasser gefüllten Behältern fressen. Diese frühen Entwicklungsstadien sind die Arbeitspferde des Mückenwachstums und ein wichtiges Ziel für Bekämpfungsstrategien. Die Studie zeigt, wie Forschende ohne Zusatz von Farbstoffen sehen können, was Larven fressen — und sogar Spuren von Plastik erkennen, das unbemerkt aus gängigen Laborgefäßen in ihre Därme übergeht. Die Ergebnisse sind wichtig sowohl für die Entwicklung sichererer Mückenbekämpfungsmaßnahmen als auch fürs Verständnis, wie Mikroplastikverschmutzung durch kleine Wassertiere transportiert werden kann.
Leuchtende Hinweise im Inneren winziger Körper
Viele natürliche Moleküle leuchten schwach, wenn sie mit bestimmten Lichtfarben beleuchtet werden – eine Eigenschaft, die als Autofluoreszenz bezeichnet wird. Die Forschenden nutzten dieses eingebaute Leuchten, um Nahrung in Larven der Asiatischen Tigermücke, eines wichtigen Krankheitsüberträgers, nachzuverfolgen. Mit leistungsfähigen Mikroskopen und spektraler Bildgebung untersuchten sie kommerzielles Larvenfutter, den Larvendarm und dünne Gewebeschnitte. Die Nahrungsbestandteile zeigten zwei Hauptleuchtsignale: ein breites bläuliches Band von proteinreichen Materialien und ein scharfes rotes Band von chlorophyllähnlichen Pigmenten pflanzlichen bzw. algalen Ursprungs. Wenn Larven dieses Futter aufnahmen, zeigten auch die Darminhalte dieselben Signaturen, was bestätigt, dass diese Lichtsignale als natürliche Marker für die aufgenommene Nahrung dienen können.
Nahrungspigmente entkommen dem Darm
Durch Vergrößerung mit konfokaler Mikroskopie entdeckte das Team etwas Überraschendes: Das rote, chlorophyllähnliche Signal war nicht auf das Darmlumen beschränkt. Es erschien auch in der umgebenden Körperhöhle, nicht jedoch in der äußeren Cuticula. Dieses Muster deutet darauf hin, dass einige aus der Nahrung stammende Pigmente die Verdauung überleben und in interne Körperflüssigkeiten übergehen können, wo sie sich möglicherweise in anderen Geweben anreichern. Dieselbe rote Emission wurde auch im Wasser nachgewiesen, in dem Larven gehalten worden waren, obwohl sie in Wasser mit nur Futter nicht vorhanden war. Das legt nahe, dass Larven chlorophyllähnliche Verbindungen aufnehmen und später teilweise wieder in ihre Umgebung abgeben — ein Weg, um zu verfolgen, wie natürlich fluoreszierende Nahrungsbestandteile durch das Tier und seinen Lebensraum zirkulieren.
Material des Behälters verändert, was Larven aufnehmen
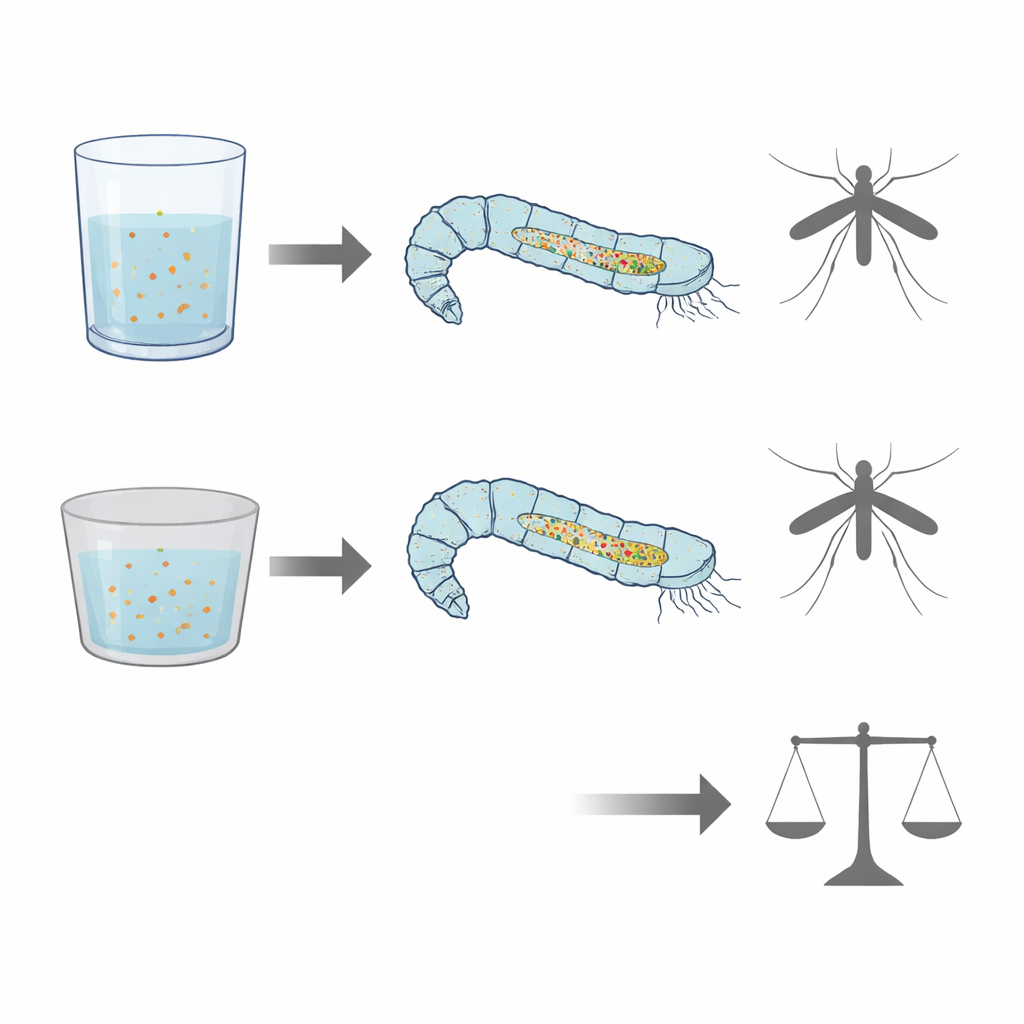
Um zu prüfen, wie die Aufzuchtumgebung das Fressverhalten beeinflussen könnte, wurden Larven entweder in Glasschalen oder in Polystyrol-Kunststoffschalen unter ansonsten identischen Bedingungen gehalten. Das Gesamtleuchten des Darms war bei Larven aus Kunststoffbehältern durchgehend stärker und ausgeprägter als bei denen aus Glas, was auf Unterschiede in Futteraufnahme oder -verarbeitung hindeutet. Spektrofluorimetrische Messungen des umgebenden Wassers zeigten Veränderungen in einer anderen Gruppe von fluoreszierenden Verbindungen, den Flavinen, die mit Energiestoffwechsel und B-Vitaminen verknüpft sind. Diese Verschiebungen deuten darauf hin, dass Larven, die in unterschiedlichen Behältermaterialien aufgezogen wurden, bestimmte Nährstoffe anders handhaben können, selbst wenn das Futter identisch ist.
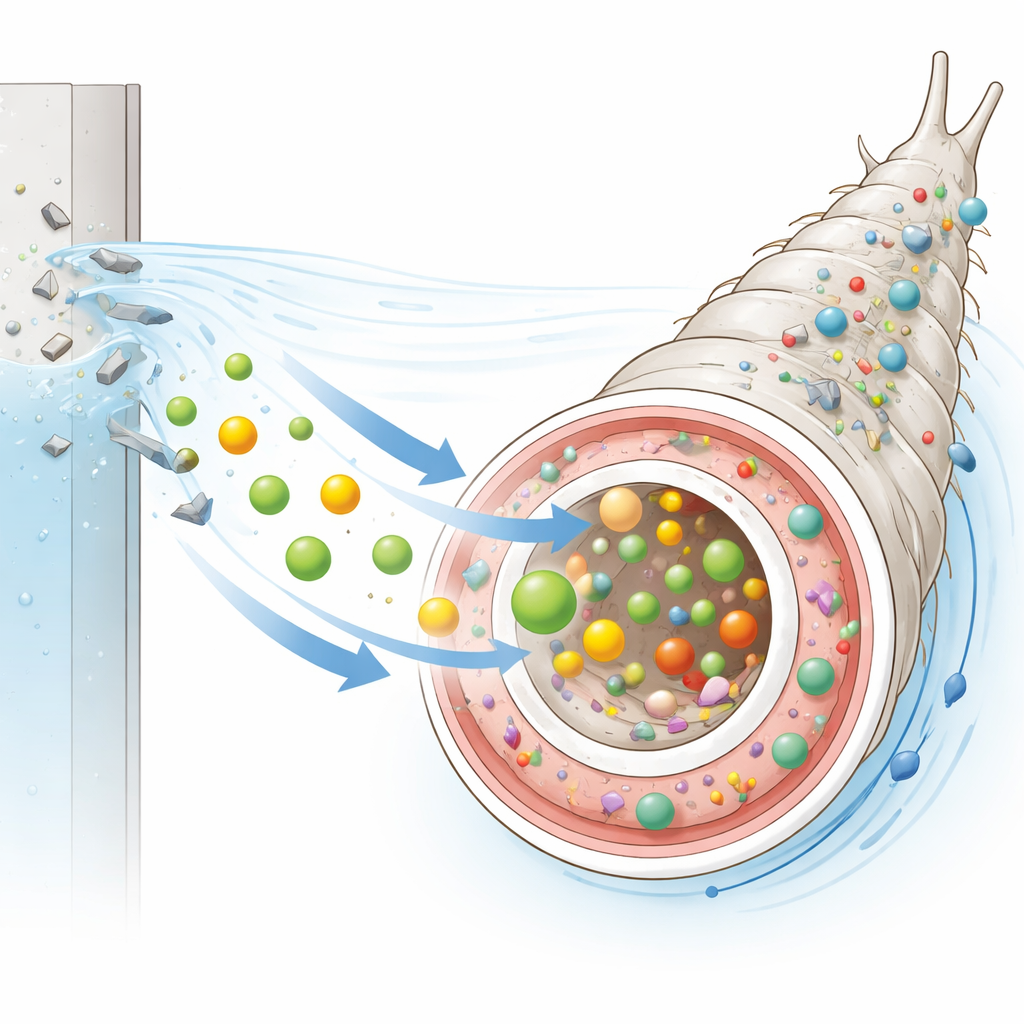
Verborgene Plastik-Fingerabdrücke im Darm
Über lichtbasierte Bildgebung hinaus nutzten die Wissenschaftler ATR-FTIR-Spektroskopie, um die chemischen „Fingerabdrücke“ von Larvendarminhalten und Aufzuchtmaterialien zu lesen. Därme von Larven, die in Kunststoffschalen aufgezogen wurden, zeigten ein charakteristisches Signal im Infrarotbereich, das eng mit einem Schlüsselmerkmal von Polystyrol übereinstimmte — ebenso wie Därme von Larven, die experimentell Polystyrolkügelchen ausgesetzt waren. Dieser Peak fehlte in Därmen von Larven aus Glas und im Futter selbst, was stark dafür spricht, dass materialabgeleitete Kunststoffpartikel in Larven aus Kunststoffbehältern vorhanden sind. Zwar zeigte die Elektronenmikroskopie keine offensichtlichen Kratz- oder Abnutzungsspuren an den Innenflächen der Schalen, frühere Arbeiten haben jedoch gezeigt, dass Kunststoff bei normaler Nutzung mikroskopische und sogar nanoskale Fragmente abgeben kann, die von Wasserorganismen aufgenommen werden.
Was das für Mückenbekämpfung und Verschmutzung bedeutet
Trotz dieser subtilen chemischen und optischen Unterschiede änderten sich Standardgrößen wie Larven-Überleben, Entwicklungsdauer und Körpergröße der erwachsenen Tiere kaum zwischen Glas- und Kunststoffgruppen, abgesehen von einer moderaten Verschiebung in der Larvenentwicklungszeit. Für einen oberflächlichen Betrachter würden die Mücken fast identisch erscheinen. Ihre Därme erzählen jedoch eine komplexere Geschichte: Sie unterscheiden sich darin, wie viel nahrungsbedingtes Leuchten sie tragen, wie sie bestimmte Vitamine und Pflanzenpigmente verarbeiten und ob Plastikfragmente in ihr Gewebe gelangt sind. Für Vektorkontrollprogramme, die auf Massenzucht von Mücken angewiesen sind — insbesondere beim Einsatz der Sterilen-Insekten-Technik — könnten solche verborgenen Effekte die langfristige Leistungsfähigkeit und Gesundheit beeinflussen. Allgemeiner zeigt die Arbeit, dass natürliche Fluoreszenz und Infrarotspektroskopie empfindliche, nicht-destruktive Werkzeuge sein können, um Ernährung, Aufzuchtbedingungen und Plastikkontamination bei kleinen Wassertieren zu überwachen. Diese Methoden könnten helfen, umweltverträglichere Larvenbekämpfungsstrategien zu verfeinern und unser Verständnis dafür zu vertiefen, wie Mikroplastik still und leise durch Süßwasserökosysteme wandert.
Zitation: Soldano, S., Weththimuni, M.L., Oldani, A. et al. Autofluorescence and Fourier transform infrared analyses trace dietary fluorophores and reveal plastic contamination in the gut of mosquito larvae. Sci Rep 16, 7841 (2026). https://doi.org/10.1038/s41598-026-38938-1
Schlüsselwörter: Mückenlarven, Autofluoreszenz, Mikroplastik, Chlorophyllpigmente, Vektorkontrolle