Clear Sky Science · de
Gefaltete Ti₃C₂Tₓ-MXene-Elektroden mit einstellbarer Oberflächenchemie für leistungsstarke und selektive elektrochemische Biosensorik
Intelligentere Sensoren für die Alltagschemie
Von der Gehirngesundheit bis zur Schmerzbehandlung zirkulieren viele wichtige Moleküle in unserem Körper — etwa Vitamin C, Dopamin, Harnsäure und Paracetamol — in sehr geringen Konzentrationen im Blut, Schweiß und anderen Flüssigkeiten. Ärzte und Lebensmittelwissenschaftler brauchen schnelle, verlässliche Methoden, um diese Stoffe zu messen, selbst wenn sie zusammen mit zahllosen anderen Verbindungen vorliegen. Diese Studie zeigt, wie ein neues, wellenartig gefaltetes, blattförmiges Material namens MXene geformt und chemisch abgestimmt werden kann, um kleine, hochempfindliche Elektroden zu bauen, die diese Moleküle schnell und präzise erkennen und damit den Weg für bessere Diagnosegeräte sowie Qualitätskontrollen in Lebensmitteln und Umwelt ebnen.
Warum diese winzigen Moleküle wichtig sind
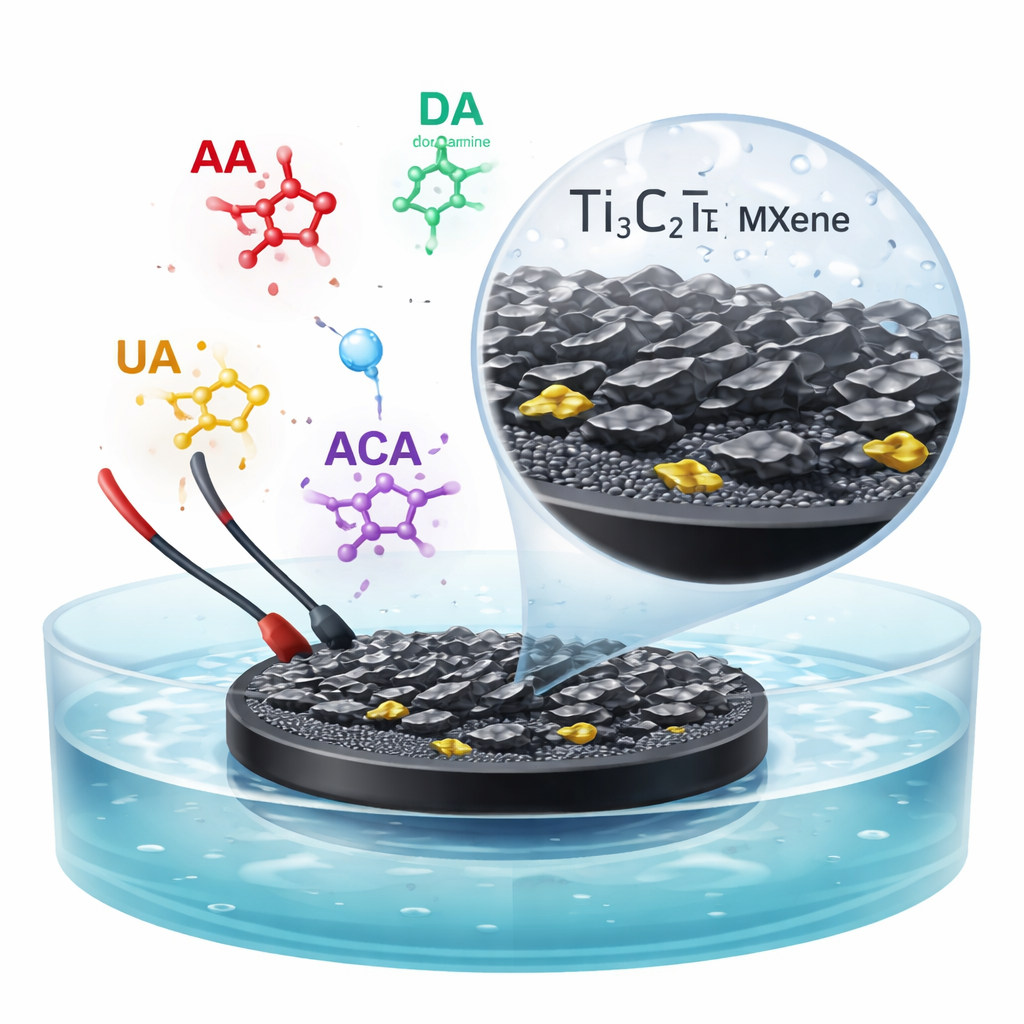
Die Forschenden konzentrierten sich auf vier bekannte Verbindungen: Ascorbinsäure (Vitamin C), Dopamin, Harnsäure und Paracetamol. Abnorme Konzentrationen dieser Substanzen stehen in Zusammenhang mit neurologischen Störungen, oxidativem Stress, Gicht und Leberbelastung durch frei verkäufliche Schmerzmittel. Standardlabortests zur Bestimmung dieser Stoffe können langsam, kostspielig sein oder aufwändige Probenvorbereitung erfordern. Elektrochemische Sensoren — kleine Elektroden, die chemische Reaktionen in elektrische Signale umwandeln — bieten eine schnellere, günstigere Alternative. Die Herausforderung besteht darin, eine Elektrodenoberfläche zu entwerfen, die empfindlich genug ist, um niedrige Konzentrationen zu detektieren, selektiv genug, um ähnliche Moleküle zu unterscheiden, und robust genug, um in echten biologischen und Lebensmittelproben mit zahlreichen Störstoffen zu funktionieren.
Gefaltete Metallschichten als neue Sensorkomponente
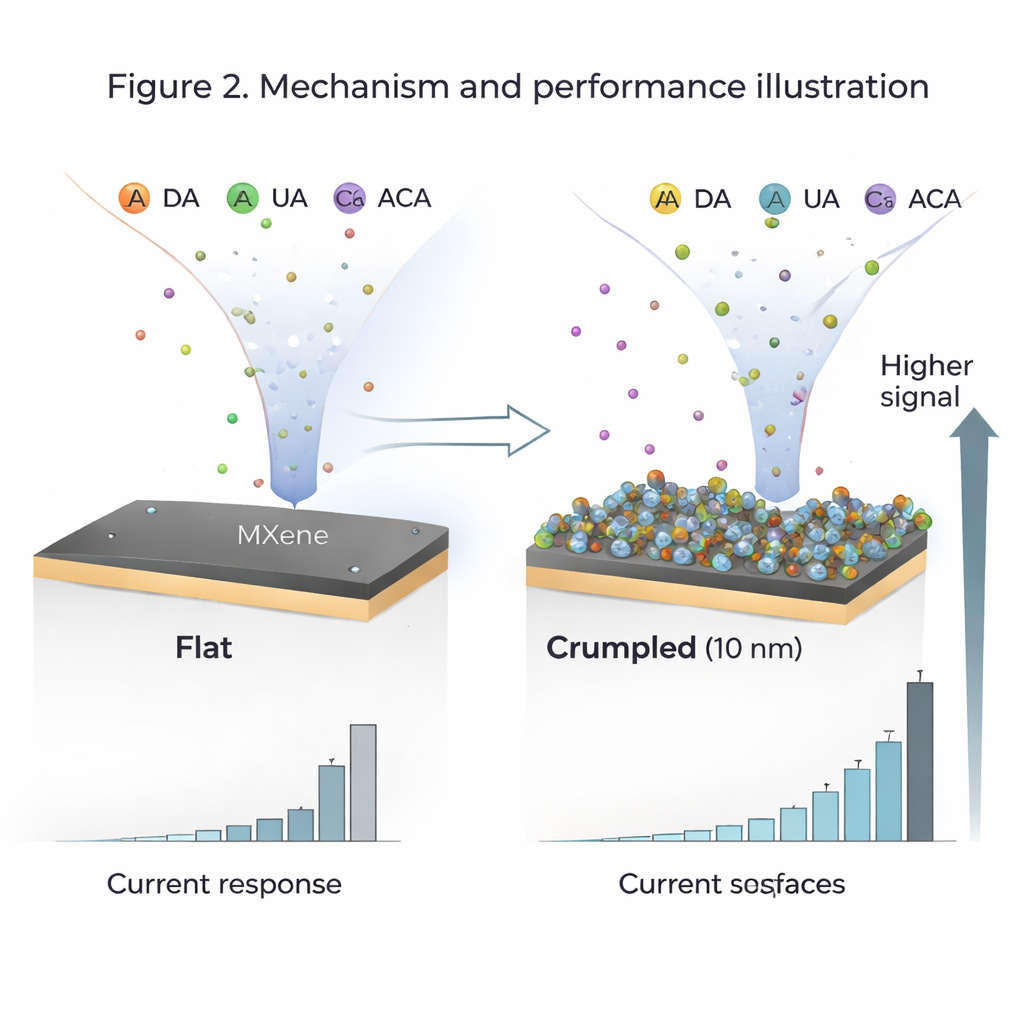
Um das Problem anzugehen, verwendete das Team ein zweidimensionales Material namens Ti3C2Tx MXene — ein Stapel atomar dünner, elektrisch leitfähiger Schichten, die mit chemischen Gruppen wie Sauerstoff und Hydroxyl (–O und –OH) versehen sind. Sie beschichteten eine Standard-Glassy-Carbon-Elektrode mit MXene und knitterten die MXene-Schicht gezielt zu winzigen Falten, nur wenige Milliardstel Meter hoch. Durch Kontrolle des Faltungsgrades (der „Amplitude“ der Falten) und der Schichtdicke konnten sie die freiliegende Oberfläche und die Zugänglichkeit für Moleküle einstellen. Sie fanden, dass eine sanft gefaltete Oberfläche mit Falten von etwa 10 Nanometern Höhe und einer dünnen 10-Nanometer-Schicht die beste Leistung erzielte.
Wie der Sensor in der Praxis funktioniert
In Tests erzeugte die gefaltete MXene-Elektrode starke, klare elektrische Signale, wenn jedes Zielmolekül in realistischen Konzentrationen zwischen 10 und 200 Mikromol vorlag. Die Empfindlichkeit — wie stark sich der Strom bei einer Konzentrationsänderung ändert — lag zwischen etwa 0,77 und 0,82 Mikroampere pro Mikromol, mit Nachweisgrenzen unter 1 Mikromol für alle vier Analyten. Die gewellte Oberfläche bietet eine große Oberfläche (etwa 150 Quadratmeter pro Gramm MXene) und viele –O/–OH-Gruppen, die die Moleküle über Wasserstoffbrücken und Stapelwechselwirkungen aromatischer Ringe anziehen. Selbst wenn alle vier Moleküle gemeinsam vorhanden waren, fielen die Signale nur um etwa 5–8 Prozent, da sie um dieselben Bindungsstellen konkurrierten — das heißt, der Sensor kann jedes einzelne in einem Gemisch weiterhin unterscheiden.
Bestätigung des Mechanismus mit Computermodellen
Um die Vorgänge jenseits des Labortisches zu verstehen, erstellten die Autorinnen und Autoren detaillierte Computermodelle mit COMSOL Multiphysics. Sie simulierten, wie die Moleküle in Lösung diffundieren, sich auf der gefalteten Oberfläche adsorbieren und Elektronen mit der Elektrode austauschen. Das Modell sagte Diffusionskoeffizienten, Ansprechzeiten von etwa 1,5–2,5 Sekunden und Stromstärken voraus, die gut mit den Experimenten übereinstimmten. Durch den Vergleich verschiedener Faltenmaße und Schichtdicken in den Simulationen zeigten sie, warum moderate Faltung und dünne Schichten den besten Kompromiss liefern: mehr aktive Bindungsstellen, kürzere Transportwege für Moleküle und weniger Überfüllung in tiefen Falten. Die Modellierung bestätigte außerdem, dass die MXene-Oberfläche die Zielmoleküle deutlich stärker bindet als häufige Störstoffe wie Glukose und Zitronensäure, was erklärt, warum die Anwesenheit dieser Hintergrundstoffe den Strom um weniger als etwa 2,5 Prozent veränderte.
Was das für Tests in der realen Welt bedeutet
Praktisch gesehen zeigt diese Arbeit, dass das gezielte Knittern und die chemische Abstimmung von MXene-Filmen einfache Kohlenstoffelektroden in leistungsfähige, selektive Detektoren für biologisch relevante Moleküle verwandeln. Da diese Sensoren schnell sind, bei niedrigen Konzentrationen empfindlich reagieren und gegenüber üblichen Störstoffen robust sind, könnten sie in tragbare Geräte zur Überwachung von Gesundheitsmarkern, zur Prüfung des Nährstoff- oder Verderbszustands von Lebensmitteln oder zur Verfolgung von Schadstoffen integriert werden. Die Kernbotschaft lautet, dass die nanoskalige Formgebung eines Materials zusammen mit den chemischen Gruppen auf seiner Oberfläche gemeinsam so gestaltet werden kann, dass die Leistung verbessert wird — und damit eine Roadmap für die nächste Generation kleiner, intelligenter elektrochemischer Biosensoren bietet.
Zitation: Aburub, F., Abdullah, Q., Mohammad, S.I. et al. Crumpled Ti₃C₂Tₓ MXene electrodes with tunable surface chemistry for high-performance and selective electrochemical biosensing. Sci Rep 16, 7663 (2026). https://doi.org/10.1038/s41598-026-38937-2
Schlüsselwörter: elektrochemischer Biosensor, MXene, Dopaminbestimmung, nanostrukturierte Elektroden, Oberflächenchemie