Clear Sky Science · de
A2-Pancortine interagieren mit Bcl-xL und WAVE1, um Mitochondrien-ER-Kontaktstellen (MERCs) zu fördern und die mitochondriale Kalziumerhöhung zu verstärken, wodurch der Zelltod bei Schlaganfall vermittelt wird
Warum winzige Hirnverbindungen bei Neugeborenen-Schtanfall wichtig sind
Schlaganfall wird oft als Krankheit Erwachsener wahrgenommen, doch wenn er Neugeborene trifft, kann er still die Entwicklung des Gehirns schädigen und lebenslange Probleme nach sich ziehen. Diese Studie untersucht, was während einer solchen Krise tief in Nervenzellen geschieht. Die Autorinnen und Autoren konzentrieren sich auf eine wenig bekannte Familie von Proteinen, die Pancortine genannt werden, und zeigen, wie zwei entwicklungsbedingte Varianten wie gefährliche „Verstärker“ wirken, indem sie die Verbindungen zwischen wichtigen Zellstrukturen verstärken und eine Kalziumflut auslösen, die junge Neurone in Richtung Zelltod drängen kann.
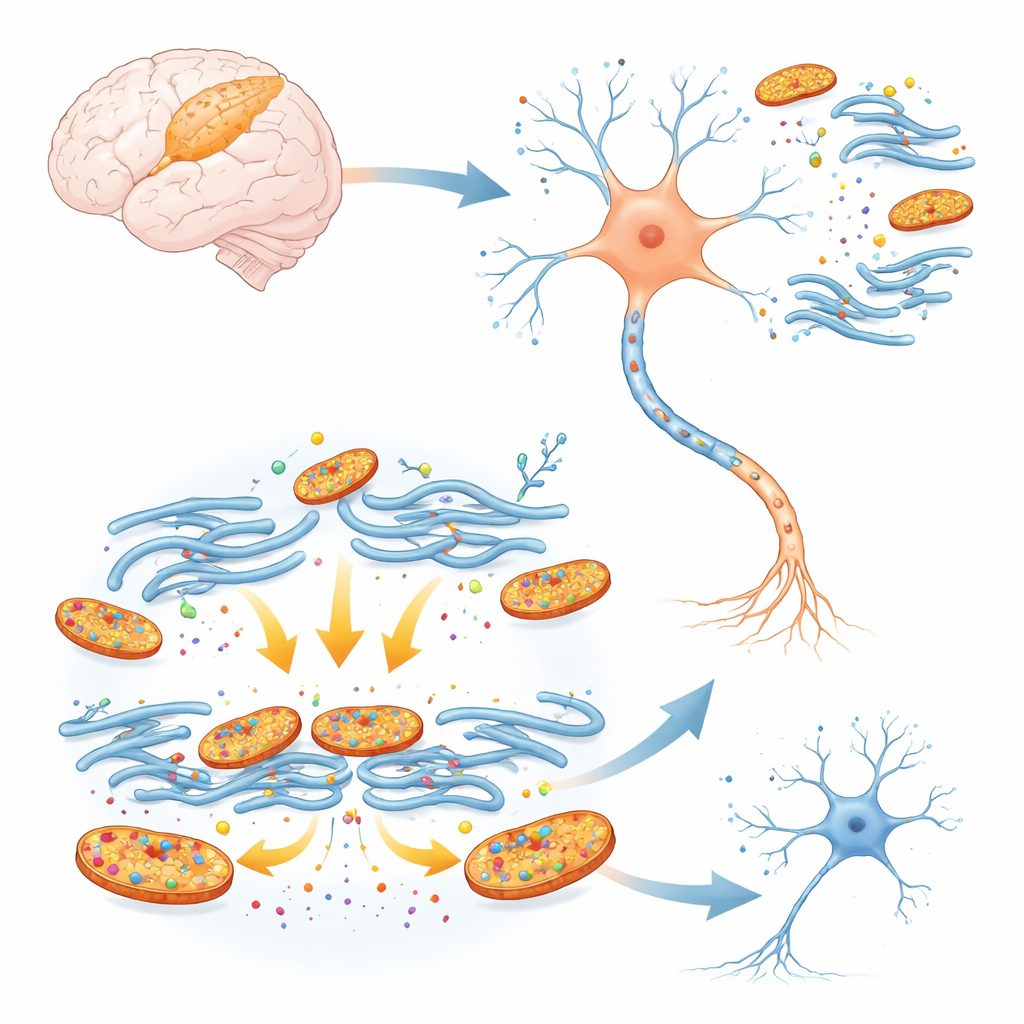
Verborgene Schuldige im neugeborenen Gehirn
Pancortine sind gerüstähnliche Proteine, die beim Formen des wachsenden Gehirns helfen. Zwei Formen, als A2-Pancortine bezeichnet, sind in der frühen Entwicklung reichlich vorhanden und gehen dann weitgehend zurück, wenn das Gehirn reift. Da Neugeborenenhirne besonders verletzlich gegenüber Sauerstoffmangel sind, fragten die Forschenden, ob diese frühzeitigen Proteine den Schaden verschlimmern könnten, wenn die Durchblutung der Hirnrinde kurz unterbrochen wird, wie bei neonatalem Schlaganfall. In kultivierten kortikalen Mausneuronen setzten sie genetische Werkzeuge ein, um alle Pancortin-Spiegel zu senken, und setzten die Zellen einem Sauerstoff‑ und Glukosemangel aus, der Schlaganfall nachahmt. Neurone mit reduziertem Pancortin überlebten deutlich häufiger, was darauf hindeutet, dass diese Proteine junge Zellen unter Stress eher in Richtung Schädigung treiben, statt sie zu schützen.
Von Maus‑Schlaganfallmodellen zu gerettetem Hirngewebe
Um zu prüfen, ob diese schädliche Rolle auch im lebenden Gehirn auftritt, erzeugte das Team Mäuse, denen speziell die entwicklungsbedingten A2-Pancortin‑Formen fehlen. Junge, zwei Wochen alte Knockout‑Mäuse und ihre normalen Wurfgeschwister wurden dann einer Blockade einer großen Hirnarterie ausgesetzt, einem Standardmodell des ischämischen Schlaganfalls. Nach einem Tag zeigten beide Gruppen Verletzungen in tiefen Hirnregionen, doch die Hirnrinde von Mäusen ohne A2‑Pancortine wies nur etwa halb so viel Schaden auf wie die normaler Tiere. Auffällig war, dass dieser schützende Effekt bei fünf Wochen alten Mäusen verschwand, wenn erwachsene Pancortin‑Varianten vorherrschen. Diese altersabhängigen Ergebnisse deuten auf A2‑Pancortine als wichtige pro‑Tod‑Faktoren in der neonatalen Hirnrinde hin und verbinden ein Entwicklungsprogramm mit Schlaganfallanfälligkeit.
Gefährliche Kontaktzonen innerhalb von Neuronen
Innerhalb der Zellen liegen die energieproduzierenden Mitochondrien nahe am endoplasmatischen Retikulum (ER), einem gefalteten Membrannetzwerk, das Kalzium speichert. Dort, wo die beiden Membranen in Nähe zueinander treten, fungieren sogenannte Mitochondrien‑ER‑Kontaktstellen als mikroskopische Tunnel, durch die Kalzium fließen kann. Mäßiger Transfer unterstützt die Energieproduktion, doch zu viel kann Mitochondrien überlasten und Zelltod auslösen. Die Forschenden fanden, dass A2‑Pancortine zusammen mit zwei Partnern — Bcl‑xL und WAVE1 — einen dreiteiligen Komplex bilden, der an diesen Kontaktstellen sitzt. Wenn sie die Zellen zur Überproduktion von A2‑Pancortinen und diesen Partnern zwangen, berührten sich Mitochondrien und ER häufiger und enger, wie ein spezialisierter Split‑Fluoreszenzsensor berichtete. Ein Verankerungsprotein namens GRP75 schloss sich diesem Komplex an und half, die Kontaktzonen zu stabilisieren.
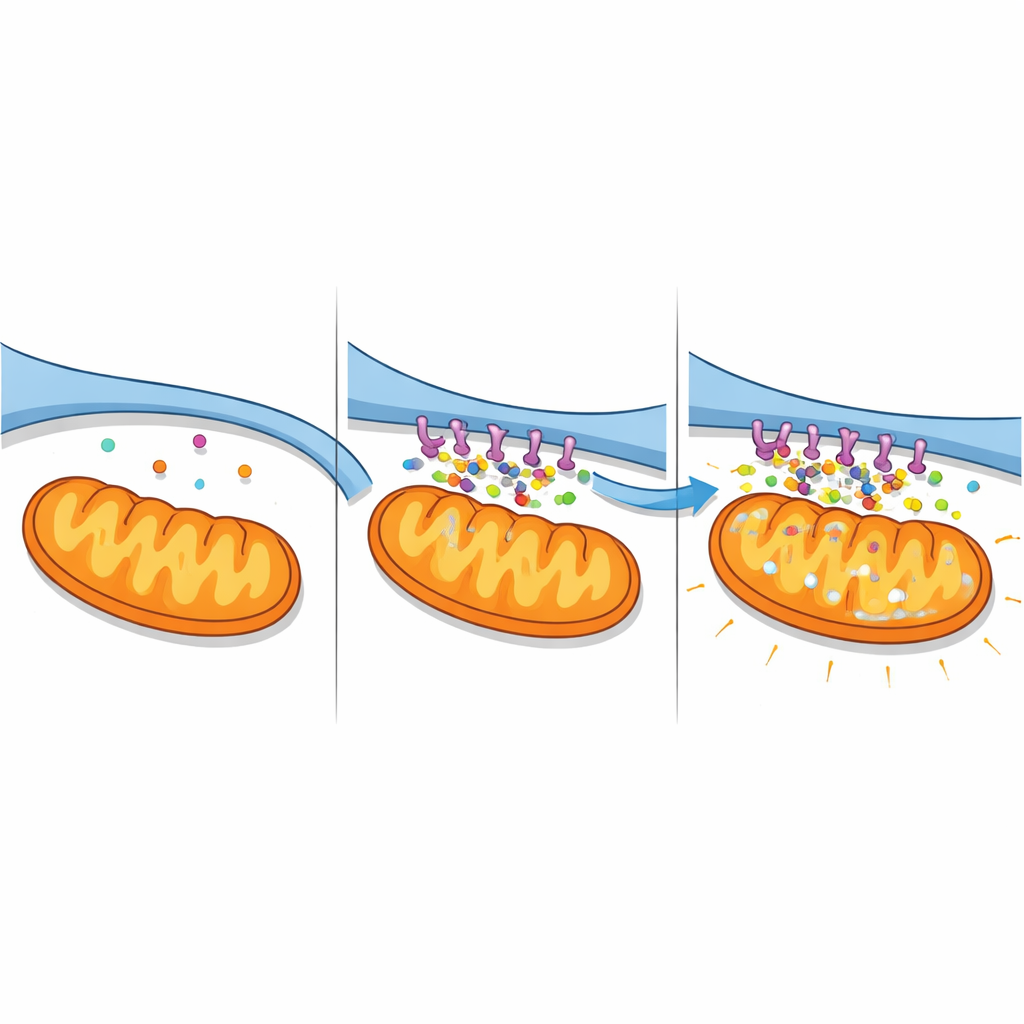
Kalziumfluten und versagende Kraftwerke
Die verstärkten Kontakte hatten gravierende Folgen für das Kalziumgleichgewicht. Mithilfe fluoreszenter Indikatoren, die getrennt Kalzium im Zytosol, ER und in Mitochondrien melden, verfolgten die Autorinnen und Autoren zeitliche Änderungen. Zellen, die den A2‑Pancortin‑Komplex exprimierten, zeigten einen stetigen Anstieg des Kalziums in den Mitochondrien und im umliegenden Zellplasma sowie einen Abfall der ER‑Speicher, ein Kennzeichen massiven Transfers vom ER in die Mitochondrien. Die Blockade eines wichtigen Kalziumfreisetzungskanals an der ER‑Oberfläche (IP3R) verhinderte diese Veränderungen weitgehend und bestätigte, dass der Komplex eine spezifische ER‑zu‑Mitochondrien‑Route verstärkt. In nervenähnlichen Zellen, die einem schlaganfallähnlichen Sauerstoff‑ und Glukoseentzug ausgesetzt wurden, hatte das Herunterregulieren von Pancortinen die entgegengesetzte Wirkung: die Kalziumüberladung wurde abgeschwächt und die ER‑Speicher blieben besser erhalten. Zusammengenommen zeigen diese Befunde A2‑Pancortine als Organisatoren einer Kalzium‑„Autobahn“, die unter ischämischem Stress tödlich wird.
Was das für den Schutz neugeborener Gehirne bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Diese Arbeit identifiziert einen neuen molekularen Schalter, der mitentscheidet, ob junge Neurone nach einem Schlaganfall überleben oder sterben. Indem sie die mikroskopischen Verbindungen zwischen kalziumspeichernden Membranen und zellulären Kraftwerken verstärken, bringen A2‑Pancortine Mitochondrien dazu, an überschüssigem Kalzium zu ersticken und zu versagen. Das Entfernen dieser Proteine bei jungen Mäusen mildert die Folgen des experimentellen Schlaganfalls und legt nahe, dass Medikamente oder gentherapeutische Ansätze, die darauf abzielen, A2‑Pancortin‑Komplexe zu stören — oder die Kontaktstellen, die sie verstärken, zu lockern — eines Tages Hirnschäden bei betroffenen Neugeborenen reduzieren könnten. Obwohl solche Therapien vorerst Zukunftsmusik sind, zeichnet die Studie einen klaren und prüfbaren Weg von Entwicklungsproteinen über Kalziumüberladung bis zum neuronalen Verlust beim neonatalen Schlaganfall nach.
Zitation: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Schlüsselwörter: neonataler Schlaganfall, Mitochondrien-ER-Kontaktstellen, Kalziumüberladung, Pancortin-Proteine, neuronaler Zelltod