Clear Sky Science · de
Eine neuartige C/EBPα–miR-335-5p–PRKAA2-Regulationsachse treibt die hepatische Lipidakkumulation bei MASLD voran
Warum die Fettlebererkrankung wichtig ist
Viele Menschen, die kaum Alkohol trinken, entwickeln trotzdem eine „Fettleber“, eine Erkrankung, die heute als metabolisch bedingte Steatose der Leber (MASLD) bezeichnet wird. Sie steht in engem Zusammenhang mit Adipositas und Typ‑2‑Diabetes und kann stillschweigend zu Lebervernarbung, Zirrhose und sogar Leberkrebs fortschreiten. Diese Studie stellt eine einfache, aber entscheidende Frage: Was geschieht in den Leberzellen, sodass sie so viel Fett speichern, und lässt sich ein molekularer Schalter finden, der abgeschaltet werden könnte, um die Leber zu schützen?
Eine verborgene Kaskade in Leberzellen
Die Forschenden konzentrierten sich auf eine molekulare Kaskade, die Ernährung und Stoffwechsel mit Fettansammlung in der Leber verbindet. Sie untersuchten Mäuse, die mit fettreicher Kost gefüttert wurden, sowie kultivierte Leberzellen, die in Fettsäuren gebadet wurden, um MASLD nachzubilden. In diesen Modellen nahmen die Tiere zu, ihre Blutfettwerte stiegen und ihre Lebern füllten sich mit öliger Tropfen, womit wesentliche Merkmale der menschlichen Fettleber reproduziert wurden. In diesen fettreichen Lebern fiel dem Team auf, dass ein bestimmter genetischer Regulator, ein Transkriptionsfaktor namens C/EBPα, und ein kleines RNA‑Molekül, miR‑335‑5p, hochreguliert waren, während eine schützende Enzymuntereinheit namens PRKAA2, Bestandteil des bekannten Energiesensors AMPK, heruntergefahren war.
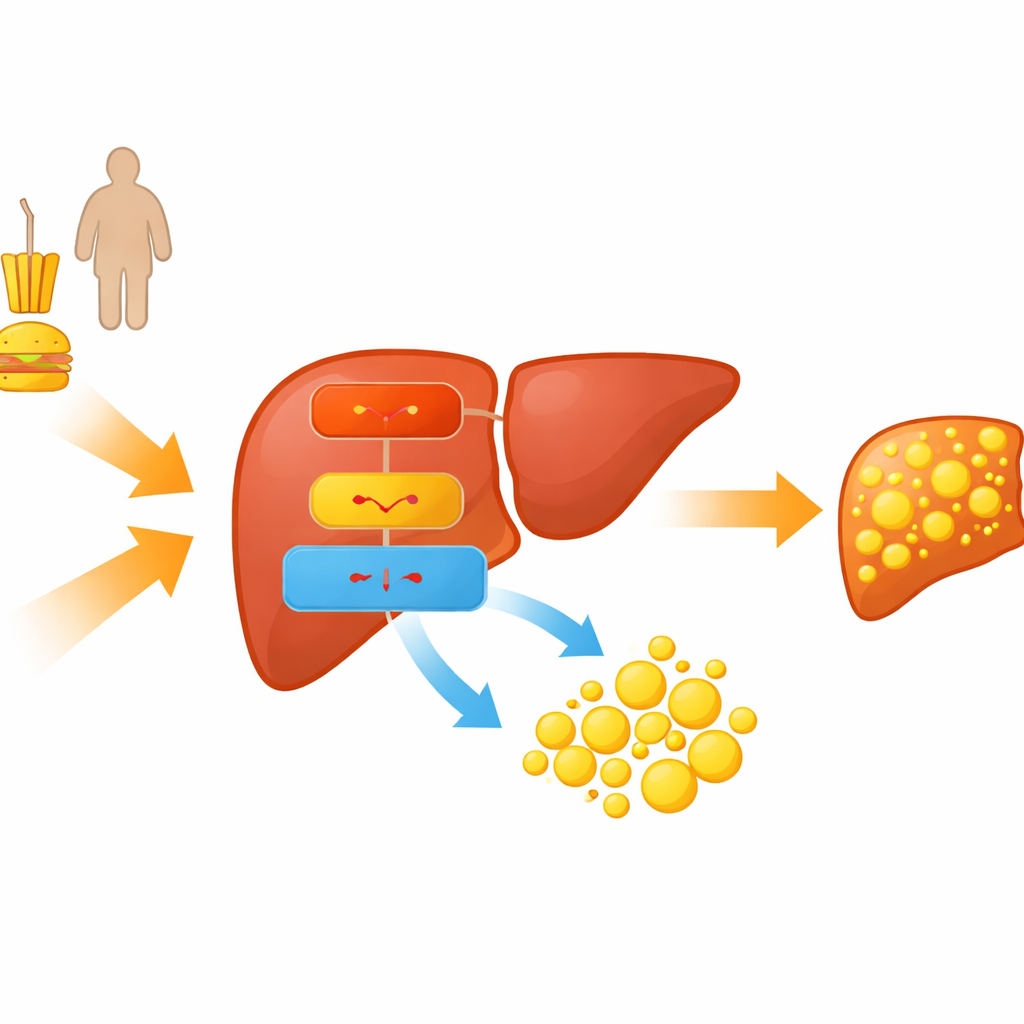
Wie eine kleine RNA das Gleichgewicht zugunsten von Fett verschiebt
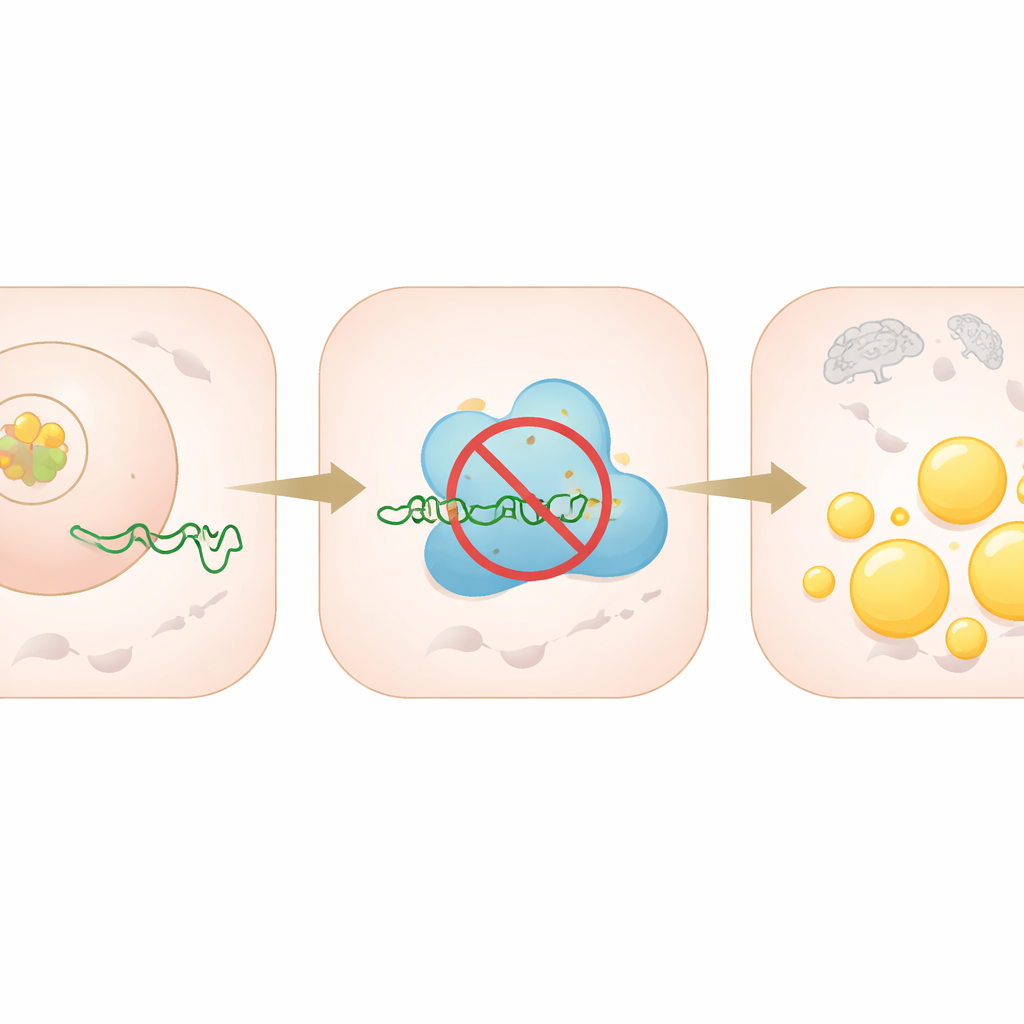
Kleine RNA‑Moleküle, sogenannte MicroRNAs, wirken wie molekulare Dimmer und dämpfen gezielt bestimmte Gene. Das Team zeigte, dass miR‑335‑5p direkt an die Botschaft bindet, die für PRKAA2 kodiert, und dadurch die Produktion dieses Proteins verhindert. PRKAA2 hilft beim Zusammenbau des AMPK‑Komplexes, der normalerweise Energiemangel erkennt und daraufhin die Fettbildung drosselt und den Fettabbau fördert. Wenn miR‑335‑5p in Leberzellen künstlich erhöht wurde, sanken die PRKAA2‑Spiegel, die AMPK‑Aktivität nahm ab und fettaufbauende Proteine stiegen an, was zu sichtbaren Ansammlungen von Fetttropfen führte. Wurde miR‑335‑5p blockiert, trat das Gegenteil ein: PRKAA2 und die AMPK‑Aktivität stiegen und die Fettansammlung nahm ab.
Der Hauptschalter, der die Kaskade auslöst
Was schaltet miR‑335‑5p überhaupt an? Durch das Durchmustern der DNA‑Region, die diese MicroRNA kontrolliert, sagten die Wissenschaftler mehrere mögliche Hauptschalter voraus und konzentrierten sich auf C/EBPα, das bereits dafür bekannt ist, Fett‑ und Zuckerstoffwechsel zu beeinflussen. Sie bestätigten, dass C/EBPα direkt an die Steuerregion von miR‑335‑5p bindet und deren Aktivität verstärkt. Eine Erhöhung von C/EBPα in Leberzellen hob die miR‑335‑5p‑Spiegel an, senkte PRKAA2, schwächte die AMPK‑Signalgebung und förderte die Fettansammlung. Die Stilllegung von C/EBPα hatte den umgekehrten Effekt, stärkte die energie‑sensing Bremse der Zelle und senkte die Lipidwerte. Rescue‑Experimente, bei denen miR‑335‑5p blockiert oder PRKAA2 wiederhergestellt wurde, zeigten, dass ein Großteil der fettfördernden Wirkung von C/EBPα über diese einzelne Kette vermittelt wird.
Von Zellkulturen zu lebenden Mäusen
Um zu prüfen, ob dieser Signalweg in lebenden Tieren relevant ist, setzten die Forschenden gentechnisch veränderte Viren ein, um genetische Werkzeuge direkt in die Lebern von fettreich gefütterten Mäusen zu bringen. Ein Werkzeug senkte die C/EBPα‑Spiegel, ein anderes fing überschüssiges miR‑335‑5p auf. In beiden Fällen enthielten die Lebern der Tiere weniger Fett, ihr mikroskopisches Erscheinungsbild verbesserte sich und PRKAA2 sowie die AMPK‑Aktivität erholten sich, während Proteine, die die Fettsynthese antreiben, zurückgingen. Diese In‑Vivo‑Ergebnisse stimmten mit den Zellkulturbefunden überein und unterstrichen, dass die C/EBPα–miR‑335‑5p–PRKAA2‑Kette nicht nur eine Laborbeobachtung ist, sondern ein starker Treiber der Fettleber in einem lebenden Organismus.
Was das für künftige Therapien bedeutet
Kurz gesagt zeigt die Studie eine dreistufige molekulare Relee, die Leberzellen dazu bringt, Fett zu horten: C/EBPα schaltet miR‑335‑5p an, das seinerseits PRKAA2 abschaltet und damit AMPK, die Energieregelbremse der Zelle, schwächt. Ist diese Bremse außer Kraft gesetzt, läuft die fettbildende Maschinerie unkontrolliert und die Leber wird mit Lipiden überfüllt. Das Unterbrechen eines beliebigen Glieds dieser Kette — die Dämpfung von C/EBPα, das Blockieren von miR‑335‑5p oder die Stärkung von PRKAA2/AMPK — verringerte die Fettmenge in den Lebern von Mäusen. Obwohl noch viel Arbeit nötig ist, bevor solche Strategien sicher beim Menschen angewendet werden können, bietet dieser Signalweg ein klares und überprüfbares Ziel für zukünftige Medikamente, die darauf abzielen, MASLD zu verlangsamen oder umzukehren.
Zitation: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
Schlüsselwörter: Fettlebererkrankung, MicroRNA, AMPK, Lipidstoffwechsel, Stoffwechselerkrankung