Clear Sky Science · de
Darmmikrobiota und Stoffwechselweg-Profile bei infizierten und nicht infizierten Herztransplantationspatienten vor und nach der Operation
Warum Ihr Darm nach einem neuen Herzen wichtig ist
Eine Herztransplantation kann Menschen mit schwerer Herzinsuffizienz eine zweite Lebenschance geben, doch Infektionen in den Wochen nach der Operation bleiben eine große Gefahr. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie verändert sich die Gemeinschaft von Mikroben in unserem Darm — die Darmmikrobiota — rund um die Herztransplantation, und können diese Veränderungen erklären, wer eine Infektion entwickelt und wer nicht?
Das winzige Ökosystem bei Transplantationspatienten
In unserem Darm leben Billionen von Bakterien, die bei der Verdauung helfen, das Immunsystem schulen und eindringende Krankheitserreger in Schach halten. Operation, starke immunsuppressive Medikamente und breitwirkende Antibiotika können dieses fragile Ökosystem aus dem Gleichgewicht bringen. Um nachzuvollziehen, was bei Herztransplantationspatienten passiert, begleiteten Forscher in China 20 Erwachsene, die ein Spenderherz erhielten. Sie sammelten Stuhlproben etwa eine Woche vor der Operation und erneut 30 Tage danach, untersuchten die DNA, um die vorhandenen Bakterien zu katalogisieren, und nutzten computergestützte Werkzeuge, um vorherzusagen, welche Stoffwechselaktivitäten diese Mikroben ausüben könnten.
Vier Patientengruppen, vier mikrobielle Muster
Das Team teilte die Patienten in vier Gruppen ein: solche mit und ohne Infektionen vor der Operation und solche mit und ohne Infektionen im ersten Monat nach der Operation. Vor der Transplantation waren die Gesamtdiversität und Struktur der Darmmikrobiota überraschend ähnlich, unabhängig davon, ob die Patienten bereits eine Infektion hatten oder nicht. Personen ohne voroperative Infektionen waren überwiegend von einer bekannten Gattung namens Bacteroides kolonisiert, die oft mit stabiler Darmgesundheit assoziiert wird. Im Gegensatz dazu zeigten infizierte Patienten eine Mischung, die potenziell schädliches Enterococcus casseliflavus neben häufig als günstig eingestuften Bakterien wie Limosilactobacillus und Weissella cibaria enthielt, was auf eine Darmgemeinschaft in fragiler, veränderlicher Balance hindeutet.
Nach der Operation: eine Gabelung im mikrobiellen Weg
30 Tage nach dem Eingriff bildeten sich bei den Patienten, die eine Infektion vermeiden konnten, ein erkennbares mikrobiales Muster, während jene mit Infektionen sehr unterschiedlich aussahen. Nicht infizierte Patienten wiesen reichere, ausgeglichenere Mikrobiota auf, mit vielen Vertretern der Gattung Blautia und verwandter Bakterien, die Butyrat produzieren — eine kurzkettige Fettsäure, die Darmzellen nährt und die Immunstabilität unterstützt. Ihre Darmökosysteme wirkten vielfältig und ausgewogen. Bei Patienten mit Infektionen dagegen sank die Diversität und die Gemeinschaft wurde von Enterococcus faecium dominiert, einem widerstandsfähigen Bakterium, das häufig bei Krankenhausinfektionen vorkommt und für Antibiotikaresistenzen bekannt ist. Statistische Analysen zeigten, dass sich die Mikrobiota dieser infizierten Gruppe deutlich von allen anderen abgrenzte, was auf eine klare postchirurgische Störung des Mikrobioms, also Dysbiose, hindeutet.
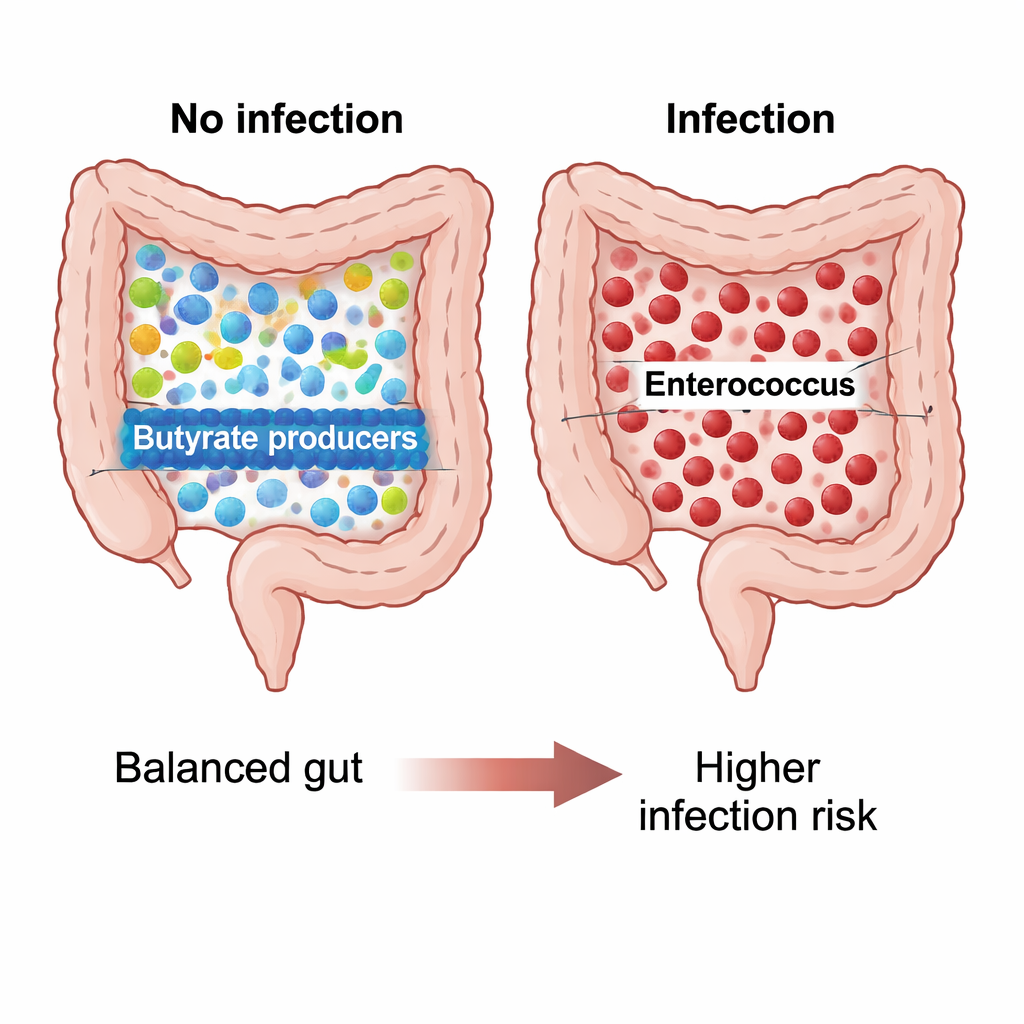
Mikrobielle Chemie verknüpft mit Schutz oder Risiko
Die Forscher untersuchten auch, welche chemischen Aufgaben diese Mikroben erfüllen könnten. Mittels prädiktiver Software stellten sie fest, dass bei der nicht-infizierten, postoperativen Gruppe Blautia mit Stoffwechselwegen verbunden war, die einen Stoff namens L-1,2-propandiol abbauen — ein Zwischenprodukt bei der Fermentation von Ballaststoffen, das letztlich die Produktion nützlicher Fettsäuren wie Propionat fördert. Bei infizierten Patienten war dieses vorhergesagte Stoffwechselpotenzial deutlich geringer, was zu einer Darmgemeinschaft passt, die weniger in der Lage ist, schützende Moleküle zu erzeugen. Vor der Operation war Enterococcus casseliflavus bei infizierten Patienten mit ungewöhnlichen Fermentationswegen verknüpft, die auf ein gestresstes, energiehungriges mikrobielles Umfeld hinweisen könnten, wobei hierfür noch direkte Laborbestätigungen nötig sind.
Was das für Patienten und Pflegeteams bedeutet
Für Menschen, die eine Herztransplantation bevorsteht, deuten diese Ergebnisse darauf hin, dass der Darm nicht nur ein Beobachter ist; er könnte das Risiko schwerer Infektionen mitgestalten. Die Studie zeigt eine dynamische Verschiebung von einer Bacteroides-Dominanz vor der Operation hin zu entweder schützendem Blautia-Reichtum oder schädlichem Enterococcus-Überwuchs danach, abhängig davon, wie sich die frühe Erholungsphase gestaltet. Starker infektionstypischer Stress und Antibiotikaanwendung scheinen die Darmgemeinschaft in den Enterococcus-dominierten, niedrigdiversen Zustand zu treiben, wie er bei infizierten Patienten beobachtet wurde. Die Autoren schlagen eine „Dual-Target“-Strategie vor: die Rückkehr butyratproduzierender Bakterien fördern — möglicherweise durch Ernährung oder gezielt ausgewählte Probiotika — und gleichzeitig Enterococcus-Spiegel engmaschig überwachen. Zwar sind größere und längere Studien erforderlich, doch eröffnet diese Arbeit die Möglichkeit, dass die Feinabstimmung der Darmmikrobiota künftig ein routinemäßiger Teil der Transplantationsversorgung wird, um Patienten vor lebensbedrohlichen Infektionen zu schützen.
Zitation: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Schlüsselwörter: Herztransplantation, Darmmikrobiota, postoperative Infektion, Antibiotika, butyratproduzierende Bakterien