Clear Sky Science · de
Verbesserte kinetische Leistung und Stabilität von Katalase, immobilisiert auf epoxy-funktionalisiertem Kaolinit
Aus einem natürlichen Ton einen intelligenten Reiniger machen
Wasserstoffperoxid wird breit eingesetzt, um zu desinfizieren, zu bleichen und Wasser zu behandeln, doch Reste von Peroxid in industriellen Abwässern können lebende Zellen und die Umwelt schädigen. Die Natur bietet bereits ein wirksames Reinigungswerkzeug: das Enzym Katalase, das Wasserstoffperoxid in ungefährliches Wasser und Sauerstoff zerlegt. Freie Enzyme sind jedoch empfindlich und schwer wiederzuverwenden. Diese Studie zeigt, wie ein verbreiteter Tonmineral, Kaolinit, schonend so verändert werden kann, dass Katalase fest daran haftet und so eine robustere, wiederverwendbare „Reinigungsoberfläche“ bildet, die industrielle Prozesse und Abwasserbehandlung sicherer und nachhaltiger machen könnte. 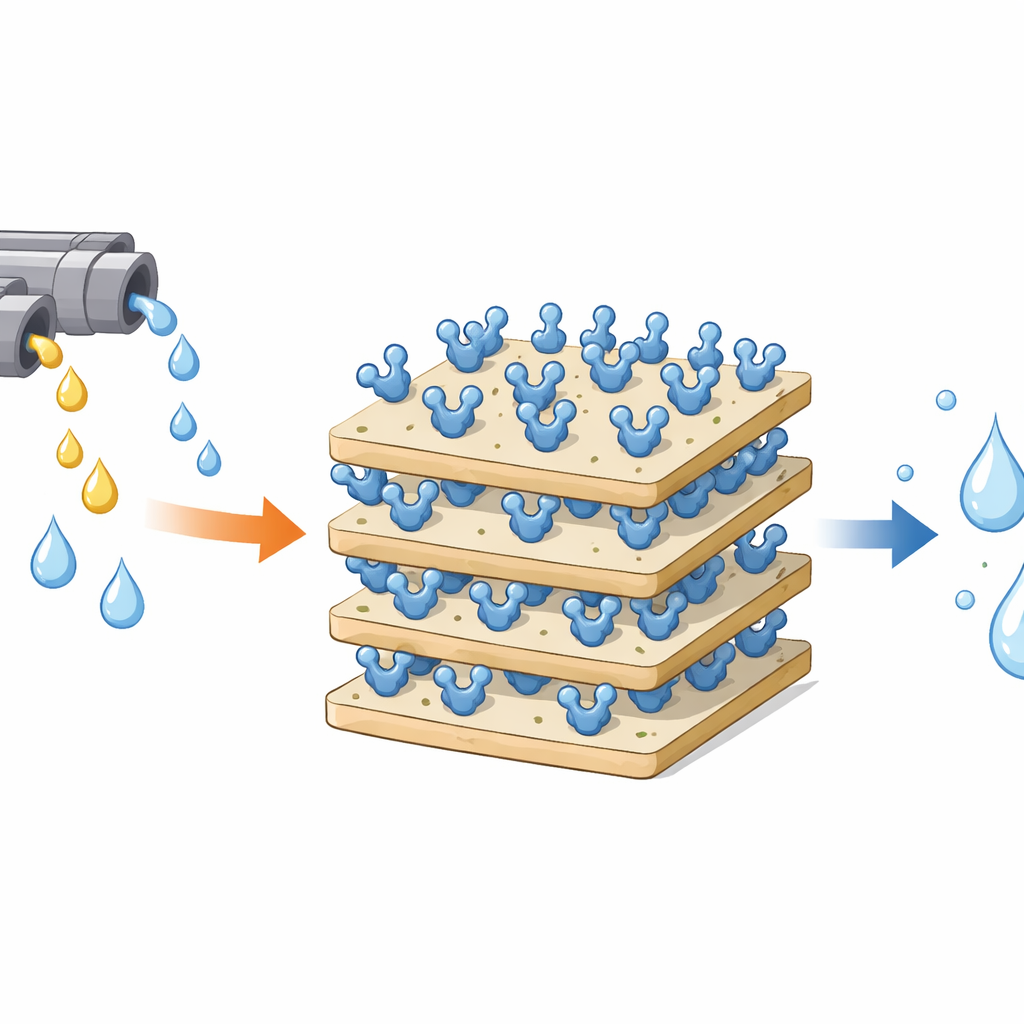
Ein gewöhnliches Mineral mit verborgenem Potenzial
Kaolinit ist ein kostengünstiger, weit verbreiteter weißer Ton, der in Papier, Keramik und sogar in der Medizin Verwendung findet. Er besitzt eine geschichtete Struktur, die mechanisch stabil und chemisch beständig ist, aber seine Oberfläche ist relativ träge, sodass Enzyme nicht gut haften und leicht ausgewaschen werden. Frühe Versuche, Katalase auf unbehandeltem Kaolinit zu halten, setzten überwiegend auf schwache Anziehungskräfte. Diese Systeme konnten zwar etwas Enzym binden, litten jedoch unter geringer Beladung, leichtem Auswaschen und Aktivitätsverlust über die Zeit. Die Autoren vermuteten, dass sich der Ton, sofern man reaktive Stellen einführen kann, ohne seine Struktur zu zerstören, zu einer robusten, langlebigen Plattform für Katalase entwickeln ließe.
Aufbringen einer haftenden, aber schonenden Beschichtung
Um Kaolinit aufzuwerten, beschichteten die Forscher seine Oberfläche mit einem kleinen Molekül namens GPTMS, einer Silanverbindung mit einer Epoxygruppe. In Wasser-Alkohol-Gemischen unter leicht sauren Bedingungen wandelt sich GPTMS zunächst zu Silanolgruppen um, die an die natürlichen Hydroxylgruppen des Tons binden und eine dünne, dauerhafte organische Schicht bilden. Die Epoxyanteile bleiben erhalten und ragen als kleine, reaktive Ringe von der Oberfläche ab. Eine Reihe von Techniken bestätigte diese Umwandlung: Infrarotspektren zeigten neue Kohlenstoff–Wasserstoff- und epoxybezogene Schwingungen; Elektronenmikroskopaufnahmen offenbarten, dass der ursprünglich kompakte platenartige Ton offener und poröser wurde; thermische Analysen detektierten zusätzlichen Masseverlust bei moderaten Temperaturen aufgrund der neu angelagerten organischen Schicht; und Oberflächenspektroskopie zeigte deutlich mehr Kohlenstoff auf dem modifizierten Ton bei Erhalt des zugrundeliegenden Mineralgerüsts.
Andocken des Enzyms an den Ton
Wurde Katalase mit diesem epoxyhaltigen Kaolinit gemischt, heftete sich das Enzym schnell an die Oberfläche. Innerhalb der ersten Stunde waren die meisten Bindungsstellen bereits besetzt, und das Gleichgewicht war im Wesentlichen nach vier Stunden erreicht. Der modifizierte Ton konnte etwa 300 Milligramm Katalase pro Gramm Träger aufnehmen — deutlich mehr als frühere kaolinitbasierte Systeme. Das Team stellte fest, dass neutraler pH und moderate Temperaturen (etwa Raum- bis Körpertemperatur) für die Beladung am günstigsten waren; dies spiegelt ein Gleichgewicht zwischen Enzymstabilität und der Reaktivität von Aminogruppen im Protein mit den Epoxyringen auf der Oberfläche wider. Auf molekularer Ebene greifen nukleophile Gruppen der Katalase die angespannten Epoxyringe an und bilden mehrere starke Bindungen. Diese Mehrfachverankerung begrenzt schädliche Bewegungen, hält aber das aktive Zentrum zugänglich. 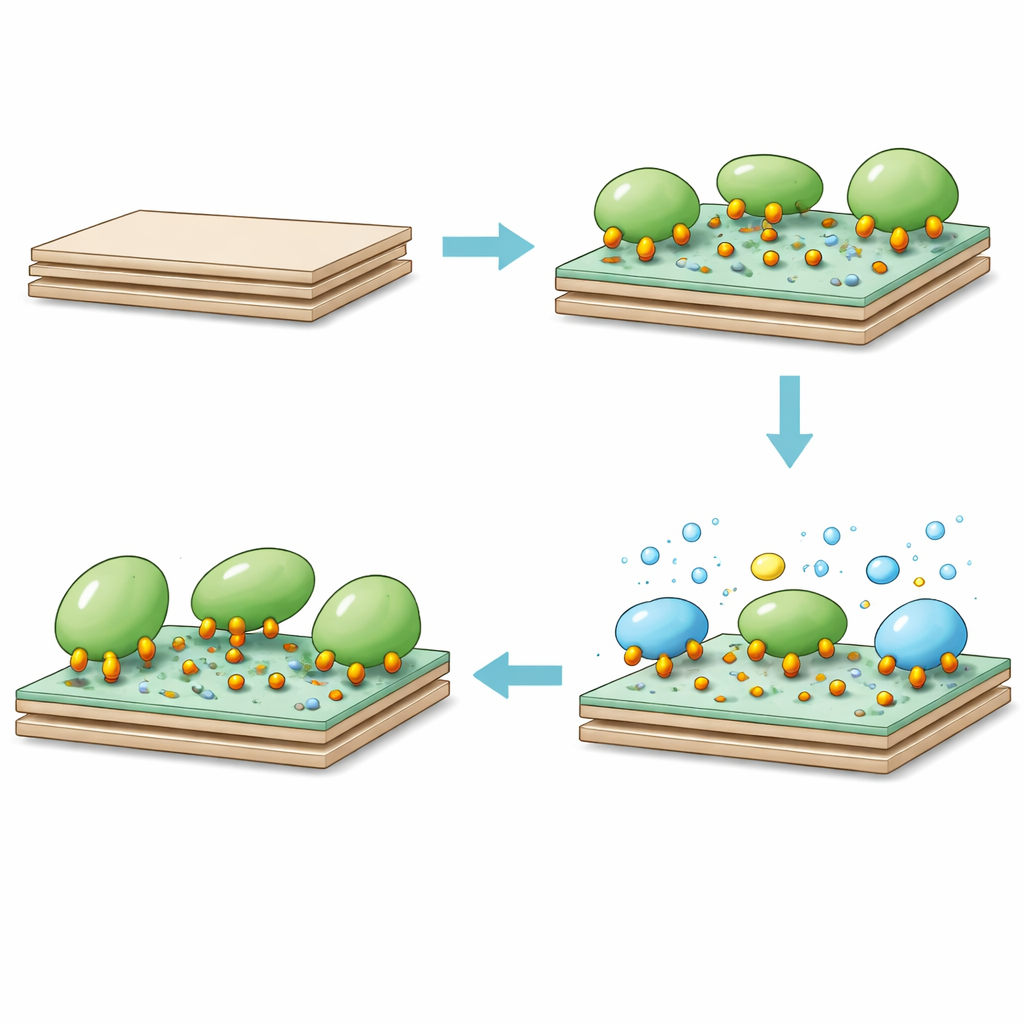
Schnelleres, robusteres und langlebigeres Wirken
Die Anlagerung der Katalase an den modifizierten Ton veränderte ihr Verhalten gegenüber Wasserstoffperoxid. Das immobilisierte Enzym zeigte eine deutlich geringere scheinbare „Nachfrage“ nach Substrat als das freie Enzym, was bedeutet, dass es effizient arbeiten kann, selbst wenn die Peroxidkonzentration moderat ist. Zwar sank die maximale Reaktionsgeschwindigkeit etwas — vermutlich weil Diffusion durch die feste Schicht und reduzierte Enzymflexibilität die Reaktion verlangsamen —, doch die gesamte katalytische Effizienz stieg um etwa 80 Prozent. Ebenso wichtig war, dass die immobilisierte Katalase wiederholte Nutzung und lange Lagerung weitaus besser überstand als die freie Form. Sie behielt nach vielen Reaktionszyklen hohe Aktivität und behielt nach Wochen im Kühllager einen deutlich größeren Anteil ihrer ursprünglichen Leistung. Der Tonsupport selbst ließ sich ebenfalls regenerieren und mehrmals für neue Enzymbeladungen wiederverwenden, mit nur allmählichem Kapazitätsverlust.
Warum das im Alltag wichtig ist
Vereinfacht gesagt verwandelt die Studie einen vertrauten, preiswerten Ton in einen intelligenten, wiederverwendbaren Träger für ein natürliches Entgiftungsenzym. Durch gezielte Gestaltung der Tonoberfläche mit einer dünnen, epoxyreichen Schicht schufen die Forscher eine Plattform, die Katalase fest anzieht, ihr hilft, das Substrat leichter zu erkennen, und sie vor Schäden schützt. Das bedeutet, dass wir potenziell peroxidehaltige Industrieabwässer reinigen, fortschrittliche Oxidationsprozesse unterstützen oder sicherere Behandlungen in der Lebensmittel- und Pharmaindustrie mit geringeren Enzymmengen über längere Zeiträume realisieren können. Die Arbeit zeigt, wie das Abstimmen der Grenzfläche zwischen Mineralien und Proteinen neue, dauerhafte Werkzeuge für grünere Technologien erschließen kann.
Zitation: Erol, K., Veyisoğlu, A., Tatar, D. et al. Enhanced kinetic performance and stability of catalase immobilized on epoxy-functionalized kaolinite. Sci Rep 16, 8196 (2026). https://doi.org/10.1038/s41598-026-38910-z
Schlüsselwörter: Enzymimmobilisierung, Katalase, Kaolinit-Ton, Abwasserbehandlung, epoxy-funktionalisierte Oberfläche