Clear Sky Science · de
Veränderte Expression der CD26/ADA-Achse bei immunvermittelter Entzündung der infektiösen Mononukleose
Warum dieses Kinderheitsvirus wichtig ist
Viele Eltern kennen die infektiöse Mononukleose, oft „Mono“ genannt, als eine unangenehme, aber meist vorübergehende Krankheit mit Fieber, Halsschmerzen und geschwollenen Lymphknoten. In einer kleinen Zahl von Kindern kann die Infektion jedoch schwer verlaufen und Organe wie die Leber schädigen. Diese Studie beleuchtet im Detail, wie das Immunsystem von Kindern auf das Epstein‑Barr‑Virus, die Hauptursache von Mono, reagiert, und konzentriert sich auf ein Paar winziger Oberflächenpartner — CD26 und ein Enzym namens ADA — die erklären könnten, warum manche Immunreaktionen gefährlich heftig werden.
Die körpereigenen Verteidiger in Übersteuerung
Wenn das Epstein‑Barr‑Virus in den Körper eindringt, infiziert es vornehmlich bestimmte weiße Blutkörperchen und löst eine starke Immunreaktion aus. In der Studie verglichen die Ärzte Blutproben von 30 Kindern mit akuter Mono mit 30 gesunden Kindern. Sie stellten fest, dass die kranken Kinder insgesamt deutlich mehr weiße Blutkörperchen hatten, insbesondere eine Untergruppe namens CD8‑T‑Zellen, die darauf spezialisiert ist, infizierte Zellen zu töten. Gleichzeitig war eine andere wichtige Hilfsgruppe, die CD4‑T‑Zellen, relativ reduziert, sodass das übliche Gleichgewicht zwischen „Angriff“ und „Unterstützung“ umgekippt war. Auch die Konzentrationen von infektionabwehrenden Proteinen im Blut, einschließlich mehrerer Botenstoffe, die Entzündungen hoch- oder herunterregulieren, waren erhöht — ein Hinweis darauf, dass das Immunsystem voll aktiviert war.
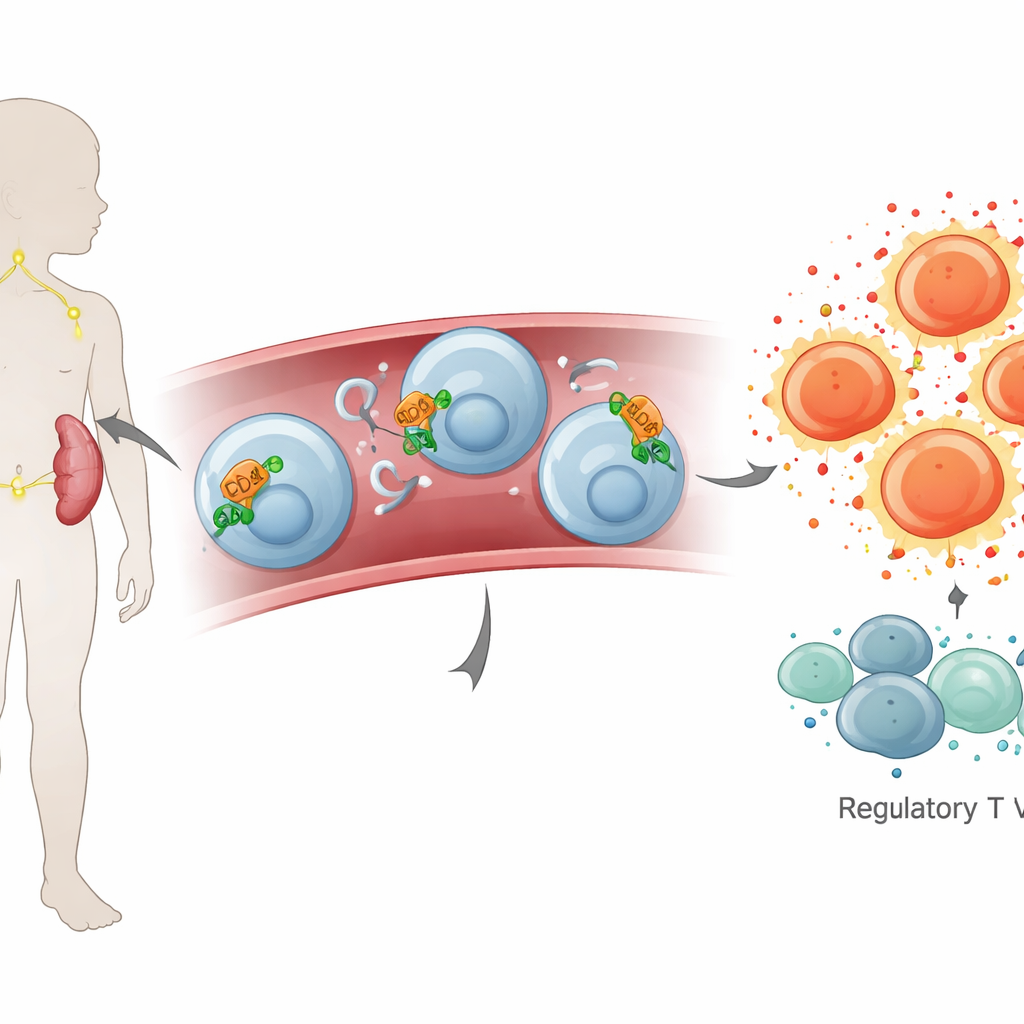
Ein genauer Blick auf einen winzigen Steuerknopf
Die Forschenden richteten ihren Fokus dann auf CD26 und ADA, zwei Moleküle, die an der Schnittstelle zwischen Zellaktivierung und chemischer Signalgebung außerhalb der Zellen sitzen. Mit genetischen Tests an Blutzellen fanden sie heraus, dass Kinder mit Mono höhere Mengen an CD26‑ und ADA‑Anweisungen (mRNA) aufwiesen, was darauf hindeutet, dass die Immunzellen sich darauf vorbereiten, mehr dieser Proteine herzustellen. Blutuntersuchungen bestätigten, dass die ADA‑Aktivität selbst erhöht war. Interessanterweise unterschied sich die zirkulierende Menge des CD26‑Proteins im Plasma kaum zwischen kranken und gesunden Kindern, was nahelegt, dass dieses Molekül bei Mono überwiegend an Zelloberflächen verbleiben könnte, statt frei im Blut zu zirkulieren.
Verschiebung des Gleichgewichts zwischen Angriff und Zurückhaltung
Um zu verstehen, wie sich dieser Steuermechanismus auf verschiedenen Immunzellen verhielt, nutzte das Team Durchflusszytometrie, eine Methode, die Zellen einzeln zählt und charakterisiert. Auf CD8‑T‑Zellen, die sich während der Mono dramatisch vermehren, war CD26 häufiger anzutreffen — unabhängig davon, ob die Zellen einen weiteren Marker namens CD39 trugen, der mit einem starken chemischen Bremssystem in Verbindung steht. Dieses Muster legt nahe, dass CD26 in diesen „Killer“-Zellen dazu beitragen könnte, lokale chemische Signale zu überwinden, die normalerweise ihre Aktivität dämpfen würden, und so einen kräftigen Angriff auf virusinfizierte Zellen zu unterstützen. Gleichzeitig war das Bild bei CD4‑T‑Zellen, die üblicherweise bei der Koordination von Immunantworten helfen, gemischter. Zellen, die sowohl CD4 als auch CD39 trugen — oft mit regulatorischen, beruhigenden Funktionen assoziiert — waren relativ häufiger, was die hohen Spiegel von dämpfenden Signalen wie dem Zytokin IL‑10 erklären könnte.
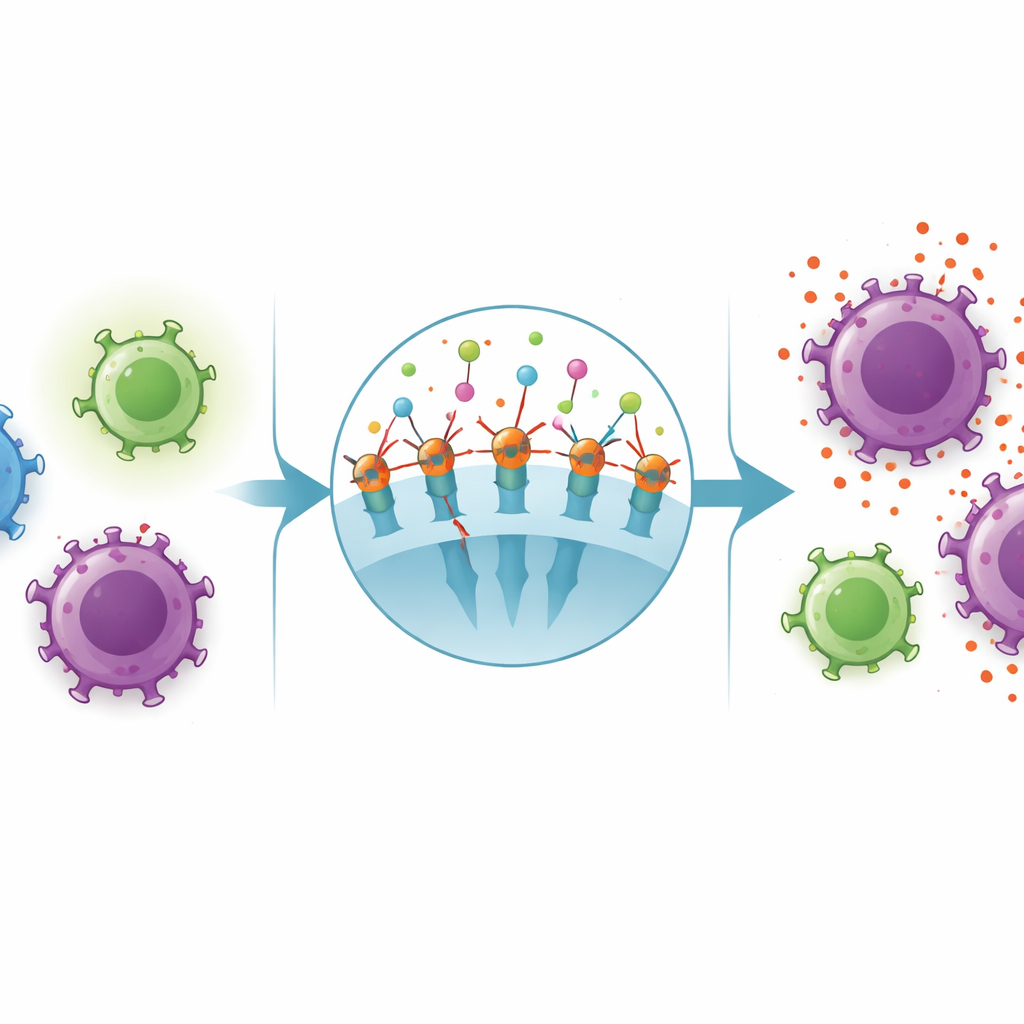
Wenn die Regulation schwächer wird
Innerhalb der CD4‑Population, die kein CD39 trägt und typischerweise aus aktiven Helferzellen besteht, war der Anteil der Zellen, die CD26 zeigten, bei Kindern mit Mono tatsächlich niedriger als bei gesunden Gleichaltrigen. Dieser Verlust von CD26 auf Helferzellen könnte ihre Fähigkeit verringern, zu proliferieren und ausgewogene Reaktionen zu koordinieren, selbst während CD8‑Zellen zu stärkerer Aktivität gedrängt werden. Die Studie zeigte außerdem, dass die Menge an CD26 im Plasma mit ADA‑Spiegeln und mit Interferon‑Gamma, einem starken Entzündungssignal, korrelierte und umgekehrt mit dem Anteil an CD4‑T‑Zellen sowie mit dem CD4‑zu‑CD8‑Verhältnis verknüpft war. Zusammengenommen deuten diese Muster darauf hin, dass die CD26/ADA‑„Achse“ eng mit der Intensität der Immunantwort während der Infektion verbunden ist.
Was das für kranke Kinder bedeutet
Für Familien und Klinikpersonal liefern diese Befunde ein klareres Bild davon, warum ein verbreitetes Virus manchmal zu besorgniserregenden Erkrankungen führen kann. Bei akuter Mono scheint das Immunsystem der Kinder stark auf CD8‑T‑Zellen zu setzen, die mit gesteigerter CD26‑ADA‑Aktivität ausgerüstet sind, und erzeugt so einen kräftigen antiviralen Schub, der das Risiko birgt, überzuschießen und Gewebe zu schädigen. Zugleich verlieren bestimmte Helfer‑ und Regulierungszellen ihre CD26‑Profile oder verändern sie, was womöglich die Bremsen schwächt, die normalerweise Entzündungen kontrollieren. Obwohl weitere Forschung nötig ist — insbesondere bei sehr schweren Verläufen — legt die Studie nahe, dass das Messen und möglicherweise Modulieren der CD26/ADA‑Achse eines Tages Ärzten helfen könnte, den Schweregrad der Erkrankung einzuschätzen oder Therapien zu entwickeln, die schädliche Immunreaktionen dämpfen, ohne die Abwehrkräfte des Körpers vollständig abzuschalten.
Zitation: Shi, T., Shi, W., Tian, J. et al. Altered expression of the CD26/ADA axis in immune-mediated inflammation of infectious mononucleosis. Sci Rep 16, 9316 (2026). https://doi.org/10.1038/s41598-026-38891-z
Schlüsselwörter: infektiöse Mononukleose, Epstein-Barr-Virus, T‑Zellen, Immunregulation, Adenosin‑Weg