Clear Sky Science · de
Einzelzell-Massendichte-Messungen mittels Microchannel-Gradientenzentrifugation
Warum das Wiegen winziger Zellen wichtig ist
Jede lebende Zelle ist mehr als nur ein Beutel voller Moleküle; ihr Gewicht und ihre Packungsdichte erzählen etwas über ihren Zustand. Feine Veränderungen in der Dichte einer Zelle können anzeigen, ob sie wächst, stirbt, eine Infektion bekämpft oder sich in Richtung Krebs verändert. Dennoch blieb das Messen der Massendichte von Tausenden einzelner Zellen bislang langsam, technisch anspruchsvoll und teuer. Dieser Artikel stellt eine neue, deutlich einfachere Methode vor, um Einzelzellen „zu wiegen“, indem man beobachtet, wie sie in einer kontrollierten Flüssigkeit innerhalb eines haarfeinen Glaskanals in einer Zentrifuge schwimmen oder sinken.
Eine neue Wendung eines alten Labotricks
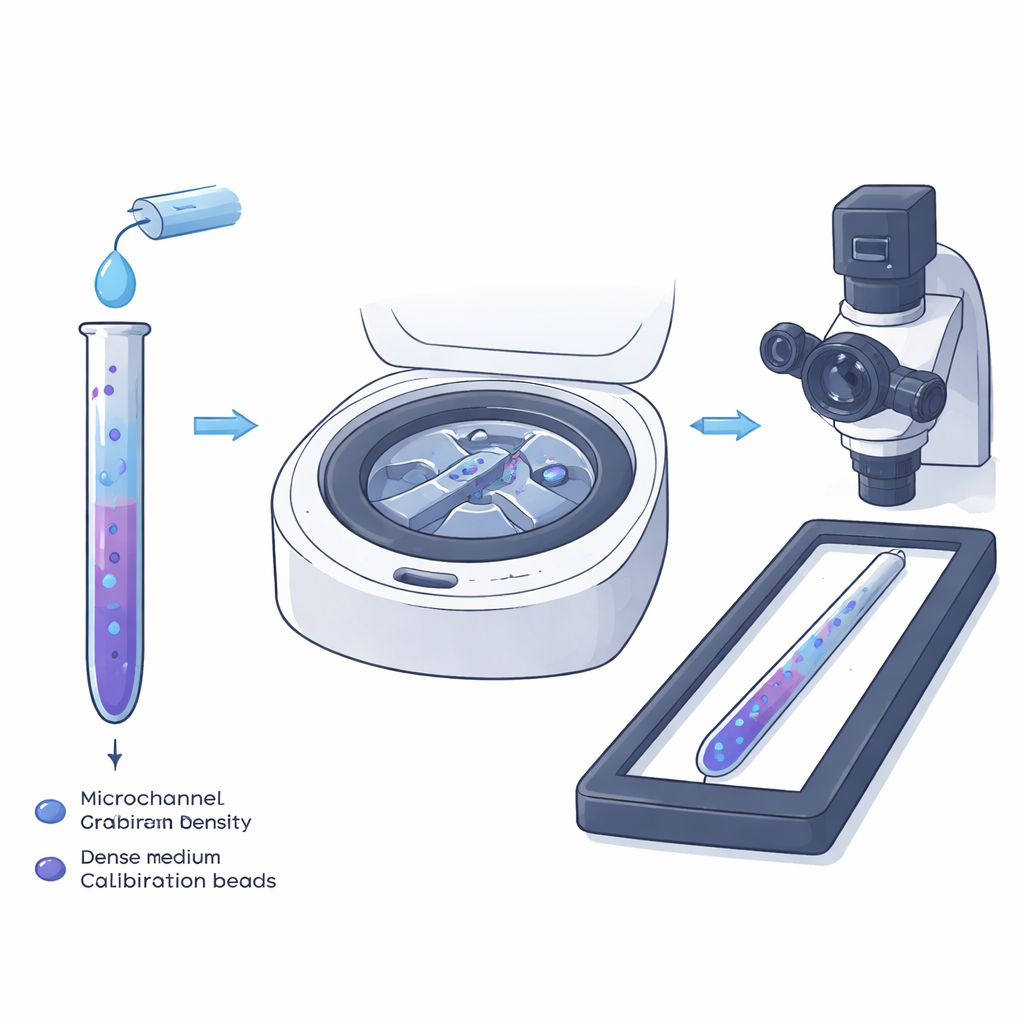
Die traditionelle Dichtegradienten-Zentrifugation wird seit langem in Reagenzgläsern eingesetzt, um Gemische von Zellen zu trennen: Beim Drehen setzen sich Zellen an der Stelle in einer geschichteten Flüssigkeit ab, an der ihre eigene Dichte der der Umgebung entspricht. Die Autorinnen und Autoren miniaturisieren diese Idee in einen schmalen Mikrokanal, sodass einzelne Zellen und nicht nur Schichten direkt unter dem Mikroskop gemessen werden können. Sie füllen den Kanal zunächst mit einer leichten Flüssigkeit, die die Zellen enthält, und anschließend mit einer dichteren Flüssigkeit, die winzige Kunststoffpartikel mit genau bekannten Dichten enthält. Wenn diese beiden Flüssigkeiten im winzigen Kanal aufeinandertreffen und strömen, bilden sie auf natürliche Weise einen glatten, eindimensionalen Dichtegradienten entlang seiner Länge.
Schaffung einer sanften Dichte-Steigung
In solchen dünnen Kanälen fließt die Flüssigkeit langsam und gleichmäßig, ohne Turbulenzen. Unter diesen Bedingungen mischt das parabolische Strömungsprofil die leichte und die schwere Flüssigkeit gerade so weit, dass eine allmähliche Übergangszone statt einer scharfen Grenzfläche entsteht. Das Team untersuchte diesen Prozess sowohl experimentell mit einem fluoreszierenden Farbstoff als auch per Computersimulation. Sie fanden heraus, dass sich innerhalb von Sekunden ein nahezu linearer Dichtegradient über mehrere Millimeter ausbilden kann. Die Kanalhöhe erwies sich als entscheidend: flache Kanäle halten den Gradient stabil und verhindern durch die Schwerkraft verursachtes Schwenken der dichteren Flüssigkeit, das die Positions-Dichte-Beziehung verwischen und Messfehler einführen würde.
Zellen bis zu ihrem Gleichgewichtspunkt drehen
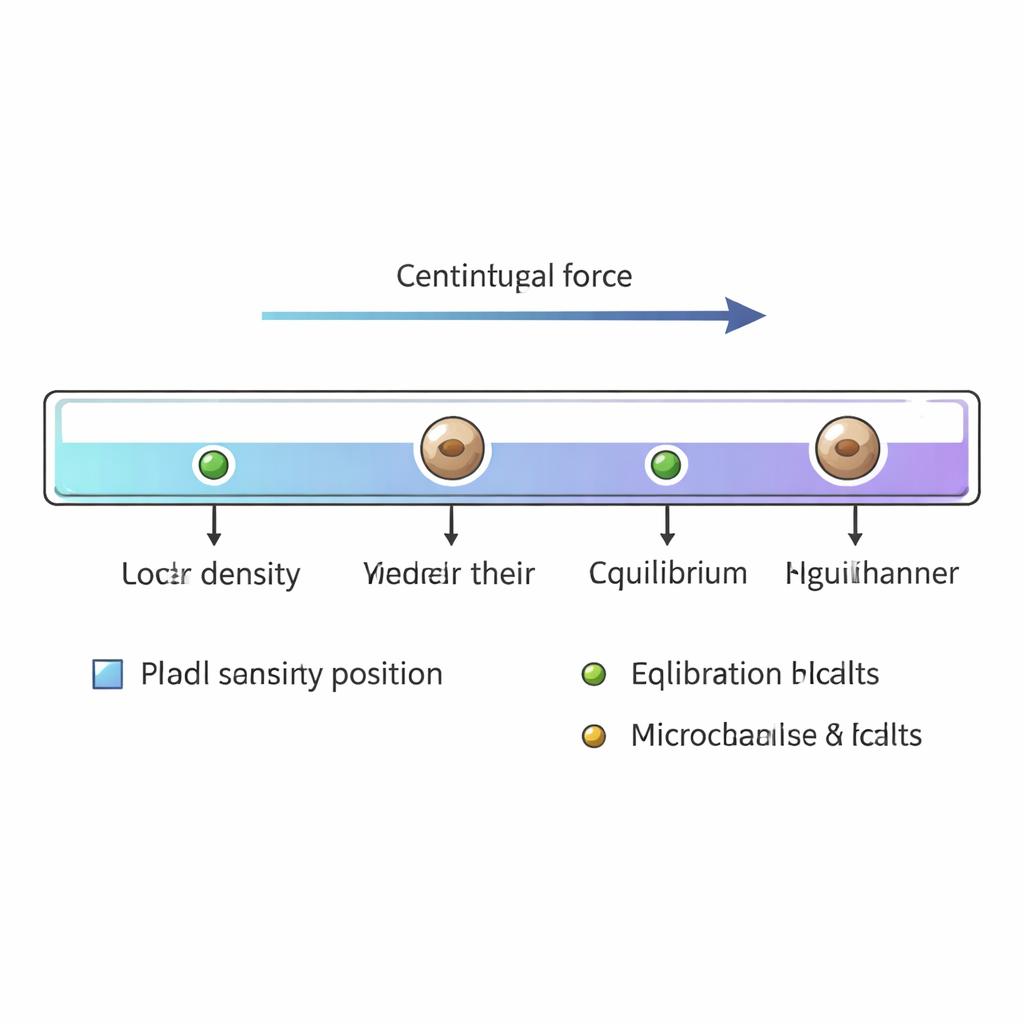
Nachdem der Kanal befüllt ist, werden seine Enden verschlossen und er wird in einer kleinen Zentrifuge platziert. Bei etwa 12.000 Umdrehungen pro Minute bewegen sich Zellen und Kalibrierungskügelchen entlang des Kanals, bis die nach außen wirkende Zentrifugalkraft durch den Auftrieb bei ihrer jeweiligen Dichte genau ausgeglichen ist. Hefezellen mit Durchmessern größer als etwa drei Mikrometer erreichen dieses Gleichgewicht in unter 20 Sekunden. Nach ungefähr anderthalb Minuten Drehen wird der Kanal entnommen und unter einem Standardmikroskop gescannt. Die Forschenden protokollieren die Positionen von Tausenden einzelner Hefezellen und der Referenzkugeln und wandeln dann jede Position entlang des Gradienten mittels der bekannten Dichten der Kugeln in einen Massendichtewert um.
Zellzustand aus winzigen Unterschieden ablesen
Mithilfe dieses Verfahrens bestimmten die Autorinnen und Autoren die Dichten von mehr als 20.000 Hefezellen über mehrere Kanäle hinweg. Die typische Messunsicherheit für eine einzelne Zelle lag bei etwa 3,3 Kilogramm pro Kubikmeter — klein genug, um echte biologische Unterschiede aufzulösen, die in ihren Proben etwa doppelt so groß waren. Über viele Stunden beobachteten sie, dass die Hauptpopulation der Hefen eine stabile Dichte behielt, während allmählich eine zweite, dichtere und leicht kleinere Population erschien. Diese dichtere Gruppe bestand wahrscheinlich aus toten oder beschädigten Zellen, die die schwere Flüssigkeit aufgenommen hatten und dadurch kompakter erschienen. Die gemessenen Werte stimmten gut mit Ergebnissen weit aufwändigerer und langsamerer Techniken wie suspendierten Mikrokanal-Resonatoren, optischen Methoden und magnetischer Levitation überein.
Vom Laborprototyp zum praktischen Biomarker
Die Studie zeigt, dass eine einfache Kombination aus Glas-Mikrokanälen, handelsüblichen Zentrifugen und Standardmikroskopen hochdurchsatzfähige Einzelzell-Dichtemessungen mit Raten von etwa 16.000 Zellen pro Stunde ermöglichen kann. Zwar ist die Methode noch nicht empfindlich genug, um die kleinsten durch Medikamente ausgelösten Veränderungen zu erfassen, doch reicht sie bereits aus, um verschiedene Zelltypen oder lebende von toten Zellen anhand ihrer Packungsdichte zu unterscheiden. Indem präzises „Zellwiegen“ zugänglicher und erschwinglicher wird, könnte diese Microchannel-Gradienten-Methode dazu beitragen, die Zellmassendichte zu einem routinemäßigen Biomarker für die Krankheitsüberwachung, die Bewertung von Therapien und die Erforschung der zellulären Innenstruktur zu machen.
Zitation: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Schlüsselwörter: Einzelzell-Dichte, Microfluidik, Zentrifugation, Hefezellen, Zell-Biomarker