Clear Sky Science · de
Konformationsdynamik und Bindungsfreie-Energie-Analysen enthüllen einen stabilen Flavonoid-Inhibitor der NS5-Polymerase des Dengue-Virus
Warum ein von Mücken übertragener Virus pflanzliche Hilfe braucht
In den letzten Jahren hat sich Dengue-Fieber weltweit explosionsartig ausgebreitet, Millionen Menschen erkrankt und Tausende gestorben. Dennoch fehlt uns weiterhin eine breit wirksame, bezahlbare antivirale Tablette zur Behandlung Infizierter. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Lassen sich natürlich vorkommende Pflanzenstoffe in präzise molekulare „Schraubenschlüssel“ verwandeln, die eine der wichtigsten Maschinen des Dengue-Virus blockieren?
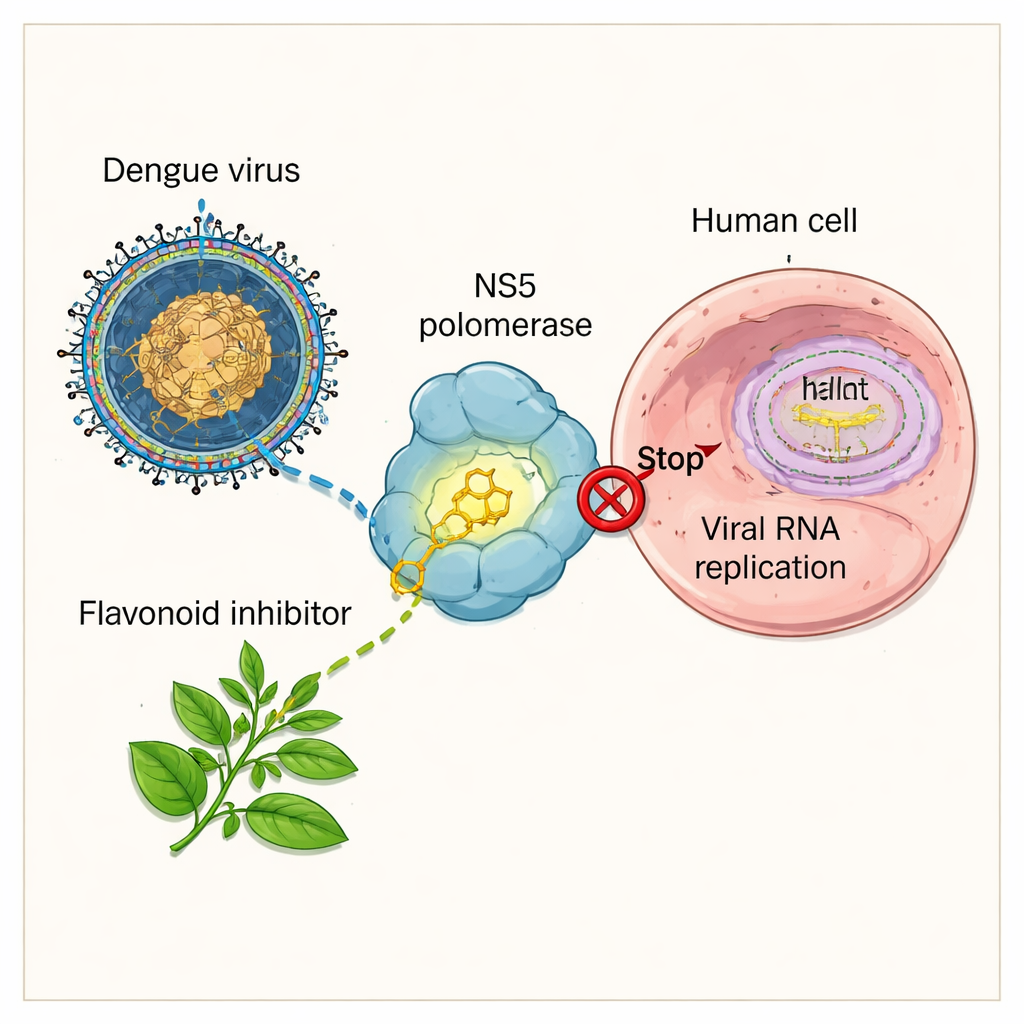
Die Virenmaschine, die Wissenschaftler zum Stillstand bringen wollen
Das Dengue-Virus überlebt, indem es sein genetisches Material in unseren Zellen kopiert. Dafür ist ein Schlüsselprotein namens NS5 verantwortlich, das wie ein winziger Kopiermotor für die virale RNA wirkt. Wenn NS5 ausfällt, kann das Virus keine neuen Genome erzeugen und die Infektion kommt zum Stillstand. Deshalb gilt NS5—insbesondere sein RNA-kopierender Teil, die RNA-abhängige RNA-Polymerase—als vielversprechendes Ziel für neue Medikamente. Mehrere synthetische Verbindungen und Pflanzenextrakte haben bereits gezeigt, dass NS5 blockiert werden kann, doch viele frühe Kandidaten weisen schwache Bindung, Instabilität oder Bedenken hinsichtlich Sicherheit und Pharmakokinetik auf.
Auf der Suche nach vielversprechenden chemischen Nadeln im Heuhaufen der Pflanzen
Die Forschenden konzentrierten sich auf Flavonoide, eine große Familie pflanzlicher Verbindungen, die in Lebensmitteln wie Beeren, Tee und Kräutern vorkommen und seit langem für antivirale und entzündungshemmende Effekte bekannt sind. Aus einer kuratierten Datenbank pflanzlicher Sekundärstoffe wählten sie 326 Flavonoide aus und erstellten dreidimensionale Modelle sowohl des NS5-Enzyms als auch jeder Kandidatenmoleküle. Mithilfe schrittweiser Computersimulationen (Docking) stellten sie die Frage: Welche Formen passen am besten in eine bestimmte „Hintertür“-Region von NS5, die N-Tasche—eine allosterische Stelle, die das Enzym ausschalten kann, wenn sie besetzt ist und die tendenziell weniger Mutationen aufweist als die Hauptaktiva?
In jeder Phase dieses virtuellen Screenings wurden Verbindungen, die schlecht passten oder unwahrscheinlich waren, sich im Körper wie echte Medikamente zu verhalten, verworfen. Die verbleibenden Moleküle wurden nicht nur nach geometrischer Passform, sondern auch nach geschätzter Bindungsstärke bewertet, mithilfe einer Methode, die die Energien approximiert, die beim Andocken einer Verbindung an NS5 in wässrigen, zellähnlichen Bedingungen beteiligt sind. Dieser Prozess reduzierte das Feld auf eine Handvoll Top-Flavonoide, wobei ein Kandidat, bezeichnet als PSCdb01560, durch besonders starke vorhergesagte Bindungsenergie hervorstach.
Moleküle im virtuellen Mikroskop beobachten
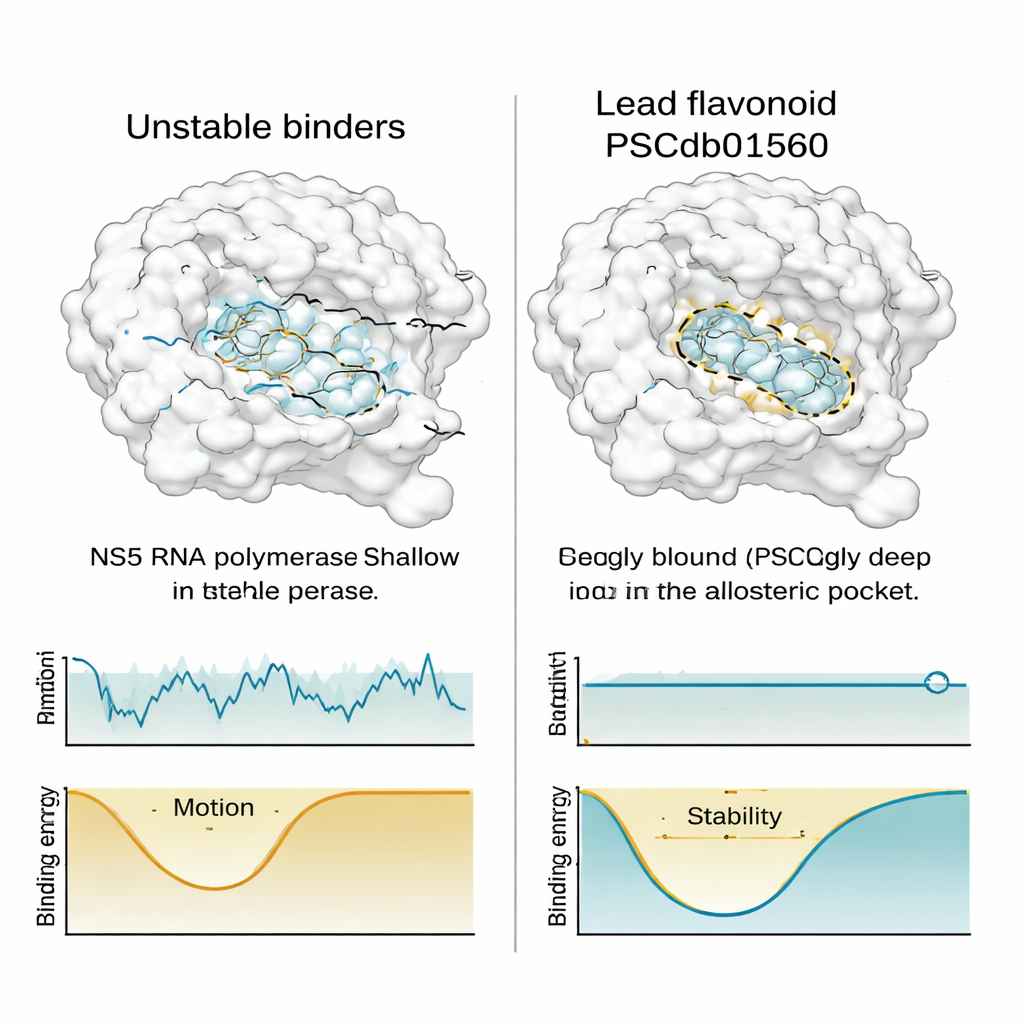
Eine gute Passform in einer statischen Aufnahme reicht nicht aus; ein brauchbares Medikament muss auch dann an seinem Platz bleiben, wenn alles in Bewegung ist. Um das zu testen, führten die Forscher lange, detaillierte Molekulardynamik-Simulationen durch—Computervideos mit einer Dauer von umgerechnet einer halben Mikrosekunde—for NS5 zusammen mit den besten Flavonoiden und einem bekannten Referenzinhibitor. Sie verfolgten, wie sehr sich das Protein und jedes Molekül bewegten, wie kompakt der Komplex blieb, wie stark er dem umgebenden Wasser ausgesetzt war und wie oft wichtige chemische Kontakte entstanden und wieder zerbrachen. PSCdb01560 zeigte bemerkenswert konstantes Verhalten: Es blieb tief in der N-Tasche verankert, bewegte sich deutlich weniger als konkurrierende Moleküle und schien die Gesamtform von NS5 zu stabilisieren, statt sie zu stören.
Im Gegensatz dazu begannen zwei andere Flavonoide, die anfangs vielversprechend wirkten, innerhalb der Tasche zu gleiten oder wurden im Verlauf stärker vom Lösungsmittel exponiert—Anzeichen für schwächere, weniger verlässliche Bindung. Als die Forschenden die „freie Energie-Landschaft“ jedes Komplexes kartierten—eine Darstellung, welche Konformationen thermodynamisch bevorzugt sind—fanden sie, dass PSCdb01560 ein tiefes, gut definiertes Energie-Tal einnahm, während die weniger stabilen Verbindungen zwischen mehreren flacheren Becken hin und her sprangen. Verglichen mit den ursprünglich gedockten Posen veränderte PSCdb01560 seine Lage kaum, was seine konformationelle Treue unterstreicht.
Zahlen, die auf Wirkstoff-ähnliche Stärke hindeuten
Schließlich nutzte das Team ein Rahmenwerk zur Energieabschätzung, um zu berechnen, wie stark jedes Flavonoid nach Berücksichtigung aller simulierten Bewegungen binden würde. PSCdb01560 erzielte eine günstigere Bindungsfreier-Energie als die etablierte Referenzverbindung, angetrieben durch eine Kombination aus enger Formkomplementarität, attraktiven elektrostatischen Wechselwirkungen und ölartigen Kontakten innerhalb der Tasche. Dieses Muster—starke berechnete Affinität, stabile Position über die Zeit, geringe interne Flexibilität und Beteiligung entscheidender NS5-Reste, die bei verschiedenen Dengue-Stämmen konserviert sind—zeichnet PSCdb01560 als besonders überzeugenden Ausgangspunkt für Wirkstoffentwicklung aus.
Was das für zukünftige Dengue-Behandlungen bedeuten könnte
Diese Ergebnisse liefern noch keine Tablette gegen Dengue, aber sie verengen die Suche deutlich. Die Arbeit identifiziert ein pflanzlich abgeleitetes Flavonoid-Gerüst, das im Computer mehreren Konkurrenten und sogar einem bekannten Vergleichs-Inhibitor sowohl in Stabilität als auch in vorhergesagter Bindungsstärke überlegen ist. Die nächsten Schritte sind experimentell: prüfen, ob PSCdb01560 NS5 in Reagenzgläsern tatsächlich blockiert, die Dengue-Replikation in infizierten Zellen stoppt und in Tiermodellen sicher ist. Werden diese Hürden genommen, könnten Chemiker dieses Flavonoid zu einem klinisch nutzbaren Virostatikum verfeinern. Vorläufig bietet die Studie eine hoffnungsvolle Botschaft: Die natürliche Chemiebibliothek birgt weiterhin vielversprechende Werkzeuge, um eine der am schnellsten wachsenden von Mücken übertragenen Bedrohungen zu entwaffnen.
Zitation: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Schlüsselwörter: Dengue-Virus, NS5-Polymerase, Flavonoid-Inhibitor, antivirale Wirkstoffforschung, molekulares Docking