Clear Sky Science · de
Neues Faltungsneuronales Netzwerk zur bakteriellen Identifikation in konfokalen Mikroskop-Datensätzen
Warum schnelleres Erkennen von Keimen zählt
Wenn Ärzte herausfinden müssen, welcher Bakterienstamm eine Infektion verursacht, ist Zeit ein kritischer Faktor. Traditionelle Laboruntersuchungen können viele Stunden oder sogar Tage dauern und erfordern erfahrene Fachleute, die Mikroskopbilder visuell auswerten. Diese Studie stellt ein neues Computer-Vision-System namens CM-Net vor, das spezialisierte Mikroskopbilder automatisch auslesen und schnell zwei häufige, medizinisch relevante Bakterien unterscheiden kann, während es zugleich erkennt, welche Zellen lebendig oder tot sind. Die Arbeit weist auf einen Weg zu schnelleren, zuverlässigeren Diagnosen hin, die eines Tages in Krankenhäusern und Forschungslabors weltweit eingesetzt werden könnten.
Leuchtende Keime in nützliche Bilder verwandeln
Die Forscher begannen mit einem leistungsfähigen Bildgebungsinstrument, der konfokalen Laserscanningmikroskopie. Einfach ausgedrückt nutzt dieses Mikroskop einen fokussierten Laser und fluoreszierende Farbstoffe, damit Bakterien je nach Lebenszustand in unterschiedlichen Farben leuchten. Lebende Zellen erscheinen grün, tote Zellen rot. Durch Abtasten der Probe in sehr dünnen Schichten erzeugt das Mikroskop scharfe, detaillierte Aufnahmen der Bakterien auf Objektträgern. Das Team arbeitete mit zwei gut bekannten Arten, die häufig Krankenhausinfektionen verursachen: dem stäbchenförmigen Escherichia coli und dem kugeligen Staphylococcus aureus. Diese hochwertigen Bilder bilden das Rohmaterial, das CM-Net erlernen muss.
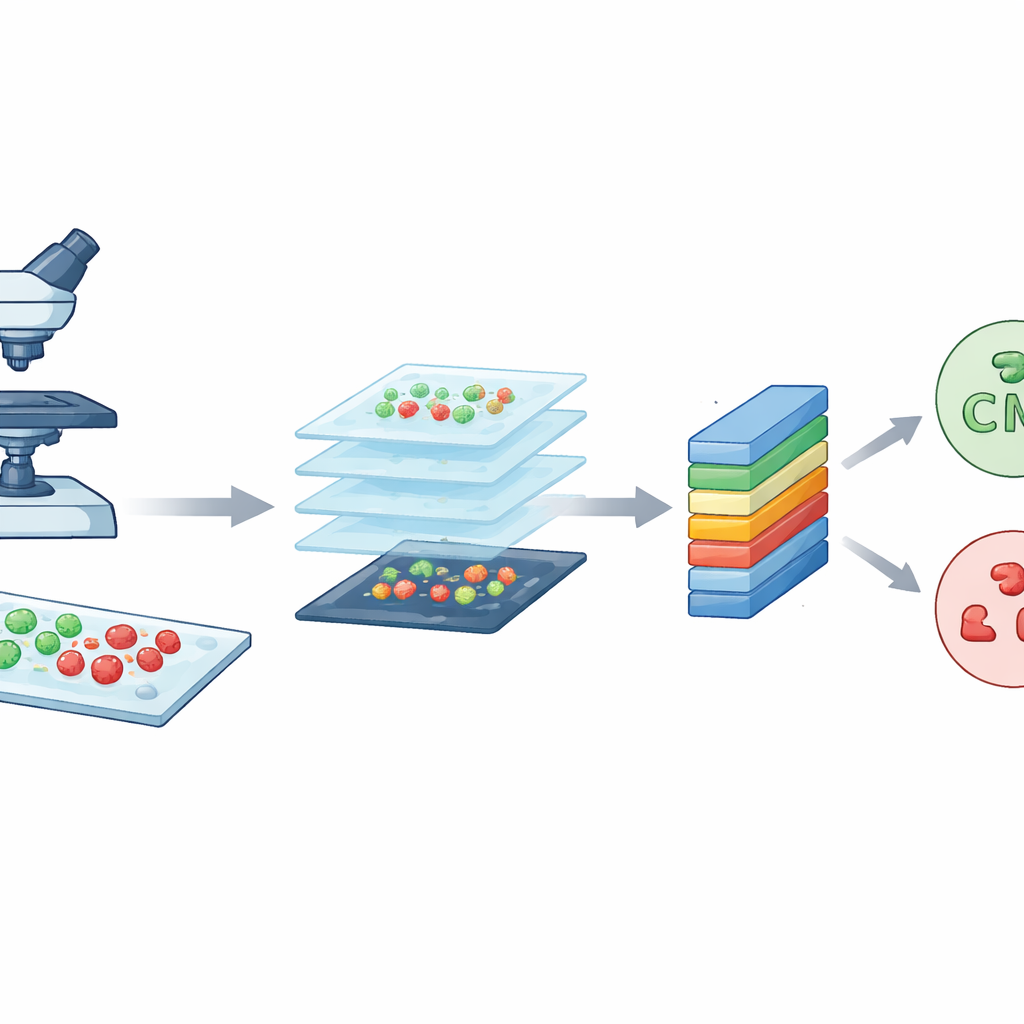
Viele kleine Kacheln aus großen Bildern machen
Obwohl jedes konfokale Bild viele Details enthält, ist es auch sehr groß, ungefähr 3000 mal 3000 Pixel. Ein Modell direkt auf solch riesigen Bildern zu trainieren wäre langsam und würde übermäßige Rechenressourcen verlangen. Zur Lösung schnitt das Team jedes große Bild in viele kleinere quadratische Kacheln von jeweils 224 mal 224 Pixeln, eine Standardgröße in der Bildanalyse. Dieser Prozess, eine Form der Datenaugmentation, reduziert die technische Last und vervielfacht zugleich die Anzahl der Trainingsbeispiele. Aus einem ursprünglichen Satz von 300 Bildern pro Bakterientyp erzeugten sie insgesamt 7.066 Kacheln. Diese Kacheln erfassen lokale Muster in Form, Farbe und Textur aus verschiedenen Bereichen der Objektträger und liefern dem Modell eine vielfältige und ausgewogene Menge an Beispielen zum Lernen.
Wie der digitale Beobachter zu sehen lernt
CM-Net ist ein speziell für die bakterielle Mikroskopie entwickeltes Deep-Learning-Modell, nicht bloß eine Anpassung von Modellen für allgemeine Fotodatenbanken. Es ist eine Form eines Faltungsneuronalen Netzwerks, einer Klasse von Programmen, die besonders gut darin sind, Muster in Bildern zu finden. CM-Net verarbeitet jede Kachel durch eine Reihe von Stufen. Frühe Stufen suchen nach einfachen visuellen Hinweisen wie Kanten und Flecken; tiefere Stufen kombinieren diese zu komplexeren Mustern, die Stäbchen von Kugeln und lebende von toten Zellen unterscheiden. Das Netzwerk verwendet Techniken wie Batch-Normalisierung, die seine internen Signale stabil halten, und eine gekappte Form seiner Aktivierungsfunktion, die extreme Reaktionen verhindert, die das Lernen destabilisieren könnten. Spätere Schichten verdichten die extrahierten Informationen und treffen eine abschließende Entscheidung über Bakterientyp und Zellzustand.
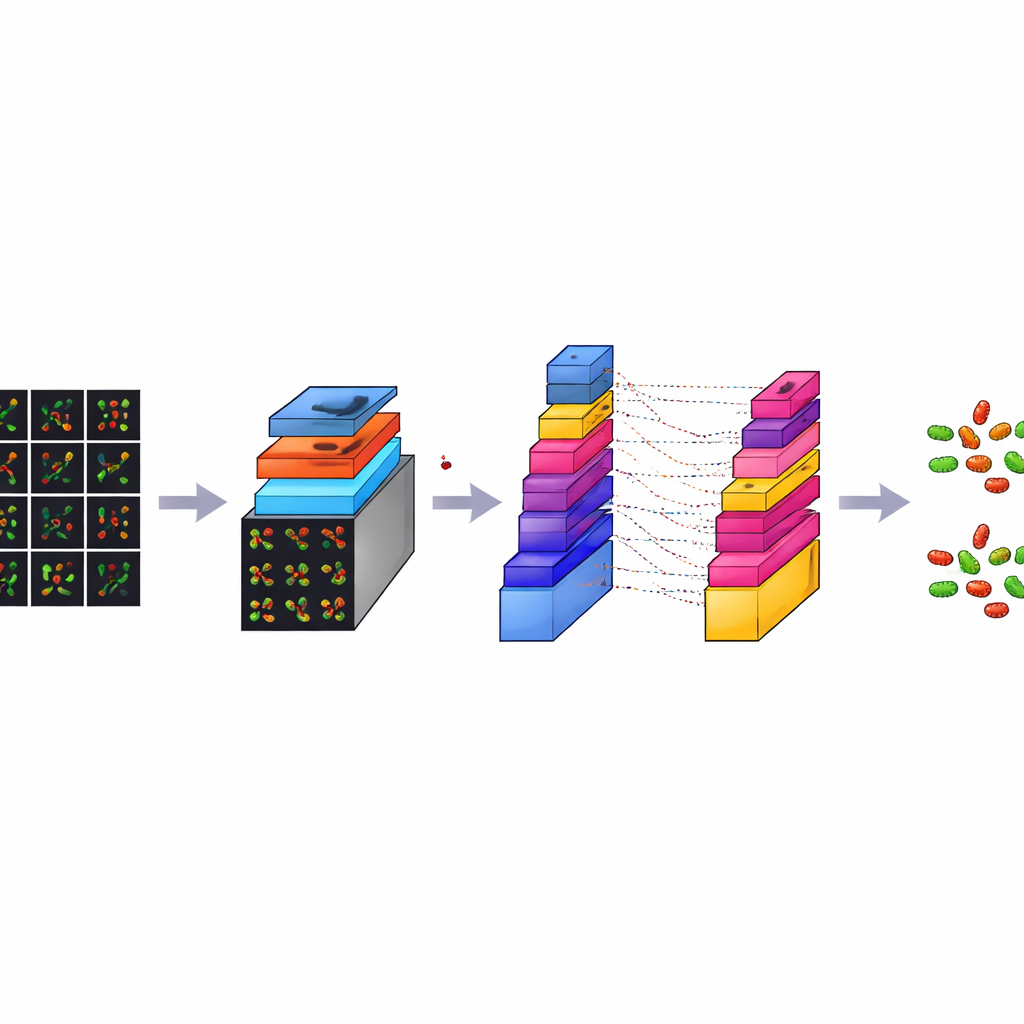
Bessere Leistung als gängige Standardmodelle
Um die Leistungsfähigkeit von CM-Net zu prüfen, trainierten und testeten die Autoren das Modell 30-mal, jeweils mit einer neuen Aufteilung der Daten in Trainings- und Testgruppen. Sie maßen Accuracy, wie oft das Modell insgesamt korrekt lag; Sensitivität, wie gut es die Zielklassen erkannte; Spezifität, wie gut es Fehlalarme vermied; sowie mehrere andere Standardmetriken. CM-Net erreichte im Mittel etwa 96% Accuracy, mit Sensitivität und Spezifität ebenfalls um 96% und einer starken Ausgewogenheit zwischen den beiden Klassen. Es benötigte außerdem weniger interne Parameter und weniger Speicher als mehrere weit verbreitete, vortrainierte Modelle — darunter GoogLeNet, MobileNetV2, ResNet18 und ShuffleNet — blieb dabei aber schneller in der Ausführung. Visualisierungswerkzeuge zeigten, dass CM-Net seine Aufmerksamkeit auf die tatsächlichen bakteriellen Körper in den Bildern richtet und nicht auf zufällige Hintergrundmerkmale, was die Annahme stützt, dass es biologisch sinnvolle Hinweise erlernt.
Was das für zukünftige Laborarbeit bedeutet
Alltäglich ausgedrückt zeigt die Studie, dass ein zweckmäßig entwickeltes Deep-Learning-System komplexe Mikroskopbilder von Bakterien genau, effizient und in einer Weise „lesen“ kann, die mit den Anforderungen menschlicher Expertinnen und Experten übereinstimmt. Momentan wurde CM-Net nur für zwei Bakterienspezies und mit Daten eines einzigen Mikroskoptyps trainiert, sodass weitere Arbeit nötig ist, bevor es als allgemeines Diagnostikwerkzeug einsetzbar ist. Die Autorinnen und Autoren planen, das Modell auf mehr Arten, verschiedene Zellzustände und größere, vielfältigere Datensätze auszuweiten. Dennoch deuten die Ergebnisse darauf hin, dass Systeme wie CM-Net Laboren künftig helfen könnten, Infektionen schneller zu identifizieren, Behandlungsentscheidungen zu unterstützen und die automatisierte Analyse mikrobiologischer Experimente für Anwender ohne spezialisierte Bildgebungsexpertise zu öffnen.
Zitation: Al-Jumaili, A., Al-Jumaili, S., Alyassri, S. et al. Novel convolutional neural network for bacterial identification of confocal microscopic datasets. Sci Rep 16, 8123 (2026). https://doi.org/10.1038/s41598-026-38861-5
Schlüsselwörter: Klassifizierung bakterieller Bilder, Konfokale Mikroskopie, Tiefes Lernen, Faltungsneuronale Netzwerke, Medizinische Diagnostik