Clear Sky Science · de
Bestimmung des Herzzeitvolumens, des Shunt-Anteils und des aktiven Kreislaufvolumens bei Kindern mit hypoplastischem Linksherzsyndrom nach dem Norwood-Verfahren mit RV‑zu‑PA‑Shunt.
Ein zerbrechliches Neugeborenenherz im Gleichgewicht halten
Bei Säuglingen mit hypoplastischem Linksherzsyndrom ist die Hauptkammer, die das Blut in den Körper pumpen sollte, stark unterentwickelt. Chirurgen können den Kreislauf beim ersten Eingriff – dem Norwood‑Verfahren – umbauen, doch die Tage nach der Operation sind ein Balanceakt: Ärztinnen und Ärzte müssen eine einzelne funktionierende Kammer sowohl für Lunge als auch für den Körper aufteilen. Diese Studie untersucht, wie unterschiedliche Sauerstoffgehalte im Atemgas dieses empfindliche Gleichgewicht beeinflussen und was tatsächlich steuert, wohin das Blut fließt.
Eine Pumpe mit Doppelaufgabe
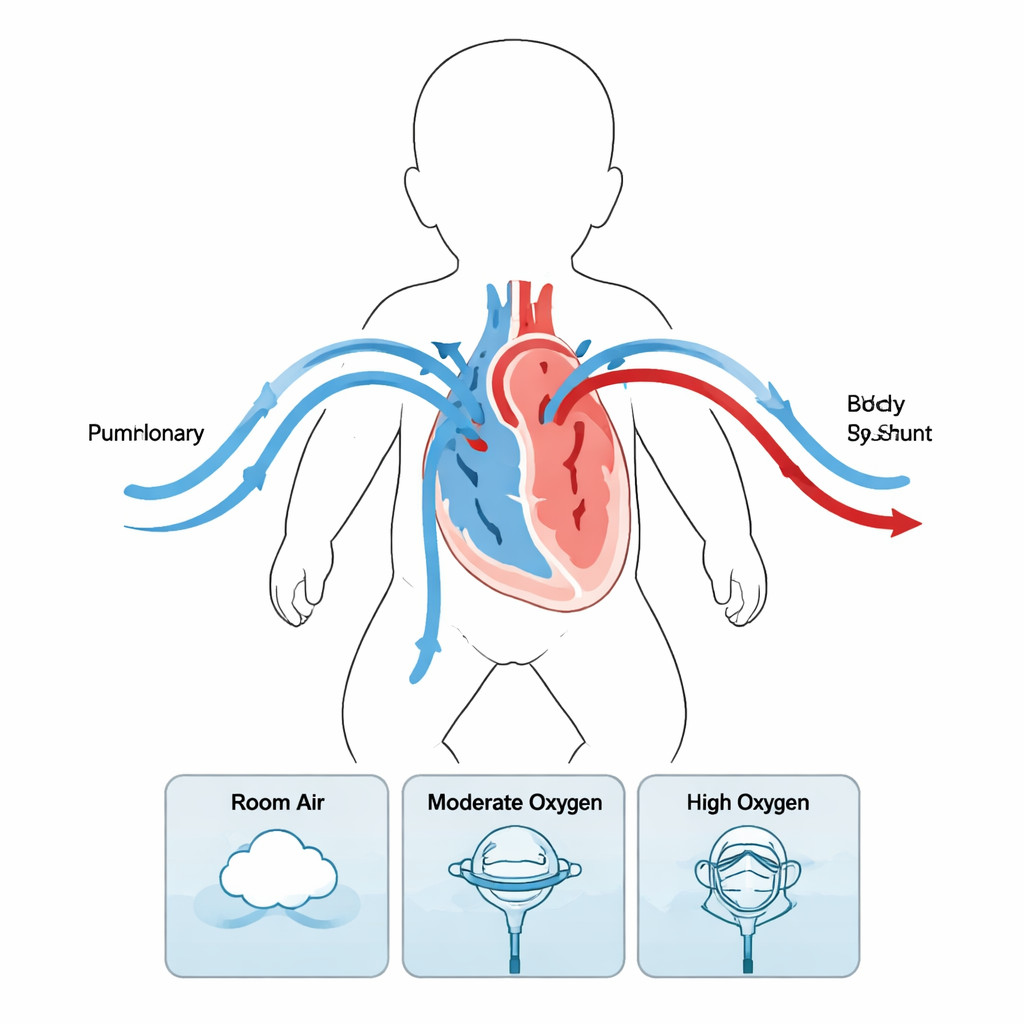
Im normalen Herzen pumpt eine Kammer in die Lunge und die andere in den Körper. Bei diesen Neugeborenen muss eine Kammer beide Aufgaben übernehmen. Beim Norwood‑Verfahren schaffen Chirurgen einen neuen Weg vom Herzen zum Körper und verbinden den rechten Ventrikel über ein kleines Röhrchen, einen Shunt, mit den Lungenarterien. Das Blut teilt sich daher: Ein Teil fließt durch den Shunt in die Lunge (pulmonaler Fluss, Qp), ein anderer Teil in den Körper (systemischer Fluss, Qs). Ein ausgewogenes Verhältnis von Qp zu Qs ist entscheidend. Zu viel Blut in der Lunge beraubt den Körper sauerstoffreichem Blut; zu wenig gefährdet die Sauerstoffaufnahme in der Lunge.
Eine neue Methode, winzige Herzen zu messen
Standard-Bettzeichen wie Blutdruck und Sauerstoffwerte liefern nur ein grobes Bild des Kreislaufs bei diesen fragilen Säuglingen. Die direkte Messung von Sauerstoffverbrauch und Blutfluss, die für klassische Berechnungen nötig ist, ist bei kleinen, kritisch kranken Babys besonders schwierig und fehleranfällig. Die Forschenden verwendeten stattdessen eine Ultraschalldilutionsmethode. Sie injizierten kurz warmes Kochsalz über eine venöse Leitung und maßen winzige Veränderungen, wie sich der Schall im Blut ausbreitet, während es durch eine extrakorporale Schleife läuft. Aus der Form der resultierenden Kurven konnte spezialisierte Software das gesamte Herzzeitvolumen, den Anteil des Bluts, der in die Lunge versus in den Körper gelangte, und das aktuell aktiv zirkulierende Blutvolumen schätzen.
Mehr Sauerstoff: Was sich wirklich ändert
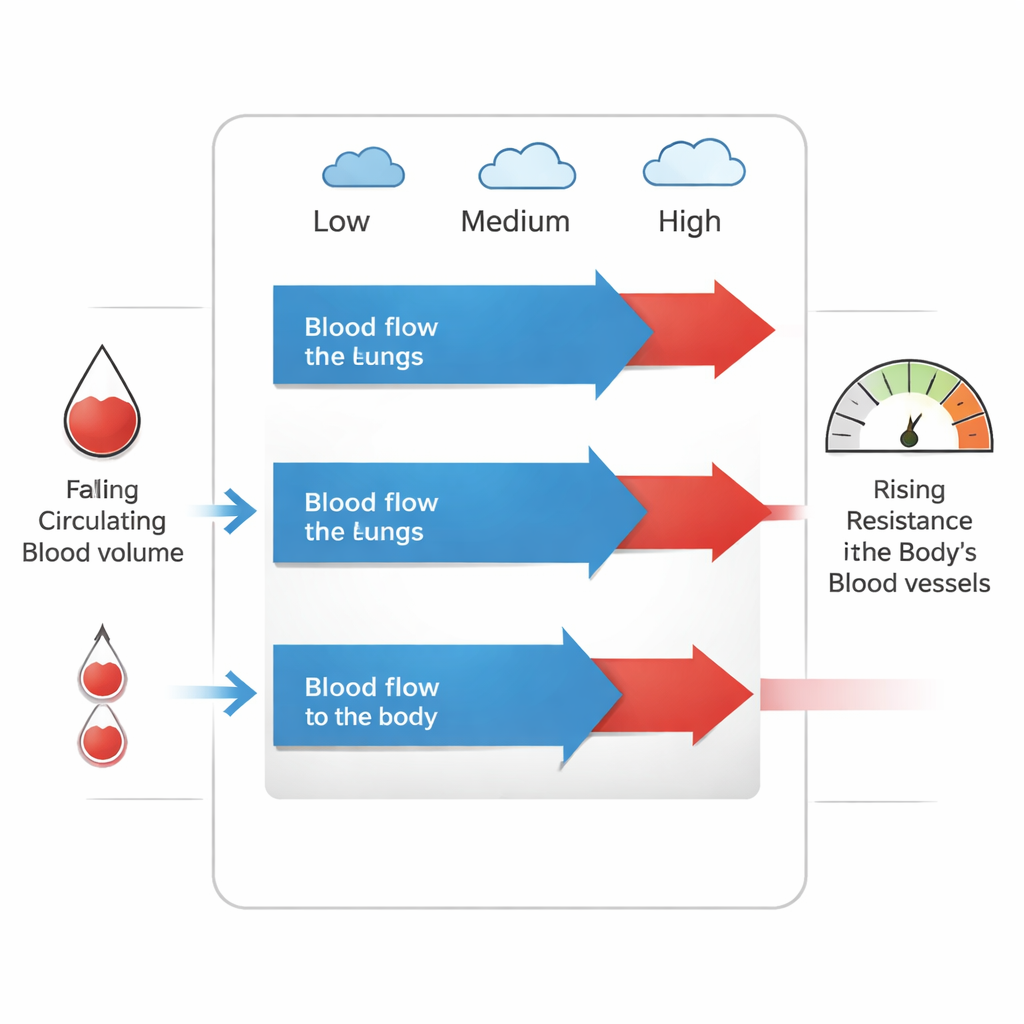
Sechzehn Neugeborene wurden kurz nach ihren Norwood‑Operationen untersucht, während sie leicht sediert und beatmet waren. Das Team maß Fluss und Drücke bei drei Sauerstoffstufen im Atemgas: etwa Raumluft, mäßig erhöhte Sauerstoffzufuhr und sehr hoher Sauerstoffanteil. Mit zunehmendem Sauerstoff blieb der Lungenfluss praktisch unverändert, während der Körperfluss sank. Da der Lungenfluss stabil blieb und der Körperfluss abnahm, stieg das berechnete Verhältnis von Lunge zu Körper (Qp/Qs). Die treibenden Drücke für den Blutfluss durch die Lunge und der Gesamtwiderstand im Lungenkreislauf änderten sich jedoch nicht in nennenswertem Maße. Stattdessen verengten sich die Gefäße im Körper, wodurch der systemische Gefäßwiderstand anstieg, und das effektive zirkulierende Blutvolumen – das bereits im Vergleich zu Kindern mit zwei funktionierenden Kammern niedrig war – nahm weiter ab.
Warum ein festes Röhrchen wichtiger ist als Sauerstoff
Diese Muster deuten darauf hin, dass früh nach der Operation der starre Shunt vom Ventrikel zu den Lungenarterien als das hauptsächliche "Ventil" wirkt, das den Lungenfluss kontrolliert. Da der Shunt wie ein festes mechanisches Nadelöhr funktioniert, hat zusätzlicher Sauerstoff – normalerweise ein starker Vasodilatator in der Lunge – nur begrenzte Möglichkeiten, den Lungenfluss zu erhöhen. Stattdessen scheint höherer Sauerstoff die Gefäße des Körpers zu verengen, die Herzfrequenz leicht zu senken und die relative Knappheit an zirkulierendem Blut zu verschlechtern. Das Ergebnis ist, dass weniger Blut lebenswichtige Organe erreicht, selbst wenn die Sauerstoffwerte in Arterien und Venen steigen, weil der Gasaustausch in der Lunge verbessert wird. Kleine Verschiebungen des Blutvolumens, etwa bei Infektion oder Entzündung, können das Gleichgewicht weiter zugunsten der Lunge und zulasten des Körpers verschieben.
Was das für die Behandlung dieser Neugeborenen bedeutet
Für die Klinik legt die Studie nahe, dass einfaches Erhöhen des Sauerstoffs oder der Einsatz von Medikamenten, die die Gefäße der Lunge erweitern, möglicherweise nicht der effektivste Weg sind, diese Babys zu schützen. Da der Lungenfluss weitgehend durch Größe und Steifigkeit des Shunts bestimmt wird, sind eine sorgfältige chirurgische Wahl der Shunt‑Größe und postoperative Strategien, die das zirkulierende Blutvolumen erhöhen und den Widerstand in den Körpergefäßen behutsam senken, möglicherweise wichtiger, um die Organe ausreichend zu versorgen. Einfach ausgedrückt sprechen die Befunde dafür, die Körperseite des Kreislaufs zu unterstützen – wie viel Blut sie erhält und wie stark das Herz dagegen anpumpen muss – statt zu versuchen, den Lungenfluss allein mit Sauerstoff in den kritischen Tagen nach dem Norwood‑Eingriff feinzujustieren.
Zitation: Aronsson, A., Sigurdsson, T.S. & Lindberg, L. Determination of cardiac output, shunt-fraction, and active circulatory volume in children with hypoplastic left heart syndrome after the Norwood procedure with RV to PA-shunt.. Sci Rep 16, 4748 (2026). https://doi.org/10.1038/s41598-026-38858-0
Schlüsselwörter: hypoplastisches Linksherzsyndrom, Norwood‑Verfahren, Ein-Kammer-Herz, neonatale Hämodynamik, Sauerstofftherapie