Clear Sky Science · de
Kadmium löst Ferroptose in Maus-Spermatocyten über Aktivierung des ROS–TCA-Wegs aus
Warum ein weit verbreitetes Metall für die Männergesundheit wichtig ist
Kadmium ist ein weiches Metall, das in Batterien, Pigmenten und anderen industriellen Produkten verwendet wird. Es kann sich in Boden, Wasser und Lebensmitteln anreichern und gelangt über die Zeit unbemerkt in unseren Körper. Zahlreiche Studien haben Kadmiumexposition mit geringeren Spermienzahlen und schlechterer Spermienqualität bei Männern in Verbindung gebracht, doch der genaue Mechanismus, wie es die Zellen, die Spermien bilden, schädigt, war bislang unklar. Diese Studie geht dem Problem gezielt nach und zeigt, wie Kadmium Maus-Spermatocyten auf einen bestimmten Zelltodpfad treibt, der mit Eisen und einem gestörten Energiesystem in den Mitochondrien, den Kraftwerken der Zelle, verknüpft ist.
Von Umweltverschmutzung zu verletzlichen Spermienzellen
Kadmium ist ein bekannter Umweltstörer für das männliche Fortpflanzungssystem. Männer, die beruflich exponiert sind oder in belasteten Regionen leben, zeigen häufig verringerte Spermienzahl, eingeschränkte Beweglichkeit, abweichende Form und sogar DNA-Schäden in den Spermien. Tierstudien bestätigen diese Befunde und berichten über verkleinerte Hoden, undichte Schutzbarrieren, niedrige Testosteronwerte und weitreichenden Verlust von Keimzellen. Die Autoren hatten zuvor beobachtet, dass Kadmium in Hoden Gewebe eine ungewöhnliche, eisenabhängige Form des Zelltods auslösen kann, die Ferroptose genannt wird. In der vorliegenden Arbeit konzentrierten sie sich auf Maus-Spermatocyten – Zellen, die sich mitten in der Umwandlung zu Spermien befinden –, um genau zu untersuchen, wie Kadmium ihnen schadet und ob dieser eisenverknüpfte Todesweg beteiligt ist.
Eisenüberladung und eine besondere Art des Zelltods
Um das zu untersuchen, kultivierte das Team eine Maus-Spermatocyten-Zelllinie in vitro und setzte die Zellen Kadmium aus, teils mit und teils ohne Substanzen, die bekanntlich Ferroptose blockieren. Kadmium verringerte die Zellvitalität etwa um die Hälfte und verlangsamte die Zellteilung. Intrazellulär stiegen die Werte für freies Eisen und ein Marker für Lipid‑Schäden, Malondialdehyd, deutlich an, während ein wichtiges Schutzenzym, GPX4, abnahm. Andere Proteine, die an Eisenspeicherung und -export beteiligt sind, nahmen zu, was auf eine schwere Störung der Eisenhandhabung hindeutet. Wenn die Forschenden Ferroptosehemmer hinzufügten – eine Eisenchelatorverbindung und ein lipidschutzwirksames Molekül – milderten sich viele dieser schädlichen Veränderungen und die Zellüberlebensrate verbesserte sich. Zusammengenommen entsprechen diese Veränderungen dem Signaturbild der Ferroptose und deuten darauf hin, dass Kadmium die Zellen nicht unspezifisch tötet, sondern sie gezielt in dieses eisen- und lipidgetriebene Todesprogramm treibt.
Mitochondrien unter Beschuss
Die Geschichte vertiefte sich, als die Wissenschaftler ihre Aufmerksamkeit auf die Mitochondrien richteten, die Energiezentren, die auch reaktive Sauerstoffspezies (ROS) als Nebenprodukte erzeugen. Unter dem Mikroskop zeigten gesunde Spermatocyten lange, fadenförmige Mitochondrien, während kadmiumexponierte Zellen kurze, fragmentierte Mitochondrien aufwiesen – ein Zeichen struktureller Schäden. Messungen bestätigten, dass mitochondriale ROS anstiegen, während das elektrische Membranpotenzial der Mitochondrien – ein wichtiger Funktionsindikator – abnahm. Die Zellen reagierten, indem sie ihre internen Abwehrsysteme hochfuhren, einschließlich Proteinen, die vom Stresssensor Nrf2 reguliert werden, doch diese Abwehr reichte nicht aus. Wichtig ist, dass die Ferroptoseblocker die mitochondrialen ROS reduzierten und die mitochondriale Gesundheit teilweise wiederherstellten, womit die beschädigten Kraftwerke direkt mit dem eisenabhängigen Todesweg verknüpft wurden.
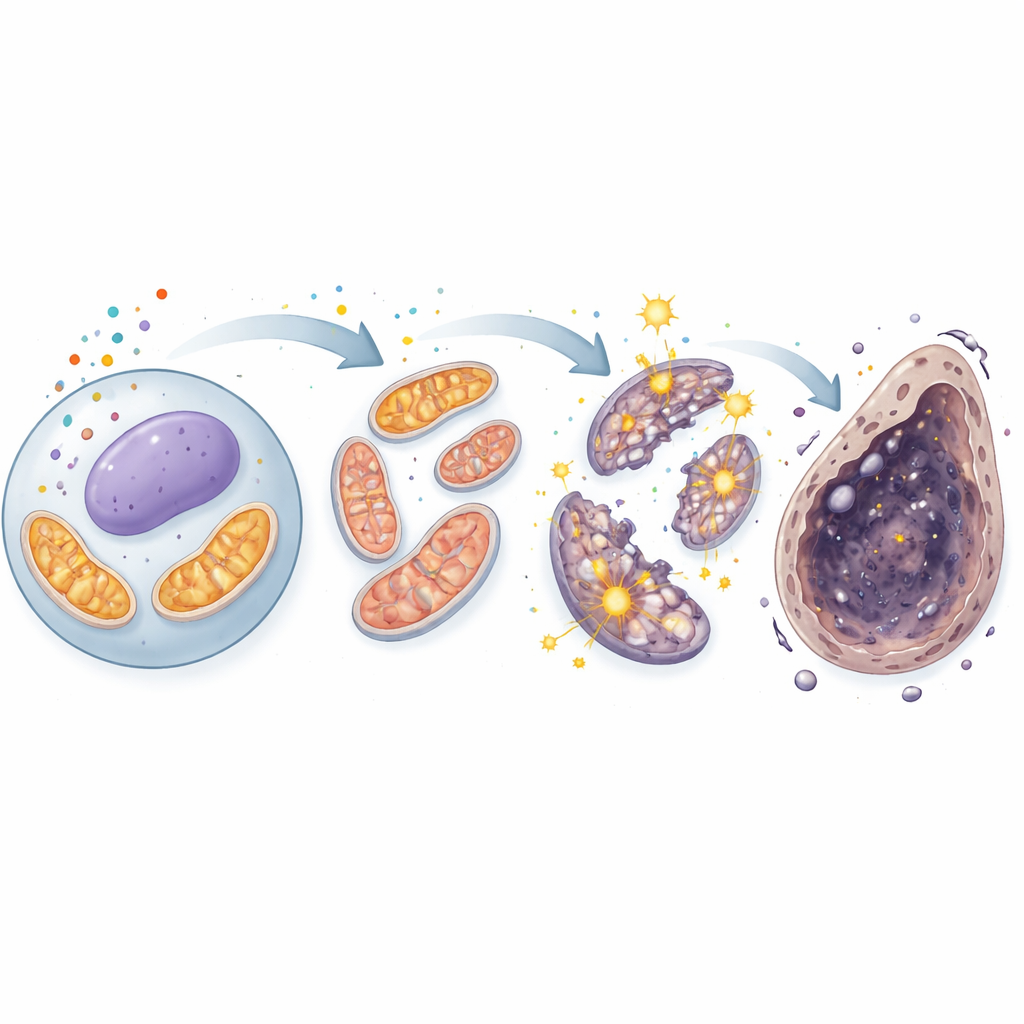
Ein Teufelskreis im Kraftwerk der Zelle
Mithilfe einer Kombination aus Genexpressionsprofiling und Metabolitmessungen stellten die Forschenden fest, dass Kadmium mehr bewirkte, als nur Mitochondrien zu schädigen – es schien deren zentralen Energiekreislauf, den Tricarbonsäure-(TCA-)Zyklus, zu kapern. Die Konzentrationen zweier zentraler TCA-Intermediäre, Alpha‑Ketoglutarat und Succinat, stiegen signifikant, und die Aktivität der Pyruvatcarboxylase, eines Enzyms, das frischen Brennstoff in den Zyklus einspeist, nahm zu. Das deutet darauf hin, dass der TCA‑Zyklus in den geschädigten Zellen paradox überaktiv wurde, mehr Elektronen durch die Atmungskette zwang und dadurch vermehrt ROS austraten. Diese zusätzlichen ROS wirkten dann auf die Eisenchemie und membranbedingte Schäden zurück und verstärkten die Ferroptose. Auch hier bremsten Ferroptosehemmer diese metabolischen Verzerrungen, was die enge Verbindung zwischen Kadmium, mitochondrialer Übersteuerung und eisenabhängigem Zelltod unterstreicht.
Was das für Fruchtbarkeit und zukünftige Forschung bedeutet
Einfach gesagt zeigt die Studie, dass Kadmium Spermatocyten angreift, indem es ihre Mitochondrien direkt schädigt und ihren Energiesystem in schädliche Überaktivität versetzt. Diese Kombination überflutet die Zellen mit reaktiven Sauerstoffmolekülen und stört das Eisen-Gleichgewicht, sodass sie in die Ferroptose gedrängt werden. Da Spermatocyten für die Produktion gesunder Spermien unerlässlich sind, kann ihr Verlust erklären, warum Kadmiumexposition so stark mit verringerter männlicher Fruchtbarkeit assoziiert ist. Zwar wurden diese Experimente an Maus-Zellen in Zellkultur durchgeführt, doch liefern sie eine klare mechanistische Karte, die künftige Tier- und Humanstudien überprüfen können. Die Arbeit hebt auch potenzielle Schutzstrategien hervor: Medikamente oder Nährstoffe, die mitochondrialen Stress dämpfen, den TCA‑Zyklus feinjustieren oder eisenbedingte Membranschäden verhindern, könnten helfen, das männliche Fortpflanzungssystem vor Umweltmetallen wie Kadmium zu schützen.
Zitation: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Schlüsselwörter: Kadmiumtoxizität, männliche Fruchtbarkeit, mitochondrialer Stress, Ferroptose, reaktive Sauerstoffspezies