Clear Sky Science · de
Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin
Warum hitzeliebende Viren für künftige Antibiotika wichtig sind
Mit dem Anstieg der Antibiotikaresistenz suchen Forschende eilig nach neuen Wegen, gefährliche Bakterien zu bekämpfen. Ein vielversprechender Ansatz bedient sich der Waffen von Viren, die Bakterien infizieren — sogenannte Bakteriophagen. Diese Viren produzieren Enzyme, Endolysine genannt, die Löcher in bakterielle Zellwände schlagen. Die hier behandelte Studie konzentriert sich auf ein bemerkenswert hitzebeständiges Endolysin, Ts2631, aus einem Virus, das in isländischen heißen Quellen lebt. Indem sie herausfinden, welche einzelnen Bausteine dieses Proteins seine Stabilität bei nahezu siedetemperaturen sichern, hoffen die Forschenden, widerstandsfähigere, langlebigere antibakterielle Enzyme für Medizin und Biotechnologie zu entwerfen. 
Ein virales Werkzeug geschmiedet in kochenden Quellen
Ts2631 stammt von einem Bakteriophagen, der das hitzetolerante Bakterium Thermus scotoductus infiziert, das in Gewässern gedeiht, die weit über 60 °C erreichen. Das Enzym Ts2631 schneidet eine spezifische Bindung im Peptidoglycan, dem robusten Geflecht, das bakterielle Zellen umgibt. Hervorzuheben ist die extreme Thermostabilität von Ts2631: Es bleibt bis etwa 100–105 °C gefaltet, abhängig von der Lösung. Das liegt weit über den Temperaturen, bei denen die meisten Proteine zerfallen. Die Autorinnen und Autoren verglichen Ts2631 mit seinem am besten untersuchten Verwandten aus einem mäßig temperierten Virus, der T7-Lysozym, um herauszufinden, welche strukturellen Tricks die Natur verwendet hat, damit Ts2631 unter so harten Bedingungen intakt bleibt.
Kürzere Schleifen und eine andere Mischung an Bausteinen
Proteine sind Ketten aus 20 Aminosäuretypen, die zu komplexen Formen gefaltet sind. Als die Forschenden die 3D-Strukturen von Ts2631 und dem T7-Lysozym überlagerten, zeigte sich, dass die Gesamtarchitektur sehr ähnlich ist: Beide besitzen einen kompakten Kern aus Helices und Strängen. Der entscheidende Unterschied liegt in den flexiblen Schleifenregionen, die diese Elemente verbinden. Bei Ts2631 sind diese Schleifen kürzer und weniger flexibel, während das T7-Lysozym längere, lockere Schleifen aufweist. Ts2631 enthält außerdem mehr von bestimmten Aminosäuren, die oft mit Hitzebeständigkeit in Verbindung gebracht werden: das starre Prolin; aromatische Reste wie Tyrosin und Tryptophan; sowie positiv geladene Argininreste. Zugleich weist es weniger Serin-, Asparaginsäure- und Glutaminsäurereste auf, die Proteine bei hohen Temperaturen verwundbarer machen können. Dieses Muster gilt nicht nur im Vergleich zum T7-Lysozym, sondern auch, wenn Ts2631 mit Hunderttausenden viraler und vielen Millionen bakterieller Proteine verglichen wird.
Einzelne Aminosäuren austauschen, um ihre Bedeutung zu testen
Um aus Korrelationen Ursache-Wirkungs-Beziehungen zu machen, ersetzte das Team systematisch 55 einzelne Aminosäuren in Ts2631 und maß, wie jede Mutation die Schmelztemperatur (Tm) und die Fähigkeit des Enzyms, bakterielle Zellwände abzubauen, beeinflusste. Einige Veränderungen rund um die zinkhaltige aktive Stelle waren besonders schädlich. Als drei zinkkoordiniertende Rückstände (H30, H131 und C139) verändert wurden, sank die Tm um bis zu etwa 20 °C und die Aktivität ging verloren. Zwei konservierte Tyrosine (Y60 und Y69) trugen ebenfalls zur Stabilität bei. Überraschenderweise erhöhte das Entfernen einer Disulfidbrücke — einer Art kovalenter Verbindung zwischen den Cysteinresten C80 und C90 — tatsächlich die Schmelztemperatur, obwohl dadurch die Aktivität zerstört wurde. Das zeigt, dass hohe Stabilität im Reagenzglas nicht immer bedeutet, dass ein Protein unter realen Bedingungen besser funktioniert. 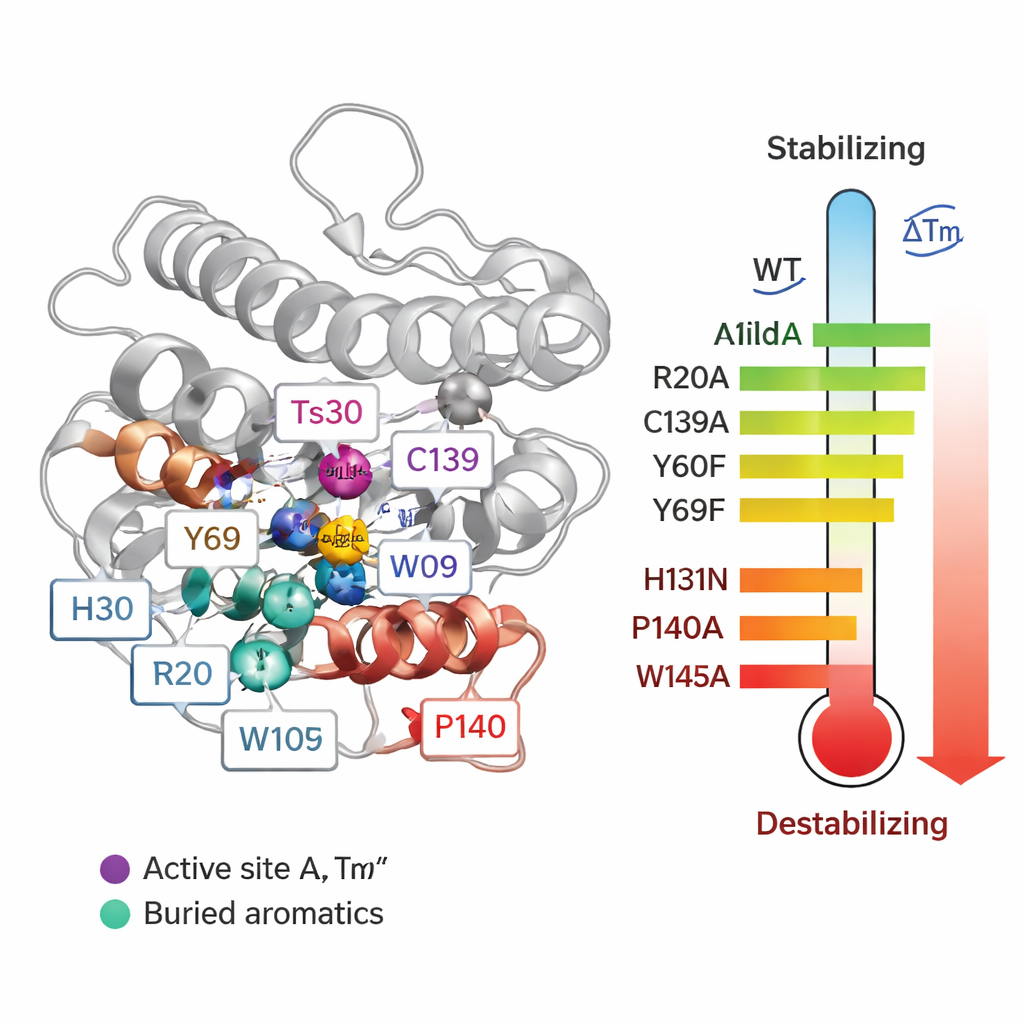
Versteckte aromatische „Anker“ und ein wichtiger Griff an der bakteriellen Wand
Die auffälligsten Ergebnisse ergaben sich aus Mutationen an Prolin- und Tryptophanresten. Die Veränderung eines einzelnen Prolins (P140), das direkt neben dem zinkbindenden C139 liegt, reduzierte die Tm um mehr als 21 °C und schwächte die Aktivität nach Erhitzung, weil die Mutation eine spezielle Bindungsgeometrie störte, die für die richtige Metallbindung nötig ist. Mehrere tief vergrabene Tryptophane (W102, W109 und besonders W145) erwiesen sich ebenfalls als kritisch: Ihr Ersatz durch Alanin verursachte Tm‑Abfälle von 14–24 °C und machte das Enzym in Aktivitätstests viel hitzeempfindlicher. Diese aromatischen Reste wirken wie innere Anker, die den Proteinkern fixieren. Unter den Argininen hatten die meisten nur geringe Auswirkungen auf die Stabilität, doch R20 erwies sich als wesentlich für das Greifen von Peptidoglycan. Beim Austausch von R20 band das Enzym die bakterielle Zellwand schlecht und verlor nach Erhitzung seine Aktivität, was zeigt, dass einige Reste eher zur Funktion als zur reinen thermischen Robustheit beitragen.
Von heißen Quellen zu robusteren Antibakteriellen
In der Summe zeigt die Studie, dass die außergewöhnliche Hitzebeständigkeit von Ts2631 auf einer Handvoll wohlplatzierter Aminosäuren beruht und nicht auf einer gleichmäßigen Verstärkung des gesamten Proteins. Zinkbindende Reste, ein konserviertes Prolin in der Nähe der aktiven Stelle und vergrabene aromatische Seitenketten bilden einen stabilisierenden Kern, während einige klassische Stabilitätsmerkmale, wie Disulfidbrücken oder Salzbrücken, hier weniger Bedeutung haben als erwartet. Für das breitere Feld legt diese Arbeit nahe, dass mesophile (mäßig temperierte) Endolysine durch gezielten Austausch ausgewählter Positionen gegen Tryptophan oder Prolin widerstandsfähiger gemacht werden könnten, ohne die antibakterielle Aktivität zu opfern. Anders gesagt: Indem man lernt, wie die Natur Enzyme baut, die nahezu siedetemperaturen trotzen, erhalten Forschende eine praktische Blaupause, um verlässlichere, langlebigere proteinbasierte Antibiotika zu entwickeln.
Zitation: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Schlüsselwörter: thermostable endolysin, bacteriophage enzymes, protein thermostability, antibiotic resistance, protein engineering