Clear Sky Science · de
Studie zu Biomarkern der von Homocystein ausgelösten Umwandlung von Gefäßglattmuskelzellen in Schaumzellen
Warum verstopfte Arterien mit winzigen Zellveränderungen beginnen
Atherosklerose — die langsame Verstopfung und Verhärtung der Arterien — ist eine führende Ursache für Herzinfarkte und Schlaganfälle. Meist hört man etwas über Cholesterin und Ernährung, seltener darüber, wie sich einzelne Zellen in der Gefäßwand im Verlauf der Krankheit verändern. Diese Studie untersucht einen solchen Auslöser näher: ein Blutmolekül namens Homocystein, und zeigt, wie es normalerweise unauffällige Muskelzellen in Arterien dazu bringen kann, Fett anzusammeln und sich in sogenannte Schaumzellen zu verwandeln, die Bausteine gefährlicher Plaques.
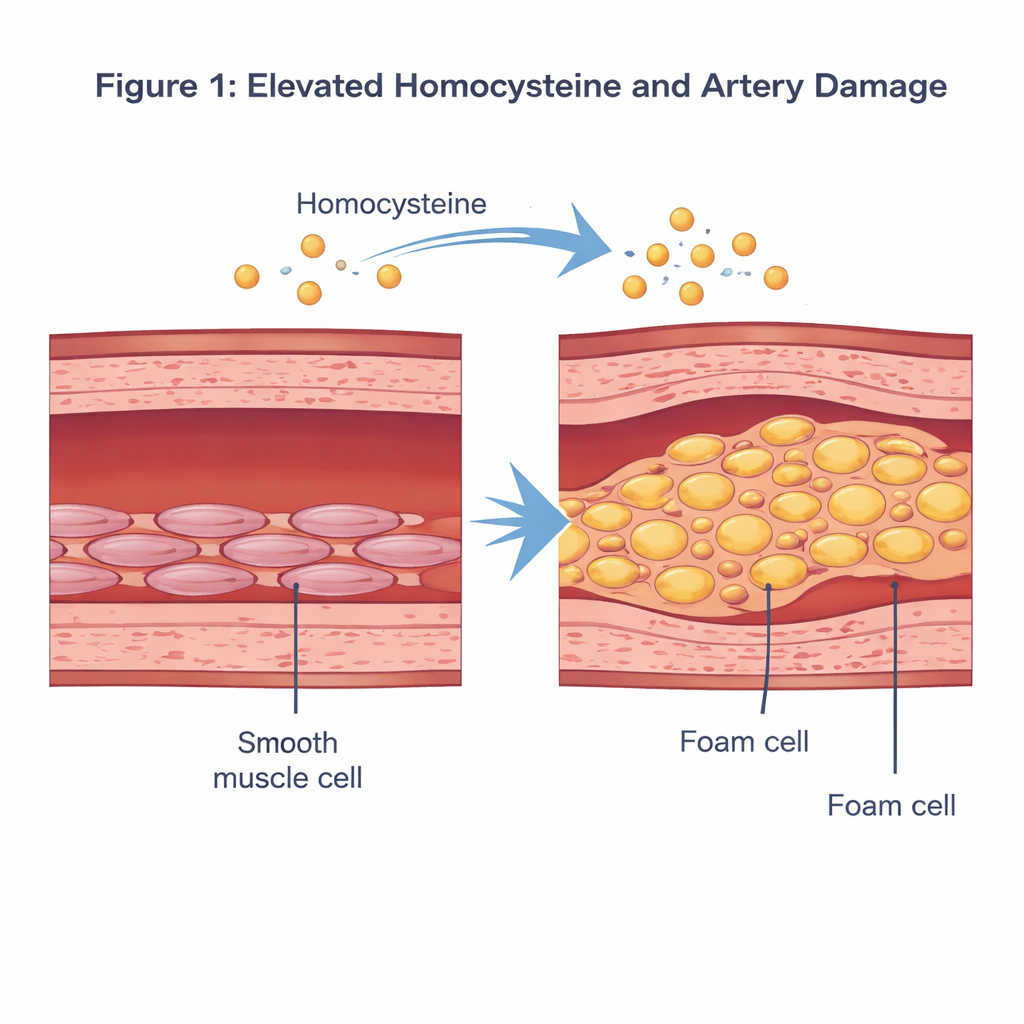
Eine schwefelhaltige Aminosäure im Blut
Homocystein ist eine schwefelhaltige Aminosäure, die beim Abbau der Nährstoffmethionin im Körper entsteht. Unter normalen Verhältnissen ist ihr Blutspiegel gering. Steigt er über etwa 15 Mikromol pro Liter — ein Zustand, der als Hyperhomocysteinämie bezeichnet wird —, haben epidemiologische Studien ein erhöhtes Risiko für Herz-Kreislauf-Erkrankungen festgestellt. Frühere Arbeiten legten nahe, dass überschüssiges Homocystein die innere Gefäßauskleidung schädigen, Entzündungen fördern und das Verhalten von Gefäßglattmuskelzellen verändern kann. Diese Zellen sitzen in der mittleren Schicht der Gefäßwand und regulieren durch Kontraktion und Relaxation den Blutdruck.
Wie Gefäßmuskelzellen zu fettbeladenen Schaumzellen werden
Die Forscher konzentrierten sich darauf, wie Homocystein diese Glattmuskelzellen umformt. Im Labor setzten sie humane Gefäßglattmuskelzellen einer Homocystein‑Dosis aus, die einen krankheitsähnlichen Zustand nachbilden sollte, und verglichen sie mit unbehandelten Zellen. Mit Standardfärbungen und biochemischen Tests beobachteten sie, dass homocysteinbehandelte Zellen sich mit rot gefärbten Fetttropfen füllten und ihre Cholesterin‑ und Triglyzeridwerte stark anstiegen. Gleichzeitig sanken Proteinmarker ihrer üblichen „kontraktilen“ Identität, während Marker eines stärker synthetischen, plaquebildenden Zustands zunahmen. Zusammengenommen zeigen diese Veränderungen, dass Homocystein Glattmuskelzellen von ihrer normalen Rolle weg und in einen schaumzellenähnlichen, fettgeladenen Phänotyp treiben kann, der direkt zur Plaquebildung beiträgt.
Auf der Suche nach molekularen Fingerabdrücken in den Zellen
Um zu verstehen, welche Proteine sich während dieser Transformation verändern, griff das Team auf moderne Proteomik zurück, eine Technologie, die Tausende von Proteinen gleichzeitig messen kann. Sie verglichen die Proteinmengen in homocysteinbehandelten Zellen mit Kontrollen und quantifizierten zuverlässig fast 4.800 Proteine. Davon fielen 54 als signifikant verändert auf: 13 waren erhöht und 41 vermindert. Viele der veränderten Proteine sind an Lipidverarbeitung, Zellüberleben, oxidativem Stress und strukturellem Umbau der Zellen beteiligt. Die Autoren nutzten anschließend Bioinformatik‑Werkzeuge, um diese Proteine in funktionelle Pfade zu gruppieren und ihre Interaktionen zu kartieren, wobei Netzwerke im Zusammenhang mit Cholesterinstoffwechsel und Stressreaktionen in der Gefäßwand hervorgehoben wurden.
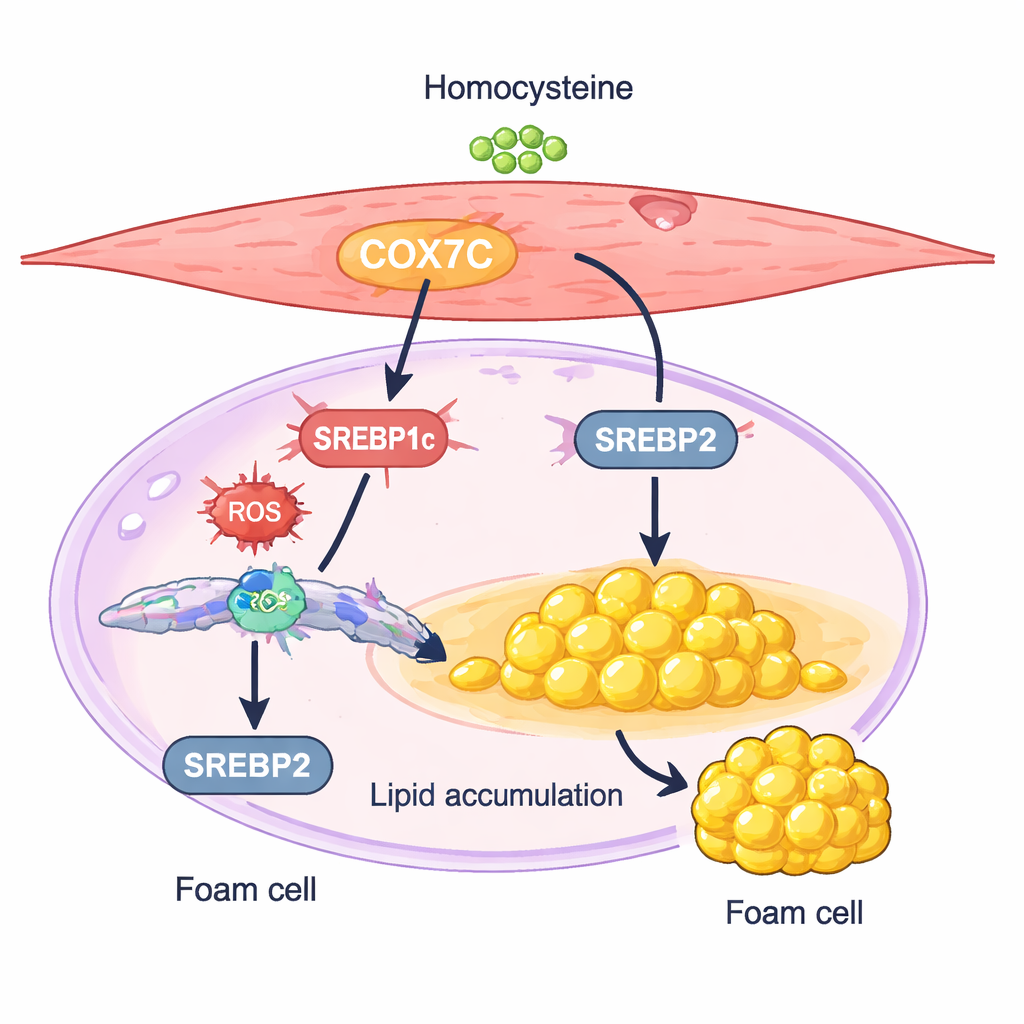
Ein mitochondrialer Schalter, der Zellen zur Fettspeicherung treibt
Ein Protein namens COX7C erwies sich als besonders interessanter Kandidat. COX7C ist Bestandteil der zellulären Kraftwerke, der Mitochondrien, und hilft bei der Steuerung der Energieproduktion. In den homocysteinbehandelten Glattmuskelzellen lagen die COX7C‑Spiegel höher als in den Kontrollen. Die Forscher zeigten, dass eine weitere Erhöhung von COX7C die Zellen noch mehr Fett ansammeln ließ und die Expression zweier Schlüsselfaktoren der Lipidsynthese, SREBP1c und SREBP2, steigerte. Das Stummschalten von COX7C hatte den gegenteiligen Effekt: Es dämpfte die SREBP‑Aktivität, reduzierte Cholesterin‑ und Triglyzeridansammlungen und verringerte die schaumzellenähnlichen Veränderungen. Diese Ergebnisse stützen ein Modell, in dem Homocystein COX7C in den Mitochondrien hochfährt, zelluläre Stresssignale erhöht und dadurch die SREBP‑gesteuerte Fettsynthese aktiviert, wodurch Glattmuskelzellen in einen lipidansammelnden Zustand kippen.
Was das für die Herzgesundheit und zukünftige Therapien bedeutet
Diese Arbeit beweist noch nicht, was genau in menschlichen Arterien passiert, und sie wurde an kultivierten Zellen statt an Patientinnen und Patienten durchgeführt. Trotzdem liefert sie einen detaillierten Einblick, wie erhöhtes Homocystein helfen kann, nützliche Gefäßmuskelzellen in schädliche Schaumzellen zu verwandeln, und identifiziert COX7C und verwandte Proteine als potenzielle Biomarker oder Wirkstoffziele. Für Laien ist die Kernbotschaft: Neben „gutem“ und „schlechtem“ Cholesterin können kleine Verschiebungen in der Blutchemie — etwa ein Überschuss an Homocystein — die Gefäßwand von innen umprogrammieren. Indem molekulare Akteure wie COX7C und der SREBP‑Weg identifiziert werden, legt die Studie das Fundament für künftige Strategien, Plaques zu verhindern, indem arterielle Zellen davon abgehalten werden, zu miniaturisierten Fettspeichern zu werden.
Zitation: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Schlüsselwörter: Atherosklerose, Homocystein, Schaumzellen, Gefäßglattmuskelzellen, COX7C