Clear Sky Science · de
Transkriptionelle Aktivierung von LINGO1 fördert Proliferation und Immunflucht beim kolorektalen Krebs
Warum ein Gehirnprotein im Darmkrebs eine Rolle spielt
Das kolorektale Karzinom gehört zu den weltweit häufigsten und tödlichsten Krebserkrankungen, und viele Patientinnen und Patienten erleiden trotz Operation, Chemotherapie und neuer immunbasierter Medikamente Rückfälle oder entwickeln Metastasen. Diese Studie konzentriert sich auf ein wenig bekanntes Molekül namens LINGO1, das ursprünglich im Gehirn untersucht wurde, und zeigt, dass es Darmtumoren beim Wachsen hilft und ihnen ermöglicht, sich vor den Abwehrkräften des Körpers zu verbergen. Das Verständnis dieses neuen Akteurs könnte die Vorhersage von Krankheitsverläufen verbessern und langfristig den Weg zu präziseren Therapien ebnen.
Ein versteckter Schalter, der in Tumorzellen aufgedreht ist
Die Forschenden fragten zunächst, ob die LINGO1-Spiegel in gesundem und krebsartigem Darmgewebe unterschiedlich sind. Mithilfe großer öffentlicher Gen-Datenbanken und mehrerer unabhängiger Patientengruppen stellten sie fest, dass LINGO1 in kolorektalen Tumoren durchgängig deutlich höher ist als im umliegenden Normalgewebe. Patientinnen und Patienten mit tumoren, die mehr LINGO1 aufwiesen, hatten tendenziell weiter fortgeschrittene Erkrankungen, Befall von Lymphknoten, Fernmetastasen und eine verkürzte Überlebenszeit. Selbst nach Berücksichtigung anderer klinischer Faktoren blieb LINGO1 ein unabhängiges Warnzeichen, was darauf hindeutet, dass es wie ein "Lautstärkeregler" wirkt, der bei höherer Stellung aggressiveren Krebs kennzeichnet.
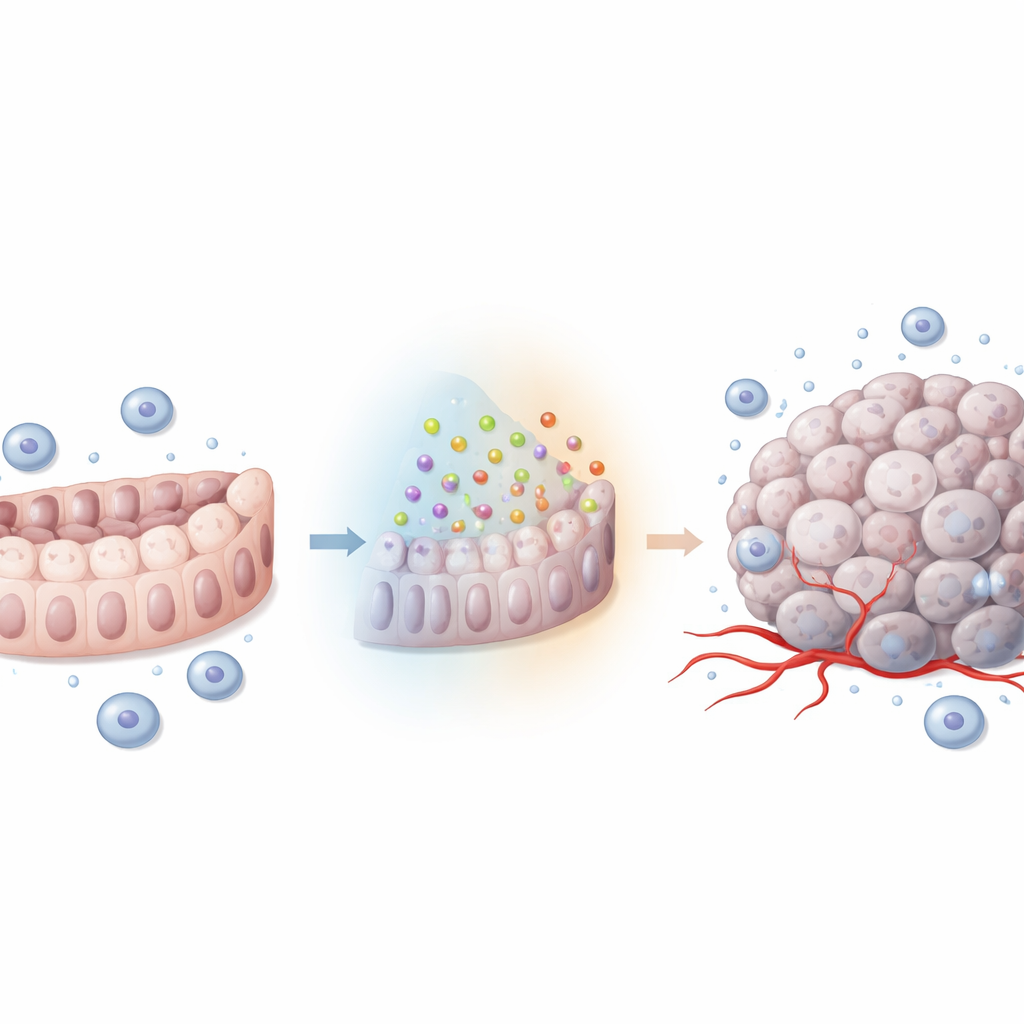
Von Genaktivität zu schnellerem Wachstum und Ausbreitung
Um über statistische Beobachtungen hinauszugehen, prüfte das Team, was passiert, wenn sie LINGO1 in im Labor gezüchteten Darmkrebszellen hoch- oder runterregulieren. Beim Verringern von LINGO1 teilten sich die Tumorzellen langsamer, bildeten weniger Kolonien und konnten weniger gut durch künstliche Membranen wandern, die Gewebebarrieren nachahmen. Sie verloren außerdem die Fähigkeit, das Wachstum und die Bewegung von Gefäßzellen zu fördern, was darauf hindeutet, dass Tumoren mit weniger LINGO1 sich schlechter selbst versorgen können. Wurde LINGO1 in einer anderen Darmkrebszelllinie gesteigert, trat das Gegenteil ein: Wachstum, Bewegung, Invasion und die Fähigkeit, Blutgefäße zu stimulieren, nahmen zu. In Mäusen wuchsen implantierte Tumoren mit ausgeschaltetem LINGO1 langsamer und zeigten weniger Zellen in aktiver Teilung, was dieses Molekül direkt mit Tumorwachstum in lebenden Organismen verbindet.
Wie LINGO1 die Nachbarschaft des Tumors umgestaltet
Die Studie untersuchte auch, welche Gene und Signalwege aktiver sind, wenn LINGO1 hoch ist. Die Muster der Genaktivität wiesen auf bekannte Krebsprogramme hin, darunter solche, die Zell–Zell-Kontakte lösen, damit Zellen migrieren können, sowie solche, die die Bildung neuer Blutgefäße vorantreiben. Ebenso wichtig war die Feststellung, dass hohes LINGO1 mit Veränderungen im umgebenden "Ökosystem" des Tumors verbunden ist. Tumoren mit viel LINGO1 enthielten weniger Killer-T-Zellen—die Immunzellen, die Krebs direkt angreifen können—und mehr Zelltypen, die Immunantworten dämpfen, wie bestimmte Makrophagen und regulatorische T‑Zellen. Viele molekulare "Bremsen", die einen Immunangriff abschalten—häufig als Immun-Checkpoints bezeichnet—waren ebenfalls bei erhöhtem LINGO1 aktiver. Klinische Tumorproben bestätigten, dass Bereiche mit hohem LINGO1 wenige Killer-T-Zellen und schwache Anzeichen zellulärer Abtötungsaktivität aufwiesen, während Bereiche mit niedrigem LINGO1 von aktiven Immunzellen durchsetzt waren.
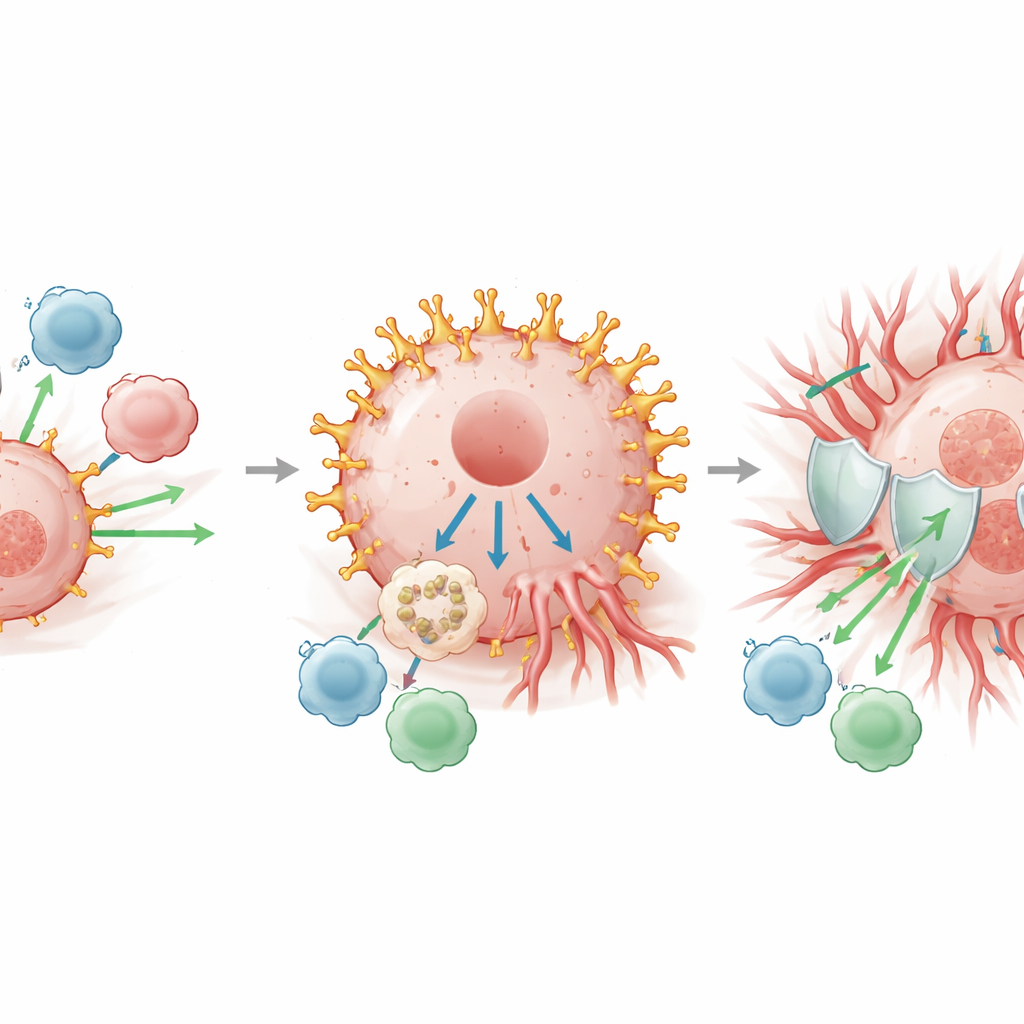
Ein möglicher Kontrollpunkt stromaufwärts
Um zu verstehen, warum LINGO1 in diesen Tumoren so hoch ist, suchten die Autorinnen und Autoren nach upstream-Kontrollproteinen, die wie Ein-/Ausschalter für das LINGO1-Gen wirken könnten. Sie identifizierten einen Faktor namens USF1, der direkt an die Kontrollregion von LINGO1 binden kann. In Reporterexperimenten erhöhte zusätzliches USF1 die Aktivität dieser Region deutlich, allerdings nur, wenn seine Andockstelle intakt war. Das legt nahe, dass in zumindest einigen kolorektalen Karzinomen USF1 dazu beiträgt, LINGO1 hochzufahren, was wiederum schnelleres Tumorwachstum und ein feindlicheres Umfeld für Immunzellen fördert. Die Arbeit zeigte außerdem, dass LINGO1 in mehreren anderen Krebsarten abnormal hoch ist und häufig mit schlechteren Prognosen verknüpft ist, was andeutet, dass sein Einfluss über den Darm hinausreichen könnte.
Was das für Patientinnen, Patienten und künftige Behandlungen bedeutet
Insgesamt zeichnet die Studie LINGO1 als doppelt wirkenden Beitrag zum kolorektalen Krebs: Es treibt Tumorzellen an zu wachsen, sich zu bewegen und neue Blutgefäße zu fördern, während es gleichzeitig dem Tumor hilft, sich gegen eine Immunattacke abzuschotten. Da seine Spiegel fortgeschrittene Erkrankung und schlechteres Überleben vorhersagen, könnte LINGO1 als Biomarker dienen, um Hochrisikopatienten zu identifizieren. Langfristig könnten Medikamente, die LINGO1-Aktivität senken—oder seine Steuerung durch USF1 stören—nicht nur das Tumorwachstum verlangsamen, sondern die Tumore auch für das Immunsystem sichtbarer machen und die Ansprechbarkeit auf Immuntherapien verbessern.
Zitation: Ma, P., Yao, F., Yue, P. et al. Transcriptional activation of LINGO1 facilitates proliferation and immune escape in colorectal cancer. Sci Rep 16, 9360 (2026). https://doi.org/10.1038/s41598-026-38760-9
Schlüsselwörter: kolorektales Karzinom, Tumorimmunität, Biomarker, Tumormikroumgebung, Krebsprogression