Clear Sky Science · de
Hemmung von Immun-Checkpoints erhöht antigenspezifische T‑Zell‑Antwort bei Kopf‑ und Hals‑Krebs
Die Abwehr des Körpers gegen Kopf‑ und Halskrebs einsetzen
Kopf‑ und Halskarzinome sind weiterhin schwer zu behandeln, und selbst leistungsfähige neue Immuntherapien nutzen nur einem Bruchteil der Patienten. Diese Studie untersucht eine vielversprechende Idee: Immunzellen so zu schulen, dass sie krebsspezifische Signale besser erkennen, und diese Zellen anschließend von molekularen „Bremsen“ zu befreien, damit sie Tumore effektiver angreifen können. Für Menschen mit oder mit Risiko für Kopf‑ und Halskrebs weist diese Arbeit auf künftige Impfstoffe und Wirkstoffkombinationen hin, die aktuelle Behandlungen potenter und nachhaltiger machen könnten.
Warum aktuelle Immuntherapien so wenigen helfen
Moderne Krebsimmuntherapie zielt häufig auf Proteine ab, die als Immuncheckpoints wirken und wie Bremsen auf T‑Zellen fungieren — die weißen Blutzellen, die Tumore zerstören können. Beim Plattenepithelkarzinom des Kopfes und Halses (HNSCC) werden bereits Wirkstoffe eingesetzt, die den Checkpoint PD‑1 blockieren, wie Nivolumab oder Pembrolizumab. Dennoch profitieren nur etwa 20 % der Patienten, und viele Tumore schreiten letztlich voran. Die Autorinnen und Autoren wollten in einem kontrollierten Laborversuch verstehen, wie die PD‑1‑Blockade und verwandte Checkpointhemmer T‑Zellen beeinflussen, die zuvor dafür präpariert wurden, tumorspezifische Marker zu erkennen, und ob die Kombination mehrerer Checkpoint‑Antikörper über die PD‑1‑Blockade hinaus einen Zusatznutzen bringt.
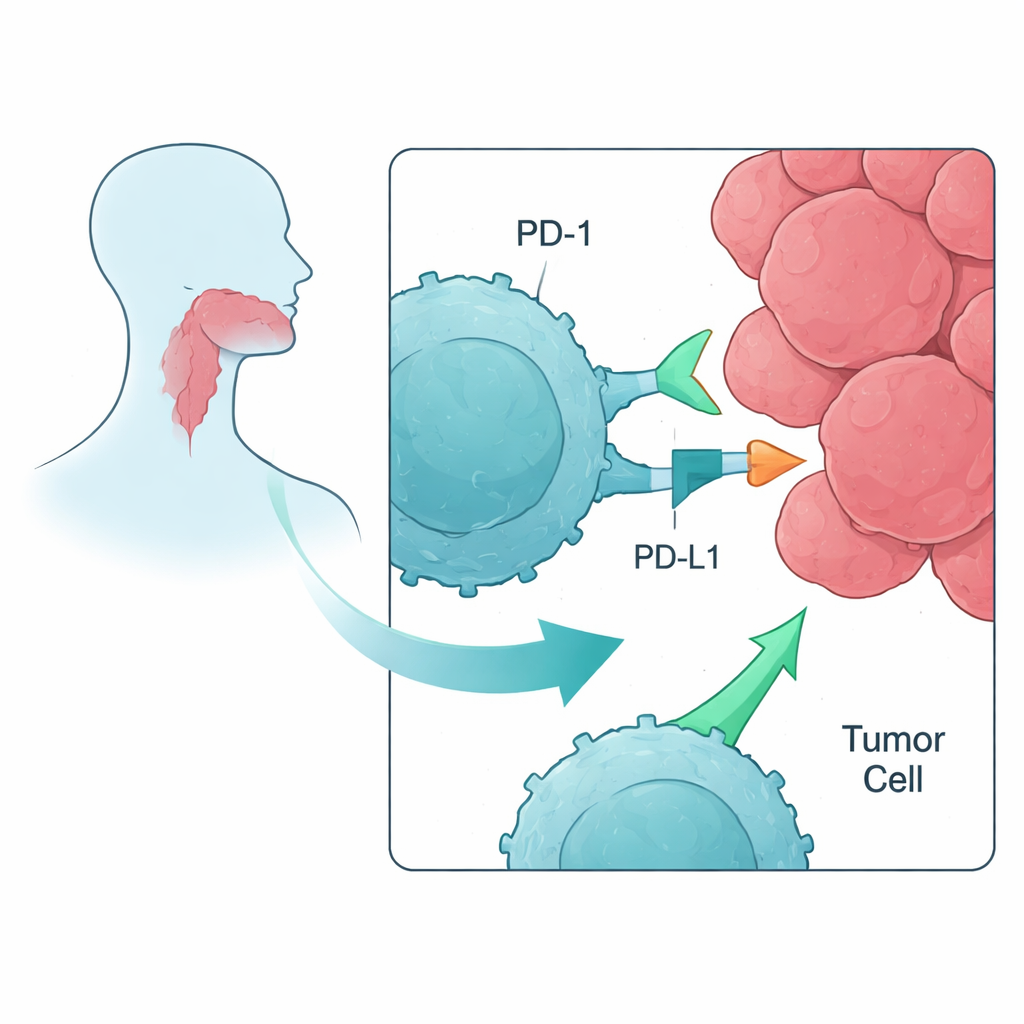
Immunzellen trainieren, Krebsziele zu sehen
Die Forschenden begannen mit Blutproben gesunder Freiwilliger statt mit Patientenmaterial, um zu modellieren, wie ein weniger geschädigtes Immunsystem früh im Krankheitsverlauf reagieren könnte. Sie isolierten periphere mononukleäre Blutzellen, zu denen auch T‑Zellen gehören, und setzten sie kurzen Proteinfragmenten (Peptiden) aus, die aus tumorspezifischen Antigenen stammen, wie sie bei Kopf‑und‑Hals‑Tumoren häufig vorkommen. Drei Targets erwiesen sich als besonders geeignet, T‑Zellen zu aktivieren: MAGE, NY‑ESO‑1 und PRAME. Während etwa einer Woche in gemischten Lymphozyten‑Peptid‑Kulturen wirkten diese Peptide wie Mini‑Impfstoffe und vermehrten seltene T‑Zellen, die jeweils das jeweilige krebsbezogene Merkmal spezifisch erkennen konnten.
Die Bremsen bei trainierten T‑Zellen lösen
Anschließend prüfte das Team, wie sich diese trainierten T‑Zellen verhalten, wenn sie in Gegenwart oder Abwesenheit von Checkpoint‑blockierenden Antikörpern mit echten Kopf‑und‑Hals‑Krebszellen konfrontiert werden. Sie verwendeten einen Standard‑Assay (ELISPOT), um die Freisetzung von Interferon‑gamma und Granzyme B zu messen — Signale dafür, dass T‑Zellen aktiviert sind und tötungsfähig sind. Über mehrere Spender hinweg steigerte die Zugabe des anti‑PD‑1‑Antikörpers konsistent die Reaktion antigenspezifischer T‑Zellen gegen die Tumorzelllinie und erhöhte die Aktivität oft um 60–100 % oder mehr im Vergleich zur reinen Peptidstimulation. Im Gegensatz dazu brachte die Blockade anderer Checkpoints wie LAG‑3 oder TIM‑3, allein oder in Kombination mit PD‑1‑Blockade, in diesem System wenig bis gar keinen zusätzlichen Nutzen.
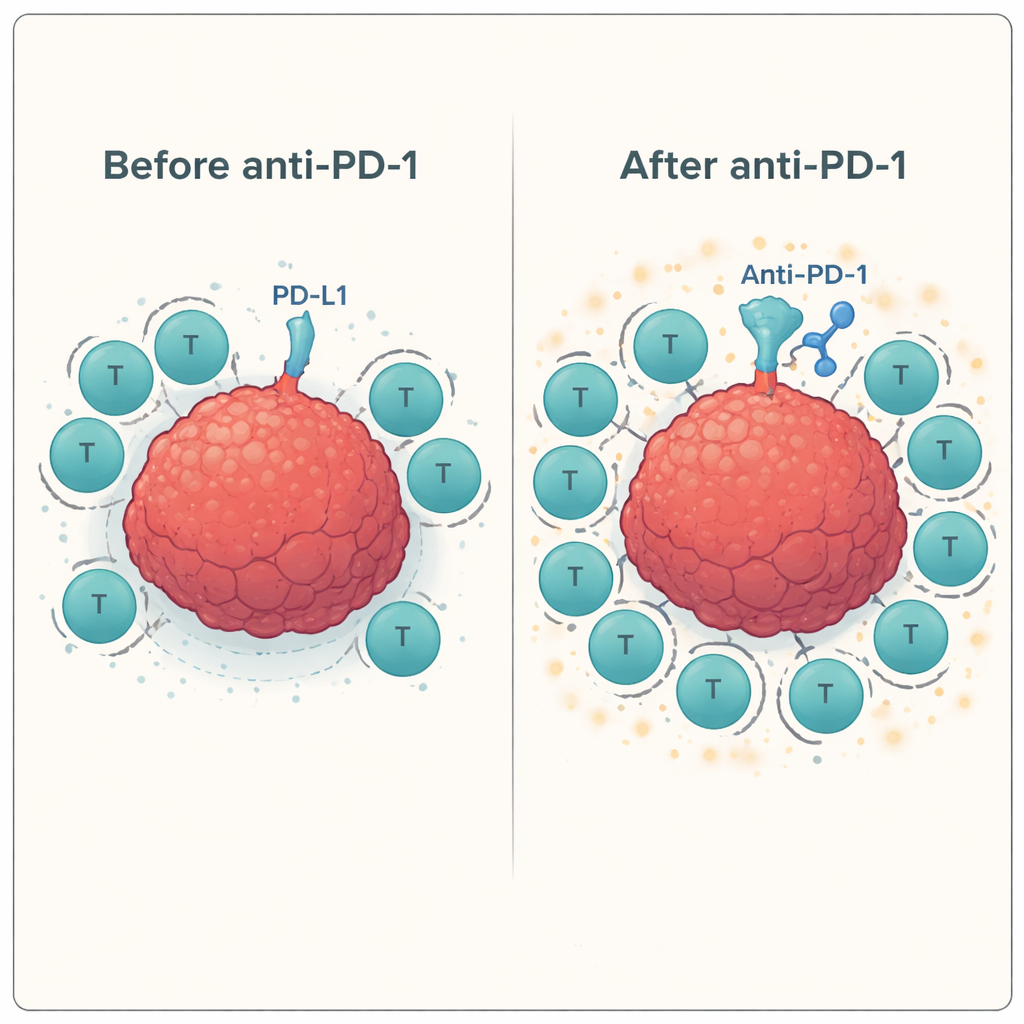
Die Immunlandschaft im Detail kartieren
Um zu verstehen, warum einige Kombinationen wirkten und andere nicht, nutzten die Forschenden Durchflusszytometrie, eine Methode zur Zählung und Charakterisierung einzelner Zellen. Sie zeigten, dass sowohl T‑Zellen als auch Tumorzellen PD‑1 und dessen Liganden PD‑L1 und PD‑L2 in relevanten Mengen exprimieren, was mehrere Kontaktpunkte schafft, an denen die PD‑1‑Bremse aktiv sein kann — und daher durch Medikamente blockiert werden kann. Marker, die mit LAG‑3 und TIM‑3 assoziiert sind, waren ebenfalls vorhanden, doch die Tumorzelllinie exprimierte nur eine Teilmenge ihrer Bindungspartner, was die begrenzte Wirkung des Zielens dieser Checkpoints erklären könnte. Außerdem beobachteten sie einen Trend zu erhöhten „Gas‑Signalen“ (ko‑stimulatorische Moleküle wie CD137 und GITR) auf T‑Zellen nach Peptidstimulation und PD‑1‑Blockade, was nahelegt, dass nach Lösung der Hauptbremse der Beschleuniger stärker durchgedrückt werden kann.
Was das für künftige Patientinnen und Patienten bedeuten könnte
Da diese Experimente außerhalb des Körpers durchgeführt wurden, können sie die komplexe Tumorumgebung oder die häufig geschwächten Immunsysteme von Patientinnen und Patienten nach Chemotherapie oder Strahlentherapie nicht vollständig nachbilden. Dennoch liefern die Ergebnisse eine klare Botschaft: Wenn T‑Zellen zuerst darin geschult werden, spezifische Krebs‑Markierungen zu erkennen (durch eine Peptid‑Impfung) und anschließend die PD‑1‑Bremse gelöst wird, sind sie deutlich besser darin, Kopf‑und‑Hals‑Tumorzellen anzugreifen. Zusätzliche Checkpoint‑Antikörper über PD‑1 hinaus halfen in diesem Setting nicht. Die Autorinnen und Autoren schließen, dass eine fokussierte Strategie — Patientinnen und Patienten mit tumorspezifischen Peptiden wie MAGE, NY‑ESO‑1 oder PRAME zu impfen und dies mit PD‑1‑Blockade zu kombinieren — in klinischen Studien geprüft werden sollte, um mehr Immunsysteme in effektive Krebsbekämpfer zu verwandeln.
Zitation: Schuler, P.J., Oliveri, F., Puntigam, L. et al. Immune checkpoint inhibition increases antigen-specific T cell response in head and neck cancer. Sci Rep 16, 5583 (2026). https://doi.org/10.1038/s41598-026-38740-z
Schlüsselwörter: Kopf‑ und Halskrebs, Immuncheckpointtherapie, PD‑1‑Blockade, Krebsimpfstoffe, Tumorantigene