Clear Sky Science · de
Chemische Synthese neuartiger Aminopyrimidin-4-yl-1H-pyrazol-Derivate als Inhibitoren der Milz-Tyrosin-Kinase (SYK)
Warum die Blockade eines einzelnen Enzyms bei Krebs und Entzündungen helfen könnte
Unser Immunsystem ist auf schnelle interne Signale angewiesen, die Zellen mitteilen, wann sie Angreifer bekämpfen und wann sie sich zurückhalten sollen. Wenn diese Signale gestört sind, können sie Autoimmunerkrankungen und Krebs fördern. Diese Studie untersucht einen vielversprechenden Weg, fehlerhafte Signale zu dämpfen, indem kleine, wirkstoffähnliche Moleküle entworfen werden, die gezielt ein Schlüsselenzym blockieren: die Milz-Tyrosin-Kinase (SYK), die im Zentrum vieler Immunreaktionen steht.
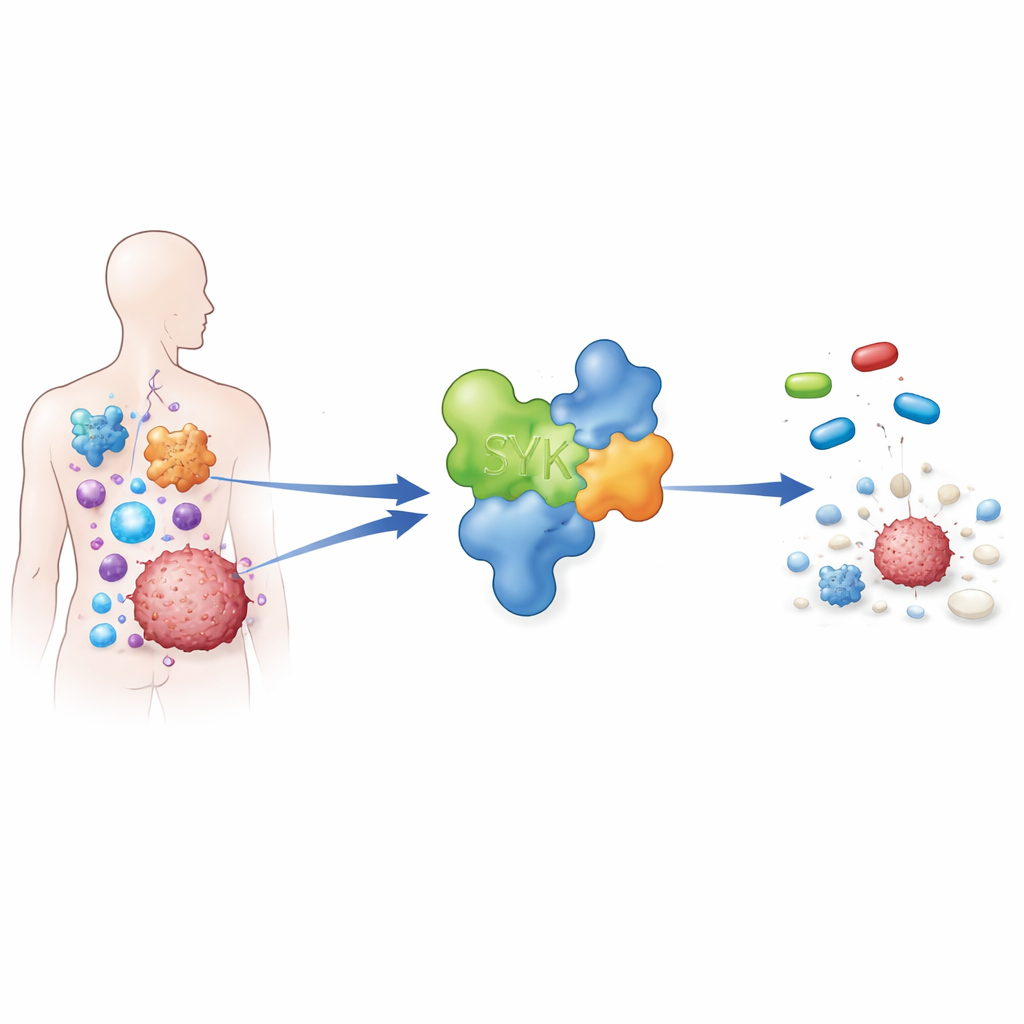
Ein Signalschalter im Kern vieler Erkrankungen
SYK wirkt wie ein Hauptschalter in bestimmten Immunzellen. Wenn es aktiviert ist, treibt es Entzündungen, Antikörperbildung und Zellwachstum voran. Unter normalen Bedingungen ist das nützlich zur Bekämpfung von Infektionen. Bei Erkrankungen wie rheumatoider Arthritis, Asthma sowie verschiedenen Blut- und soliden Tumoren kann SYK-Aktivität jedoch übermäßig werden, Immunzellen dauerhaft aktiv halten und das Überleben von Tumoren unterstützen. Aufgrund dieser zentralen Rolle versuchen Forscher weltweit, SYK-blockierende Medikamente zu entwickeln, die ausreichend wirksam sind, dabei aber präzise genug, um viele andere Enzyme nicht zu beeinträchtigen und Nebenwirkungen zu vermeiden.
Aufbau einer Familie maßgeschneiderter kleiner Moleküle
Die Autorinnen und Autoren entwickelten eine neue Reihe verwandter Moleküle, die auf einem gemeinsamen chemischen Gerüst basieren: Aminopyrimidin-4-yl-1H-pyrazol. Aus einfachen Bausteinen wurden diese Teile schrittweise zusammengesetzt und anschließend ein Bereich der Struktur modifiziert, um neun finale Kandidaten zu erhalten. Jedes Molekül wurde mit gängigen Analyseverfahren sorgfältig geprüft, um Struktur und Reinheit zu bestätigen. Dieser modulare Ansatz erlaubte dem Team, zu untersuchen, wie feine Veränderungen in Form und Flexibilität beeinflussen, wie die Verbindungen mit SYK interagieren.
Beobachten, wie die Verbindungen ihr Ziel fassen
Bevor sie an die Labortische gingen, verwendeten die Forschenden Computersimulationen, um abzuschätzen, wie fest jedes Molekül an SYK binden könnte. Docking-Berechnungen schätzten, wie gut die Verbindungen in die Bindungstasche des Enzyms passen, und hoben einen Kandidaten mit der Bezeichnung 44 als besonders vielversprechend hervor. Detailliertere Molekulardynamik-Simulationen, in denen das Protein–Wirkstoff-Komplex über hunderte Nanosekunden verfolgt wurde, zeigten, dass 44 eine besonders stabile Partnerschaft mit SYK eingeht. Das Protein blieb kompakt, wichtige Kontakte blieben erhalten, und das System fiel in eine einzige, energiearme Konformation mit vielen starken Wasserstoffbrücken, insbesondere unter Beteiligung von Aminosäuren wie Tryptophan und Serin, die das Molekül stützen.
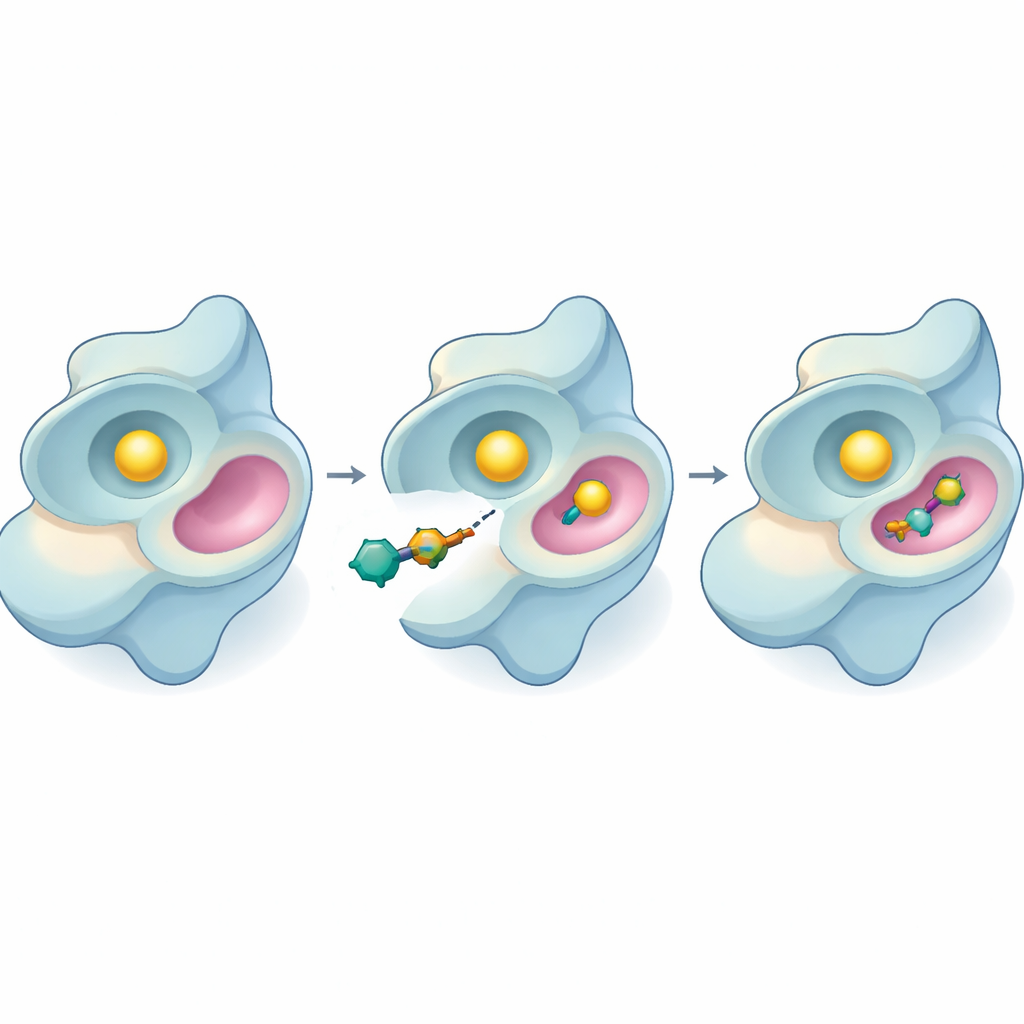
Die neuen Inhibitoren auf dem Prüfstand
Das Team führte anschließend Laborexperimente mit einem lichtbasierten Test durch, der misst, wie aktiv SYK sein Energieträgermolekül ATP verbraucht. Mehrere der neuen Verbindungen verlangsamten das Enzym, doch 44 stach erneut hervor. Es hemmte SYK bei sehr niedrigen Konzentrationen und wurde wirksamer, je länger es mit dem Enzym in Kontakt blieb. Durch Variation der Substratmenge konnten die Forschenden schließen, wie 44 wirkt: Statt direkt mit ATP um die Hauptaktivationsstelle zu konkurrieren, scheint es an einer anderen, allosterischen Stelle zu binden und das Enzymverhalten aus der Distanz zu verändern. Das ist wichtig, weil allosterische Inhibitoren ihre Wirkung oft beibehalten, selbst wenn ATP-Spiegel hoch sind oder Mutationen die primäre Stelle verändern.
Was das für künftige Behandlungen bedeuten könnte
Zusammen ergeben die Computermodelle und Laborbefunde ein stimmiges Bild: Molekül 44 bindet SYK stark, hält das Enzym in einem stabilen, weniger flexiblen Zustand und schaltet seine Aktivität über einen indirekten, nicht-kompetitiven Mechanismus herunter. Für Nicht-Fachleute bedeutet das, dass die Forschenden einen fein abgestimmten chemischen Schlüssel identifiziert haben, der in ein Schloss passt, das für viele immungetriebene Erkrankungen kritisch ist, ohne einfach die Hauptöffnung zu blockieren. Obwohl noch viel Arbeit vorliegt – insbesondere Tests in Zellen, an Tieren und in erweiterten Panels verwandter Enzyme – bietet dieses Gerüst einen vielversprechenden Ausgangspunkt für künftige Wirkstoffe, die schädliche Entzündungen dämpfen und bestimmte Krebsarten verlangsamen könnten, indem sie SYK ins Visier nehmen.
Zitation: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Schlüsselwörter: Milz-Tyrosin-Kinase, Kinaseninhibitoren, Krebstherapeutika, Autoimmunerkrankung, allosterische Medikamente