Clear Sky Science · de
Validierung von Chemoresistenz-Phänotypen beim Pleura-Mesotheliom in 2D-, 3D- und In-vivo-Modellen
Warum manche Krebsarten Chemotherapie abschütteln
Bei Menschen mit Pleuramesotheliom — einem mit Asbestexposition in Verbindung gebrachten Krebs — ist Chemotherapie oft die Hauptbehandlungsoption. Viele Tumoren sprechen jedoch kaum an, oder sie schrumpfen zunächst und wachsen dann schnell wieder nach. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Sind die Labor‑Modelle, die Forschende zur Prüfung von Medikamenten verwenden, realistisch genug, um vorherzusagen, was tatsächlich im Körper eines Patienten passiert?
Von flachen Zellschichten zu winzigen Tumorkugeln
Die meisten Krebsmedikamente werden zunächst an Zellen getestet, die als flache Schichten auf Plastikplatten wachsen. Diese zweidimensionalen (2D) Kulturen sind praktisch, ähneln aber nicht echten Tumoren, die dreidimensionale (3D) Massen aus dicht gepackten Zellen sind, eingebettet in eine komplexe Nachbarschaft aus Blutgefäßen, Gerüstproteinen und Immunzellen. Die Forscher bauten ein 3D‑"Sphäroid"‑Modell des Mesothelioms, in dem Krebszellen zu kompakten Mini‑Tumoren zusammenklumpen. Sie verglichen, wie Mesotheliomzellen aller wichtigen Subtypen — epithelioid, biphasisch und das hochaggressive sarkomatoide — auf die Standardchemotherapie reagieren, wenn sie entweder als flache 2D‑Schichten oder als 3D‑Sphäroide kultiviert werden.
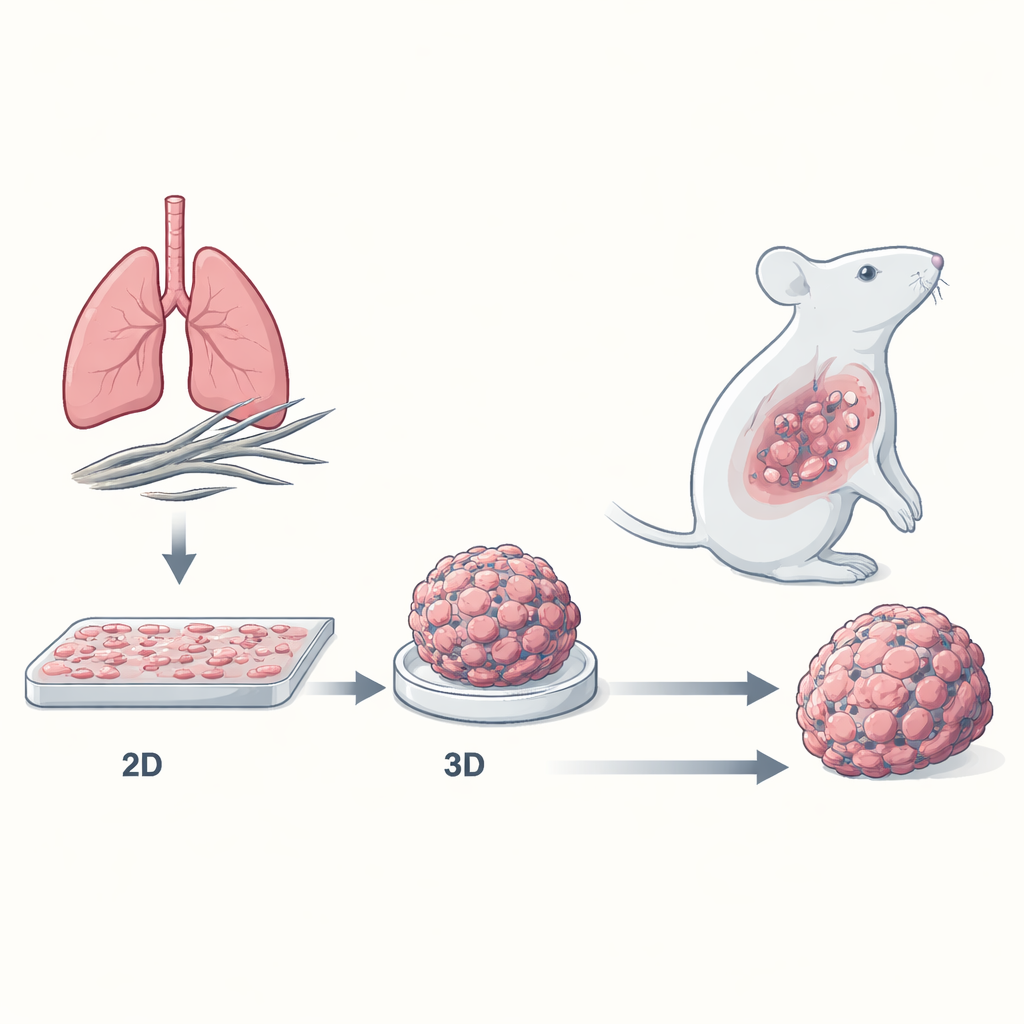
3D‑Mini‑Tumoren sind deutlich schwerer zu töten
Bei Exposition gegenüber der häufig verwendeten Kombination Cisplatin–Pemetrexed wurden Mesotheliomzellen in 2D‑Schichten schnell geschädigt: ihr Wachstum verlangsamte sich, viele blieben in einer gestoppten "S‑Phase" des Zellzyklus stecken und zahlreiche Zellen durchliefen den programmierten Zelltod (Apoptose). Dagegen schrumpften 3D‑Sphäroide kaum und benötigten deutlich höhere Dosen, um vergleichbare Effekte zu erzielen. Der sarkomatoide Subtyp, der klinisch als am schwersten behandelbar gilt, war auch im 3D‑Modell am resistentesten — ein Spiegelbild des klinischen Verhaltens. Detaillierte Messungen zeigten, dass 2D‑Zellen nach der Behandlung an Vitalität verloren und in Richtung Zelltod fortschritten, während Zellen in Sphäroiden größtenteils am Leben blieben, mit nur moderaten Zunahmen an frühstadialer Apoptose.
Ein ruhigerer Stoffwechsel und überlebensfördernde Signale
Das Team untersuchte die Unterschiede im Energieverbrauch der beiden Modelle mittels eines metabolischen "Stresstests". Die Chemotherapie drängte 2D‑Zellen aus einem aktiven, energiehungrigen Zustand in einen ruhigeren Modus, mit starken Einbrüchen in der mitochondrialen Sauerstoffverbrauchsrate — ein Hinweis darauf, dass die Behandlung ihre inneren Kraftwerke störte. Im Gegensatz dazu befanden sich die 3D‑Sphäroide bereits in einem energiearmen, sauerstoffarmen Zustand, der sich durch die Behandlung kaum veränderte, ähnlich den gestressten, hypoxischen Verhältnissen in echten Tumoren. Die Forschenden maßen außerdem kleine regulatorische Moleküle, sogenannte microRNAs, und fanden subtypspezifische Muster, die mit Arzneimittelresistenz verknüpft sind. Insbesondere nicht‑epithelioide Sphäroide erhöhten microRNAs, die zuvor mit ungünstiger Prognose und reduziertem Zelltod in anderen Krebsarten in Verbindung gebracht wurden. In Tumoren, die bei Mäusen aus 3D‑Sphäroiden gewachsen waren, waren Proteine involviert in starken Überlebenswegen — PI3K/AKT und VEGF/Notch — hochreguliert, was die Krebszellen zusätzlich vor dem Absterben schützte.
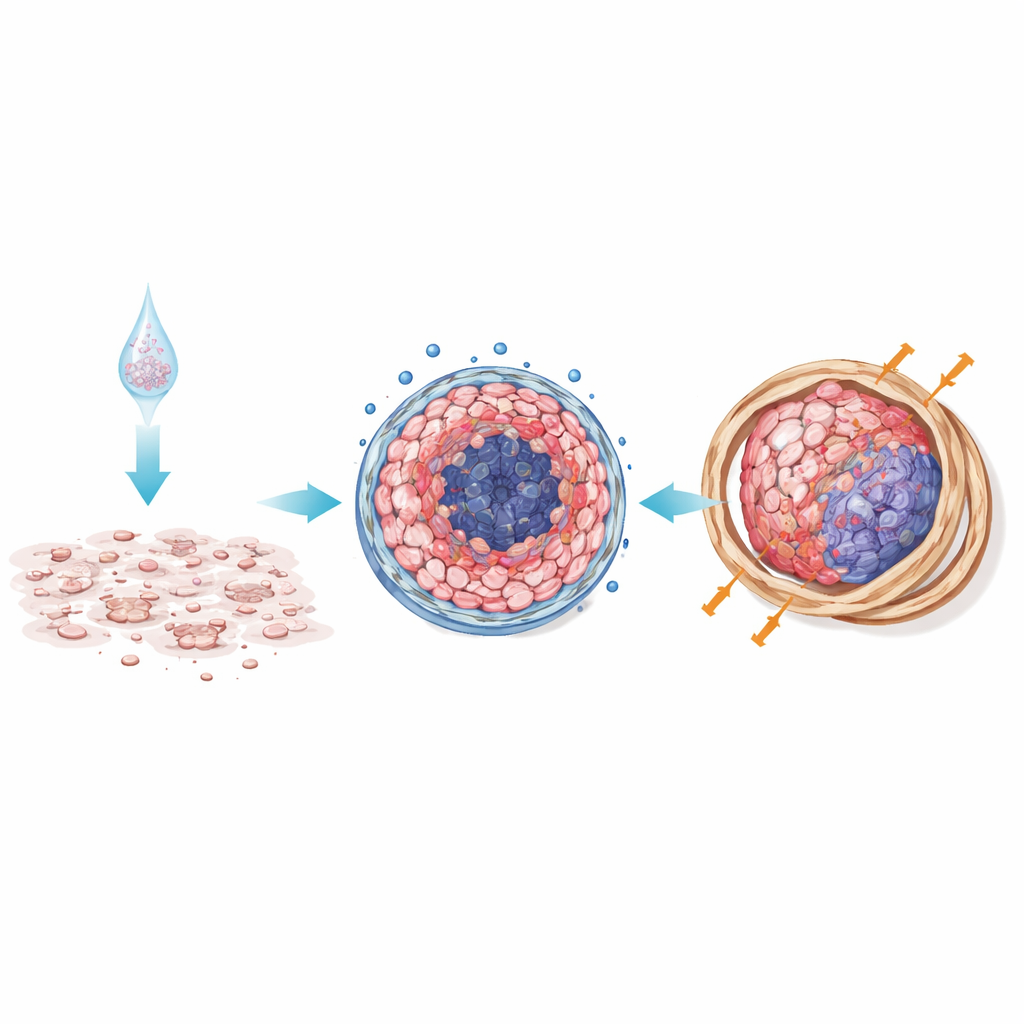
Maus‑Tumoren bestätigen, was die Schale vorhersagt
Um zu prüfen, ob diese Unterschiede in lebenden Organismen relevant sind, implantierten die Wissenschaftler Mesotheliomzellen in Mäuse entweder als Einzelzellen (als Modell für 2D‑Kultur) oder als vorgeformte 3D‑Sphäroide. Tumoren, die als Sphäroide begonnen hatten, wuchsen größer und sprachen schlechter auf Chemotherapie an als jene, die als Einzelzellen begonnen hatten. Unter dem Mikroskop zeigten aus 3D stammende Tumoren dichte Bänder aus Kollagen und faserigem Gewebe, mit stärker organisierten Zellnestern und weniger totem Gewebe. Diese fibröse Hülle wirkt wahrscheinlich als physikalische und biochemische Barriere, begrenzt die Medikamentendurchdringung und verstärkt Überlebenssignale — Bedingungen, die hartnäckigen menschlichen Tumoren sehr ähnlich sind.
Was das für künftige Behandlungen bedeutet
Für Laien lautet die zentrale Botschaft: Wie wir Krebszellen im Labor züchten, kann die Realitätsnähe von Medikamententests entscheidend beeinflussen. Winzige 3D‑Tumorsphäroide reproduzieren zentrale Eigenschaften des Mesothelioms, die flache Zellschichten nicht abbilden: sauerstoffarme Kerne, gestresste, aber schwer zu tödende Zellen, schützendes narbenähnliches Gewebe und die Aktivierung von Überlebenswegen, die den Zelltod blockieren. Weil sich diese 3D‑Modelle im Verhalten deutlich eher wie echte Tumoren bei Patienten und in Mausmodellen verhalten, bieten sie eine robustere Grundlage, um Wirkstoffe zu entdecken und Kombinationen zu testen, die sowohl die Krebszellen als auch ihre schützende Umgebung angreifen. Langfristig könnten solche realistischeren Modelle Forschenden helfen, Behandlungen zu identifizieren, die in der Klinik bessere Erfolgschancen haben — nicht nur im Labor.
Zitation: Shi, H., Selvamani, S.P., Zelei, R. et al. Validation of chemoresistance phenotypes in pleural mesothelioma across 2D, 3D, and in vivo models. Sci Rep 16, 8396 (2026). https://doi.org/10.1038/s41598-026-38692-4
Schlüsselwörter: Pleuramesotheliom, Chemotherapie-Resistenz, 3D-Tumor-Sphären, Tumormikroumgebung, Modelle für Krebsmedikamententests