Clear Sky Science · de
Adaptive Multi‑Feature‑Fusionsarchitektur mit optimiertem Lernen für hochauflösende Hirntumorklassifikation in der MRT
Warum es wichtig ist, Hirntumoren früh zu erkennen
Hirntumoren gehören zu den gefährlichsten Krebsarten, und nicht nur ihr Vorhandensein, sondern auch ihre Schwere früh zu bestimmen, kann über wirksame Behandlung oder schnellen Krankheitsverlauf entscheiden. Ärztinnen und Ärzte stützen sich stark auf MRT‑Scans, doch selbst erfahrenen Spezialisten fällt es schwer, langsam wachsende Tumoren von schnellen, tödlichen Varianten zu unterscheiden, wenn die Bilder verrauscht oder kontrastarm sind. Diese Studie stellt ein KI‑System vor, das Gehirnscans klarer und beständiger auswerten soll, mit dem Ziel, gesunde Gehirne und zwei Haupttypen von Gliomen – den häufigsten primären Hirntumoren – nahezu perfekt zu trennen.
Ein verschwommenes Bild bereinigen
Medizinische Bilder sind oft weit davon entfernt, perfekt zu sein. Tumoren können in das umgebende Gewebe verschwimmen, und Scannerrauschen kann kleine, aber wichtige Details verbergen. Die Autoren beginnen deshalb damit, die MRT‑Bilder selbst wiederaufzubauen. Zunächst wenden sie eine sorgfältig abgestimmte Kontrastanpassung an, die helle und dunkle Bereiche im Scan stärker voneinander absetzt, sodass die Ränder abnormer Gewebe deutlicher hervortreten. Unmittelbar danach setzen sie ein tiefes neuronales Netz zum Entrauschen ein, das darauf trainiert ist, körniges Rauschen zu entfernen und gleichzeitig feine Strukturen zu erhalten. Tests zeigen, dass diese zweistufige Bereinigung Bilder liefert, die schärfer sind und die anatomische Struktur besser bewahren als mehrere in Krankenhäusern gebräuchliche Standardverfahren.
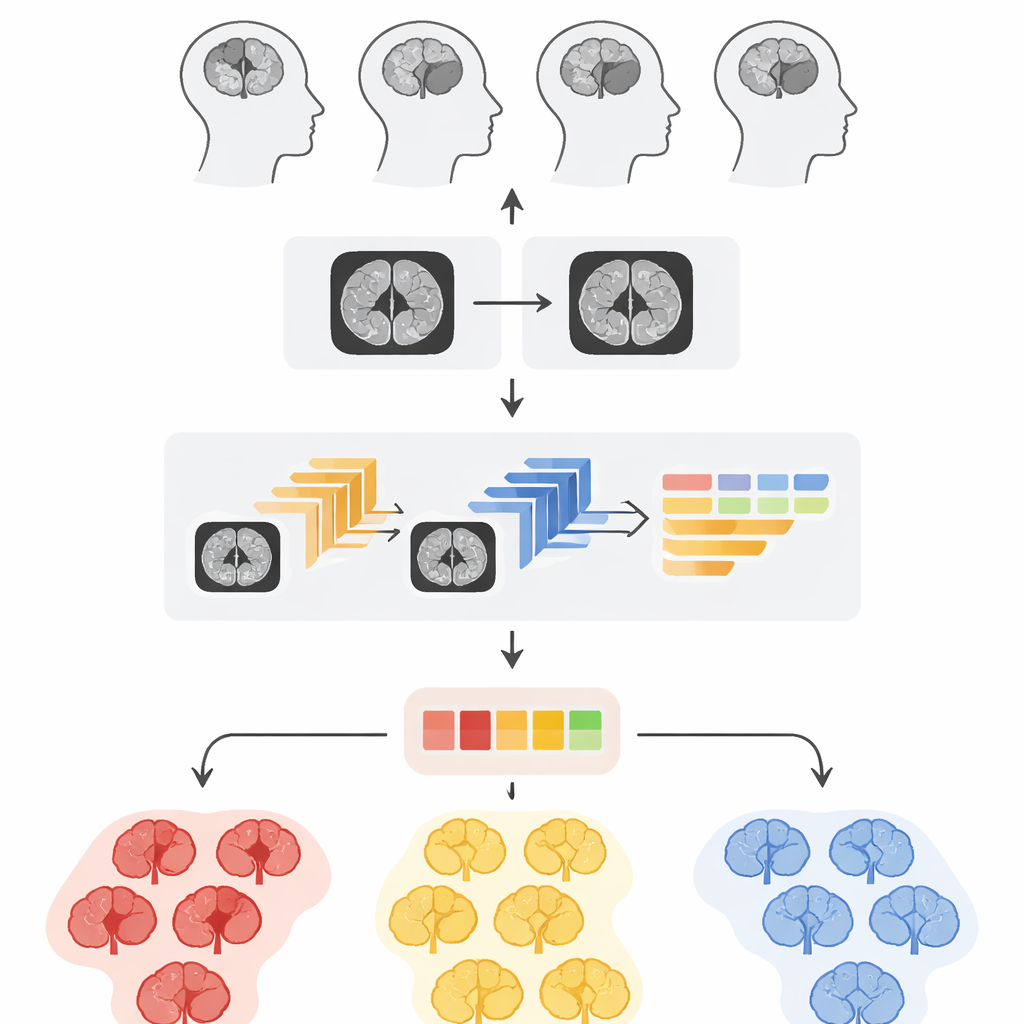
Computern beibringen, das zu sehen, was Ärzte sehen
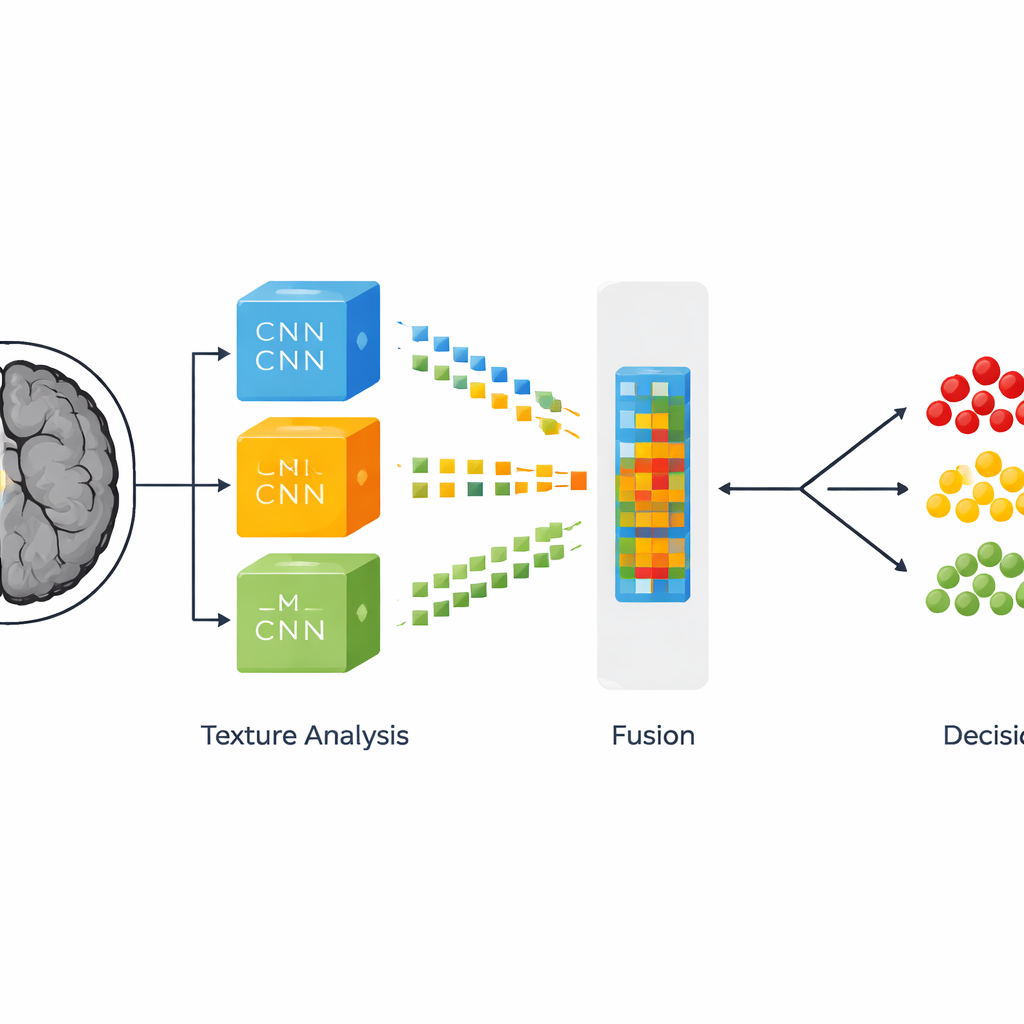
Sind die MRT‑Schnitte bereinigt und skaliert, stellt sich die subtilere Frage: Ist dieses Gehirn gesund, beherbergt es einen langsam wachsenden Tumor, oder droht ein aggressiver Tumor? Dazu kombinieren die Forschenden zwei Arten der Bildbeschreibung. Die erste stammt von drei leistungsfähigen, vortrainierten neuronalen Netzen, die ursprünglich für allgemeine Bilderkennung entwickelt und dann für Gehirnscans feinabgestimmt wurden. Diese Netze lernen, großflächige Muster wie Formen und tumorähnliche Regionen zu erkennen. Die zweite Beschreibung konzentriert sich auf Textur—feine Helligkeitsvariationen und Körnigkeit, die oft zwischen Tumorgraden unterscheiden. Diese Texturanalyse verwendet ein klassisches statistisches Werkzeug, das zählt, wie häufig verschiedene Graustufen nebeneinander auftreten, und so subtile Oberflächenmuster in Zahlen übersetzt, die ein Computer verarbeiten kann.
Viele Hinweise zu einem Urteil verschmelzen
Statt sich zwischen Deep Learning und Texturanalyse zu entscheiden, verbinden die Autoren beides. Aus jedem der drei neuronalen Netze wählen sie drei besonders aussagekräftige interne Schichten und formen deren komplexe Aktivierungsmuster zu langen Merkmalslisten. Jede dieser neun Mengen wird dann mit den entsprechenden Texturmaßen kombiniert und bildet so die von den Autoren sogenannten fused feature representations. Diese hybriden Fingerabdrücke der MRT‑Schnitte werden anschließend mehreren Entscheidungsalgorithmen übergeben, darunter Random Forests, Boosted Decision Trees und Support Vector Machines, sowie einem gestapelten Ensemble, das deren Ausgaben mischt. Durch das Ausprobieren vieler Kombinationen identifiziert das Team, welche Mischung aus Merkmalen und Klassifikator über Tausende Bilder hinweg die zuverlässigsten Entscheidungen liefert.
Verlässlichkeit messen, nicht nur rohe Genauigkeit
Um die Leistungsfähigkeit ihres Systems zu bewerten, geben die Forschenden mehr an als eine einzige Genauigkeitszahl. Sie berechnen, wie oft das System Erkrankungen korrekt erkennt, wie oft es korrekt bestätigt, dass ein Scan unauffällig ist, und wie selten es Alarm schlägt, wenn kein Grund besteht. Die beste Konfiguration—Merkmale aus einer bestimmten Netzschicht kombiniert mit Texturdaten und klassifiziert durch eine Support Vector Machine—kennzeichnet etwa 99 von 100 Bildern korrekt. Sie weist außerdem sehr hohe Sicherheit darauf hin, dass ein positives Ergebnis tatsächlich einen Tumor bedeutet und dass ein negatives Ergebnis wirklich kein gefährliches Wachstum anzeigt. Statistische Tests bestätigen, dass diese Spitzenkonfiguration nicht nur Glück ist, sondern signifikant besser als die alternativen Klassifikatoren, die sie ausprobiert haben.
Was das für Patientinnen, Patienten und Kliniken bedeutet
Praktisch zeigt die Studie, dass eine durchdachte Kombination aus stärkerer Bildbereinigung, mehreren Deep‑Learning‑Modellen und traditioneller Texturanalyse eine nahezu fehlerfreie Einordnung von Hirn‑MRTs in die Kategorien gesund, langsam wachsender Tumor und schnell wachsender Tumor ermöglichen kann. Die gesamte Pipeline kann einen einzelnen Scan‑Schnitt in deutlich unter einer Sekunde analysieren, was darauf hindeutet, dass sie sich ohne Verzögerung in klinische Abläufe integrieren ließe. Obwohl das System erfahrene Radiologinnen und Radiologen nicht ersetzt, könnte es als verlässliches zweites Augenpaar dienen—insbesondere in überlasteten Notaufnahmen oder Regionen mit wenigen Spezialisten—und dazu beitragen, dass aggressive Tumoren schnell erkannt und mildere Fälle nicht überbehandelt werden.
Zitation: Safy, M., Abd-Ellah, M.K., Bayoumi, E.S. et al. Adaptive multi-feature fusion architecture with optimized learning for high-fidelity brain tumor classification in MRI. Sci Rep 16, 8498 (2026). https://doi.org/10.1038/s41598-026-38672-8
Schlüsselwörter: Hirntumor MRT, Gliom‑Grading, KI für medizinische Bildgebung, Merkmalsfusion, Tumorklassifikation