Clear Sky Science · de
Studie zur differentiellen Expression disulfidptose‑bezogener Gene und ihrer Verbindung zur Immunregulation bei Patienten mit diabetischer Retinopathie
Warum diese Augenkrankheit uns alle betrifft
Da Diabetes weltweit häufiger wird, ist eine der gefürchtetsten Komplikationen die diabetische Retinopathie — eine Erkrankung, die das lichtempfindliche Gewebe im hinteren Teil des Auges schädigt und zu irreversibler Erblindung führen kann. Ärztinnen und Ärzte tun sich weiterhin schwer damit, vorherzusagen, welche Patienten ihr Sehvermögen verlieren werden und wie man sie am besten schützen kann. Diese Studie untersucht eine neu beschriebene Form des Zelltods, genannt Disulfidptose, und fragt, ob damit verbundene Gene im Blut frühe Schäden im Auge anzeigen und neue Wege zur Verhinderung von Sehverlust aufzeigen können.
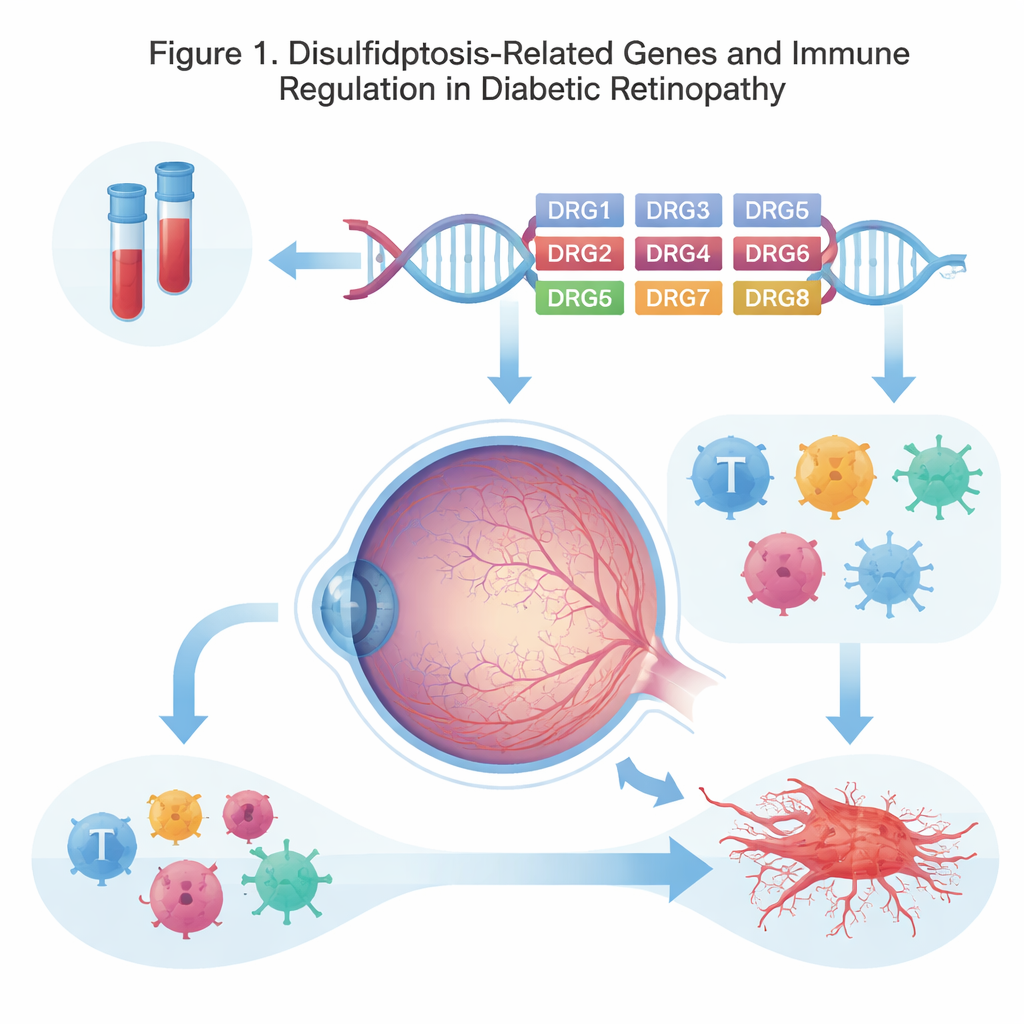
Eine neue Art des Zellzusammenbruchs
Unsere Zellen reparieren und recyceln sich ständig, und viele Krankheiten entstehen, wenn diese eingebauten Todesprogramme fehlregulieren. Forschende beschrieben kürzlich die Disulfidptose, einen Prozess, bei dem sich bestimmte chemische Bindungen in Strukturproteinen abnormal anreichern, das innere Gerüst der Zelle destabilisieren und zum Zusammenbruch führen. Weil die diabetische Retinopathie mit langfristig hohen Blutzuckerwerten, oxidativem Stress und fragilen Blutgefäßen in der Netzhaut einhergeht, vermuteten die Autorinnen und Autoren, dass Disulfidptose‑bezogene Gene an dem schleichenden Schaden beteiligt sein könnten, der Menschen das Sehvermögen raubt.
Auf der Suche nach Warnsignalen im Blut
Das Team nutzte eine große öffentliche Datenbank mit Blutproben von Personen mit und ohne diabetische Retinopathie. Sie konzentrierten sich auf 16 Gene, die zuvor mit Disulfidptose in Verbindung gebracht wurden, und verglichen, wie stark diese Gene bei Patienten mit Augenkrankheit im Vergleich zu gesunden Freiwilligen aktiviert waren. Acht Gene fielen als durchgehend unterschiedlich auf, wobei mehrere eine leicht erhöhte Aktivität und zwei eine verminderte Aktivität bei Betroffenen zeigten. Die Forschenden sammelten dann frische Blutproben von ihren eigenen Krankenhauspatienten und bestätigten, dass dieselben Gene, insbesondere die beiden Gene FLNB und GYS1, dasselbe Auf‑oder‑Ab‑Muster zeigten. Obwohl sich jedes Gen nur moderat veränderte, waren die Veränderungen über viele Personen hinweg beständig genug, um bedeutsam zu sein.
Wie Blutzellen und Thrombozyten das Auge schädigen könnten
Als Nächstes fragten die Wissenschaftlerinnen und Wissenschaftler, welche Funktion diese Gene haben könnten. Mithilfe gängiger Bioinformatik‑Werkzeuge fanden sie, dass die veränderten Gene in Signalwegen angereichert waren, die mit Blutgerinnung, Thrombozytenaktivierung und dem Erhalt der normalen Durchblutung zu tun haben. Diese Prozesse sind zentral für die diabetische Retinopathie, bei der winzige Kapillaren in der Netzhaut verstopfen, undicht werden und dann fragile neue Gefäße ausbilden. Eine andere Gruppe von Signalwegen, darunter Rap1‑ und MAPK‑Signalgebung, ist dafür bekannt, wie fest Blutgefäßzellen zusammenhalten und wie sie auf entzündlichen Stress reagieren. Die Studie legt nahe, dass subtile Verschiebungen in Disulfidptose‑bezogenen Genen Thrombozyten und Gefäßzellen in eine schädliche Richtung drängen könnten und so im Laufe der Zeit zu blockierten oder geschwächten Netzhautgefäßen beitragen.
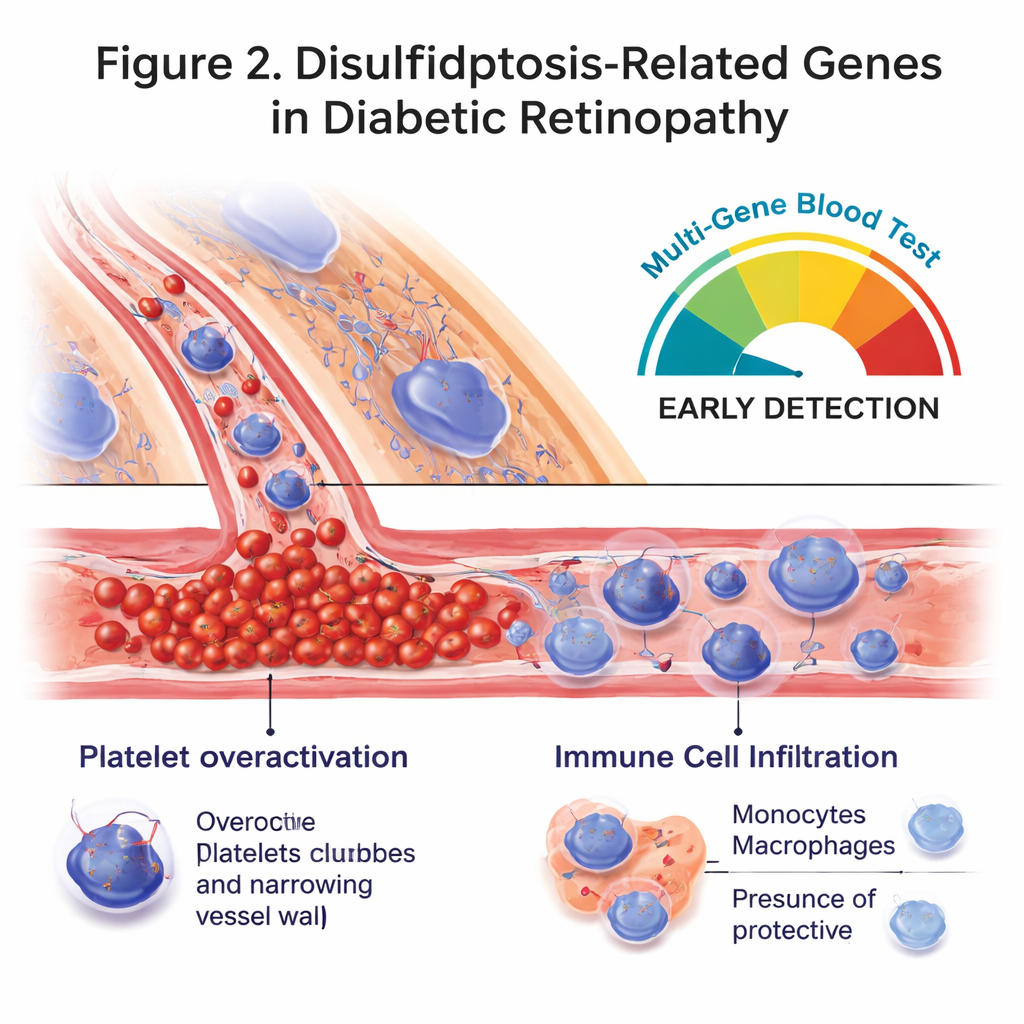
Immunzellen und ein blutbasierter Risiko‑Score
Die Autorinnen und Autoren untersuchten außerdem Muster von Immunzellen in denselben Blutproben mithilfe rechnerischer Methoden. Personen mit diabetischer Retinopathie hatten mehr zirkulierende Monozyten und wenig differenzierte Makrophagen — Zellen, die Entzündungen verstärken können — und weniger aktivierte Gedächtnis‑T‑Zellen, die normalerweise helfen, eine ausgeglichene Immunantwort zu koordinieren. Mehrere der Disulfidptose‑bezogenen Gene zeigten moderate Zusammenhänge mit diesen Immunverschiebungen, was darauf hindeutet, dass sie steuern könnten, wie sich das Immunsystem bei Diabetes verhält. Aufbauend auf diesen Verbindungen kombinierten die Forschenden alle acht Schlüssengene zu einem einzigen Risiko‑Score mithilfe eines statistischen Modells. Diese Multi‑Gen‑„Signatur“ unterschied Patienten mit Augenkrankheit von gesunden Kontrollen mit relativ hoher Genauigkeit, übertraf einzelne Gene und bietet ein mögliches Konzept für einen zukünftigen Bluttest.
Was das für Menschen mit Diabetes bedeuten könnte
Vorerst ist die Arbeit hauptsächlich ein Proof of Concept. Das Modell wurde anhand eines öffentlichen Datensatzes und einer relativ kleinen Krankenhauskohorte erstellt, und die Studie zeigte nicht direkt Disulfidptose in Augengewebe. Dennoch ist sie die erste, die diesen neuen Zelltodweg mit diabetischer Retinopathie verknüpft und ein Set von blutbasierten Genen vorschlägt, das sowohl mit Gefäßverletzung als auch mit immunologischer Dysbalance verbunden ist. Falls diese Befunde in größeren und diverseren Patientengruppen bestätigt werden, könnten diese Genmuster Teil eines kostengünstigen Bluttests werden, um Personen mit hohem Risiko für Sehverlust zu identifizieren, solange ihre Augen noch gesund erscheinen — und so früheres Monitoring und individuellere Präventionsstrategien ermöglichen.
Zitation: Hao, Y., Zhang, XX., Wang, XY. et al. Study on the differential expression of disulfidptosis-related genes and their association with immune regulation in patients with diabetic retinopathy. Sci Rep 16, 7654 (2026). https://doi.org/10.1038/s41598-026-38671-9
Schlüsselwörter: diabetische Retinopathie, Disulfidptose, Biomarker, Immunzellen, Gen‑Risikomodell