Clear Sky Science · de
ConvAHKG: Aktionsbasierter hybrider Wissensgraph mit einem dualen Faltungsansatz zur Wirkstoffumwidmung
Neue Anwendungen für alte Medikamente finden
Die Entwicklung eines völlig neuen Medikaments bis zur Marktreife kann mehr als ein Jahrzehnt dauern und Milliarden kosten, und viele Kandidaten scheitern unterwegs. Diese Studie untersucht eine klügere Abkürzung: Daten und künstliche Intelligenz zu nutzen, um neue Krankheitsindikationen zu finden, die bestehende, bereits zugelassene Medikamente sicher behandeln könnten. Die Autor*innen stellen ein Framework namens ConvAHKG vor, das viele Arten biomedizinischer Informationen zu einer einzigen vernetzten Karte verknüpft und dann ein modernes neuronales Netzwerk einsetzt, um vielversprechende Wirkstoff–Krankheits-Paare zu erkennen — ein schnellerer, kostengünstigerer Weg zu neuen Therapien.
Eine umfangreiche Karte der Wechselwirkungen von Medikamenten und Krankheiten
Im Zentrum dieser Arbeit steht ein „hybrider Wissensgraph“, eine riesige Karte, die Medikamente, Krankheiten, Proteine, Nebenwirkungen, chemische Strukturen und biologische Pfade miteinander verbindet. Statt nur einfache Ja–Nein-Verknüpfungen zu speichern (zum Beispiel „Medikament A behandelt Krankheit B“), zeichnet die Karte auf, wie ein Medikament auf ein Protein wirkt — ob es es aktiviert, hemmt oder daran bindet — und wie Proteine an Krankheiten beteiligt sind, etwa als Biomarker oder durch Aktivitätsänderungen. Der Graph enthält über 11.000 Entitäten und 59 Beziehungstypen, einschließlich detaillierter Informationen zu Medikamentenklassifikationen, Nebenwirkungen, Protein–Protein-Kontakten und chemischen Substrukturen. Indem er diese vielen Kontextschichten erfasst, kann der Graph mehr von der realen biologischen Komplexität hinter Behandlungswirkungen und unerwünschten Reaktionen widerspiegeln. 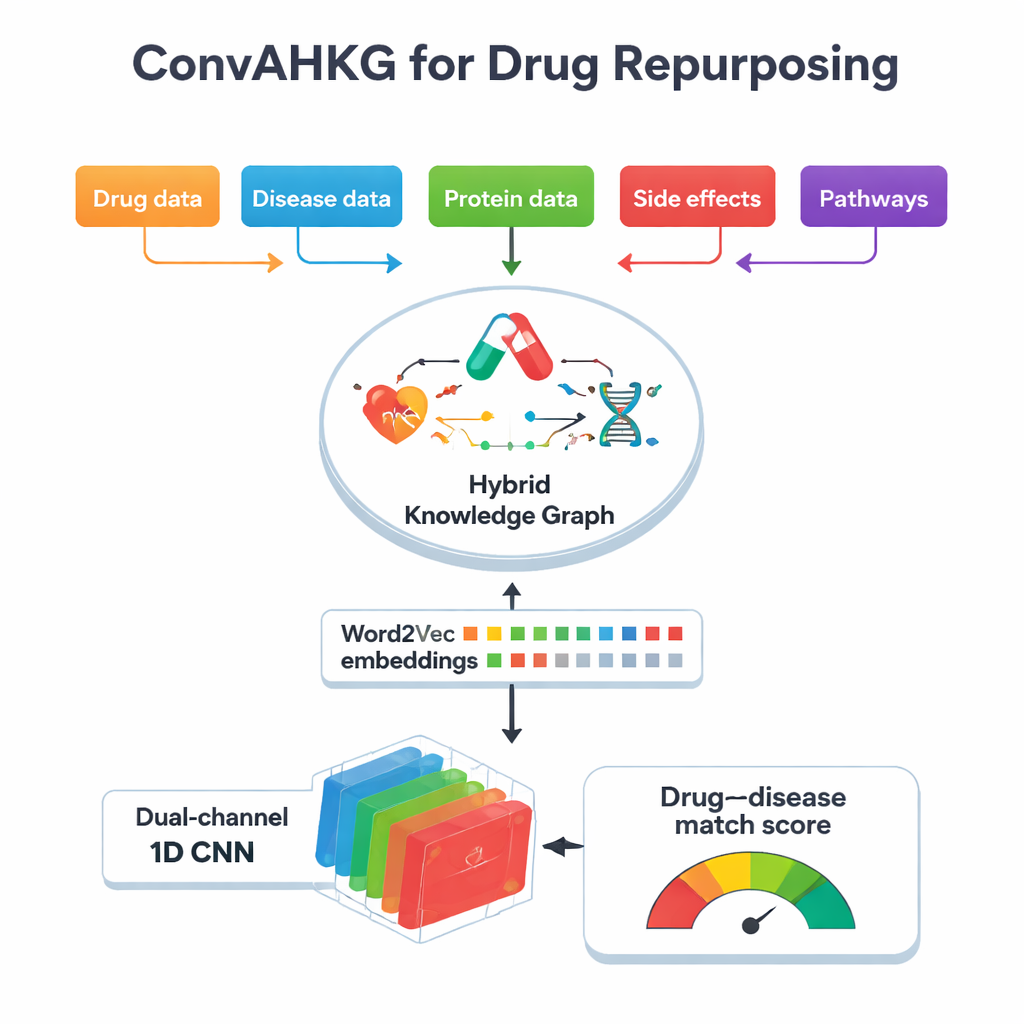
Dem Computer die Sprache der Biologie beibringen
Um diese komplexe Karte für maschinelles Lernen nutzbar zu machen, wandelt das Team jede Verbindung im Graphen in einen einfachen dreiteiligen „Satz“ um: ein Head (zum Beispiel eine Krankheit), eine Relation (zum Beispiel Biomarker) und ein Tail (zum Beispiel ein Protein). Anschließend wenden sie Word2Vec an, eine ursprünglich für die Verarbeitung natürlicher Sprache entwickelte Methode, um numerische „Embeddings“ für jedes Medikament, jede Krankheit und jedes Protein zu lernen. Elemente, die in diesen Sätzen häufig zusammen auftreten, liegen in diesem mathematischen Raum nah beieinander, ähnlich wie Wörter mit ähnlicher Bedeutung im Text. Dieser Ansatz ist deutlich einfacher und schneller als viele graphenspezifische Embedding-Techniken, erfasst dabei aber dennoch subtile Muster. In Tests gegenüber mehreren populären Wissensgraph-Embedding-Methoden erreichte Word2Vec vergleichbare oder bessere Vorhersageleistung bei deutlich geringerer Rechenzeit.
Ein dualer neuronaler Pfad für Ja/Nein-Behandlungsentscheidungen
Sobald jedes Medikament und jede Krankheit in einen numerischen Vektor übersetzt ist, speist ConvAHKG diese in ein dual-kanaliges eindimensionales Faltungsneuronales Netz. Ein Kanal verarbeitet den Medikamentenvektor, der andere den Krankheitsvektor, wobei eine Abfolge von Faltungsfiltern lokale Muster und breitere Motive erkennt — inspiriert von Entwürfen aus der Bilderkennung wie InceptionNet und AlexNet. Nach dieser separaten Verarbeitung werden die beiden Ströme zusammengeführt und durch mehrere vollverbundene Schichten geleitet, die eine einzige Wahrscheinlichkeit ausgeben: Handelt es sich bei diesem Wirkstoff–Krankheits-Paar um eine wahrscheinliche effektive Behandlung oder eher um eine schädliche Nebenwirkung? Um mit der Tatsache umzugehen, dass bekannte positive Paare viel seltener sind als negative, führen die Autor*innen eine gewichtete Verlustfunktion ein, die verpasste echte Behandlungen stärker bestraft und so die Leistung bei diesen schwer zu findenden Fällen verbessert. 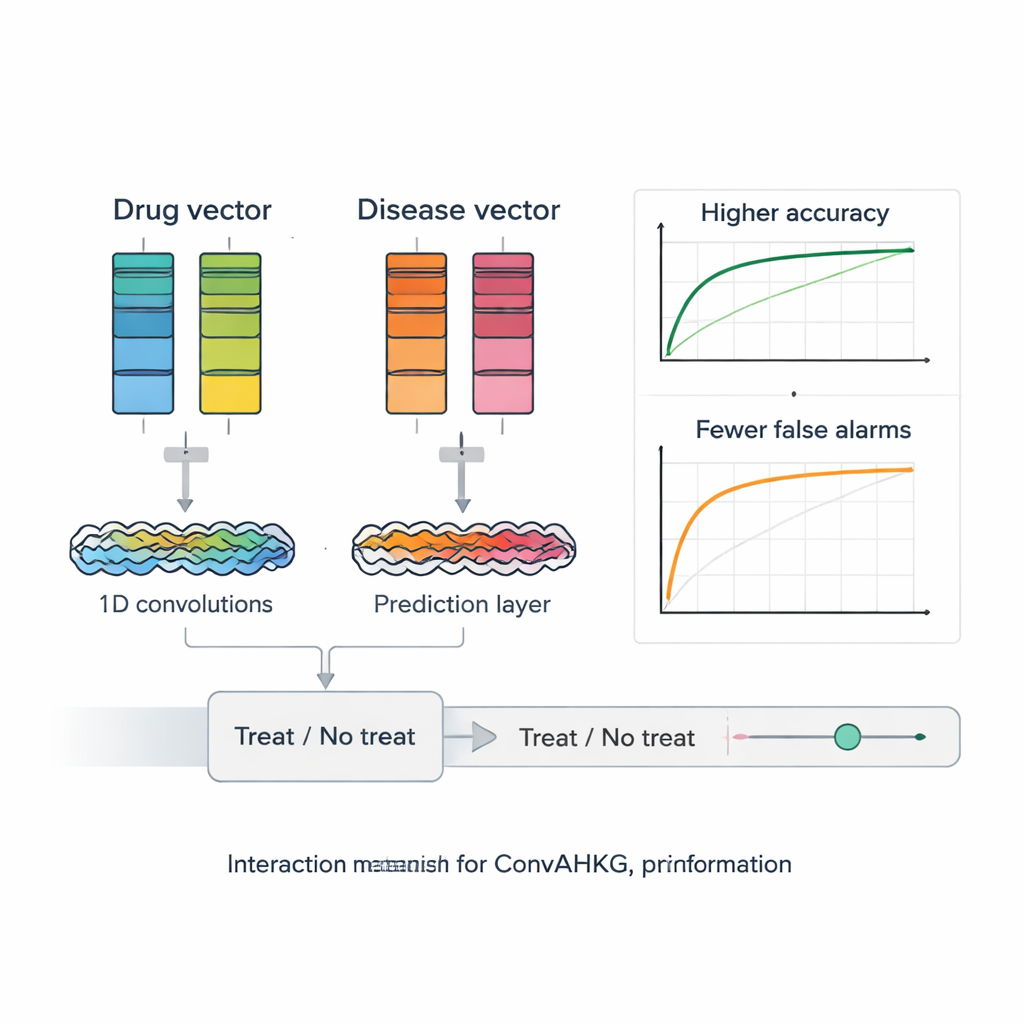
Bestehende Methoden übertreffen und Kandidaten für Krebs aufspüren
Die Forschenden testen ihr Framework rigoros gegen mehrere hochentwickelte Tools zur Wirkstoffumwidmung, die Matrixfaktorisierung, Graph Neural Networks und tiefe Autoencoder verwenden. ConvAHKG erreicht eine Fläche unter der ROC-Kurve von 0,9836 und eine Fläche unter der Precision–Recall-Kurve von 0,9686 und übertrifft damit alle konkurrierenden Ansätze auf demselben Benchmark-Datensatz. Anschließend wenden sie das Modell auf das nicht-kleinzellige Bronchialkarzinom an, die weltweit häufigste und tödlichste Form von Lungenkrebs. ConvAHKG hebt mehrere Medikamente hervor, die zuvor nicht als Behandlungen für diese Krankheit klassifiziert waren, darunter der Antikörper Trastuzumab, der das HER2-Protein anvisiert und für Lungenkrebs bereits unterstützende klinische Hinweise hat, sowie andere biologische Wirkstoffe und sogar das klassische Antibiotikum Benzylpenicillin. Docking-Simulationen deuten darauf hin, dass Benzylpenicillin möglicherweise stark an DNA und an Topoisomerase II alpha bindet, ein Enzym, das in diesen Tumoren oft erhöht ist, was auf einen möglichen antitumoralen Wirkmechanismus hindeutet, der nun Labortests rechtfertigt.
Warum das für Patient*innen wichtig ist
Einfach gesagt fungiert ConvAHKG wie ein hochinformierter Vermittler zwischen bestehenden Medikamenten und Krankheiten: Es nutzt eine detaillierte Karte biologischer Wirkungen und eine leistungsfähige Mustererkennungsmaschine, um vorherzusagen, welche alten Medikamente in neuen Indikationen wirksam sein könnten. Indem bereits sicher getestete Arzneimittel als wiederverwendbare Bausteine statt als Einzweckwerkzeuge betrachtet werden, könnte dieses Framework die Entdeckung von Therapien für Erkrankungen wie Lungenkrebs beschleunigen — insbesondere dort, wo die konventionelle Wirkstoffentwicklung zu langsam oder zu teuer ist. Zwar müssen die Vorhersagen noch sorgfältig experimentell und klinisch validiert werden, doch zeigt die Studie, dass die Kombination reichhaltigen biologischen Wissens mit moderner KI den Suchraum deutlich eingrenzen kann und potenziell lebensrettende Behandlungen schneller in Reichweite bringt.
Zitation: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Schlüsselwörter: Wirkstoffumwidmung, Wissensgraph, Tiefes Lernen, Lungenkrebs, Wirkstoffforschung