Clear Sky Science · de
Auswirkung von Sonikation und Proteaseinhibitoren auf die ELISA-Quantifizierung ausgewählter Proteine in Homogenaten von Rinder-Eutergewebe
Warum winzige Milchproteine wichtig sind
Hinter jedem Glas Milch steckt eine komplexe Fabrik im Euter der Kuh, in der Tausende von Proteinen zusammenarbeiten, um sichere, nahrhafte Milch zu produzieren. Wissenschaftler messen diese Proteine häufig, um den Zustand des Euters zu überwachen und Krankheiten wie Mastitis zu verstehen, eine kostspielige Infektion in Milchviehbeständen. Diese Studie stellt eine auf den ersten Blick einfache, aber praktisch wichtige Frage: Verfälscht die Art und Weise, wie wir Gewebeproben vor einem gängigen Labortest namens ELISA vorbereiten, stillschweigend die Ergebnisse, denen wir bei Entscheidungen vertrauen?
Wie Laborbehandlung das Ergebnis verändern kann
Um Proteine zu messen, müssen Forschende zunächst Gewebe aufbrechen und dessen Inhalt freisetzen. In dieser Arbeit untersuchten sie Eutergewebsstücke von 22 Kühen, die Hälfte gesund und die andere Hälfte mit einer Bakterienart infiziert, die Mastitis verursachen kann. Gemessen wurden drei wichtige Proteine im Zusammenhang mit Milchproduktion und Eutergesundheit: Alpha-Casein (ein Hauptmilchprotein), Lactoferrin (ein immunbezogenes Protein) und alkalische Phosphatase (ein Enzym, das mit Gewebeaktivität verbunden ist). Alle Messungen erfolgten mittels Sandwich-ELISA, einer weit verbreiteten Methode zum Nachweis sehr kleiner Mengen spezifischer Proteine. Der Unterschied war, dass dasselbe Gewebe vor der Analyse auf vier verschiedene Arten verarbeitet wurde, um zu prüfen, wie stark allein die Probenvorbereitung die Endwerte verändern kann.
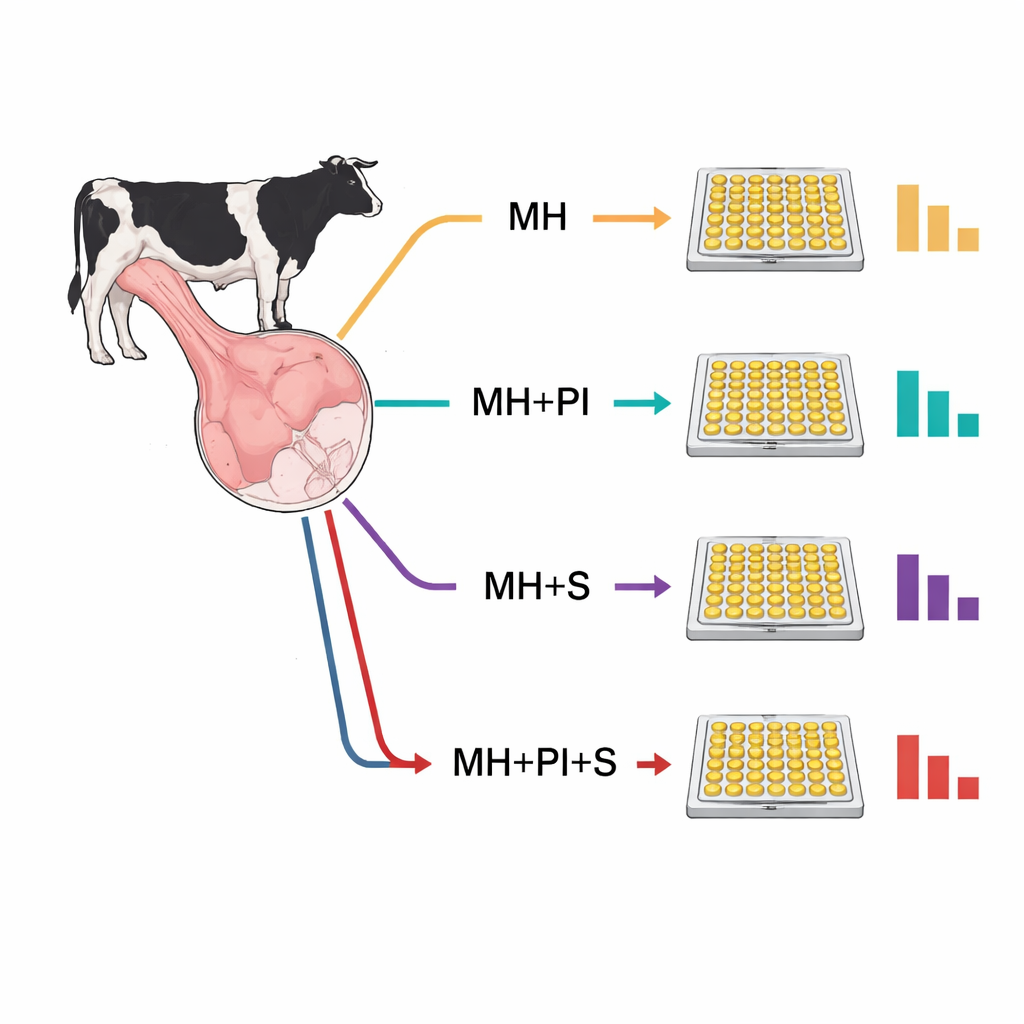
Vier Wege, dasselbe Gewebe zu behandeln
Das Team verglich einen einfachen mechanischen Homogenisierungsschritt—das physikalische Zerkleinern des Gewebes in einem Puffer—mit drei elaborierteren Varianten. Eine fügte einen Cocktail aus Proteaseinhibitoren hinzu, Chemikalien, die natürliche, beim Zellaufschluss freigesetzte Protein-spaltende Enzyme blockieren sollen. Eine andere setzte Sonikation ein, also kurze Impulse hochfrequenter Schallwellen, die Zellen zusätzlich zerstören. Die vierte Kombinationsvariante enthielt sowohl Proteaseinhibitoren als auch Sonikation. Prinzipiell sollten diese zusätzlichen Schritte Proteine schützen oder besser freisetzen. In der Praxis zeigten sie das Gegenteil: Jeder zusätzliche Schritt führte im Vergleich zur alleinigen Homogenisierung zu niedrigeren gemessenen Proteinwerten, und die Kombination aus Inhibitoren plus Sonikation ergab für alle drei Proteine die niedrigsten Messwerte.
Einige Proteine schrumpfen stärker als andere
Die Reduktionen waren nicht bei allen Proteinen gleich. Alpha-Casein erwies sich als am widerstandsfähigsten und zeigte bei zusätzlichen Verarbeitungsschritten den geringsten Rückgang. Lactoferrin und alkalische Phosphatase fielen dagegen deutlich stärker ab, insbesondere wenn Sonikation zum Einsatz kam. Dieses Muster deutet darauf hin, dass bestimmte Proteine anfälliger für physikalische Zerstörung, Hitze oder chemische Interferenzen sind, selbst wenn die Protokolle sorgfältig gekühlt und standardisiert werden. Der Gesundheitszustand der Kühe spielte ebenfalls eine Rolle, aber nur für Alpha-Casein: Euter mit Infektionen durch koagulasepositive Staphylokokken zeigten höhere Werte dieses Milchproteins, während Lactoferrin und alkalische Phosphatase zwischen gesunden und infizierten Tieren keine klaren Unterschiede aufwiesen. Entscheidend ist jedoch, dass Richtung und Ausmaß der verarbeitungsbedingten Abnahmen in beiden Gruppen ähnlich waren.
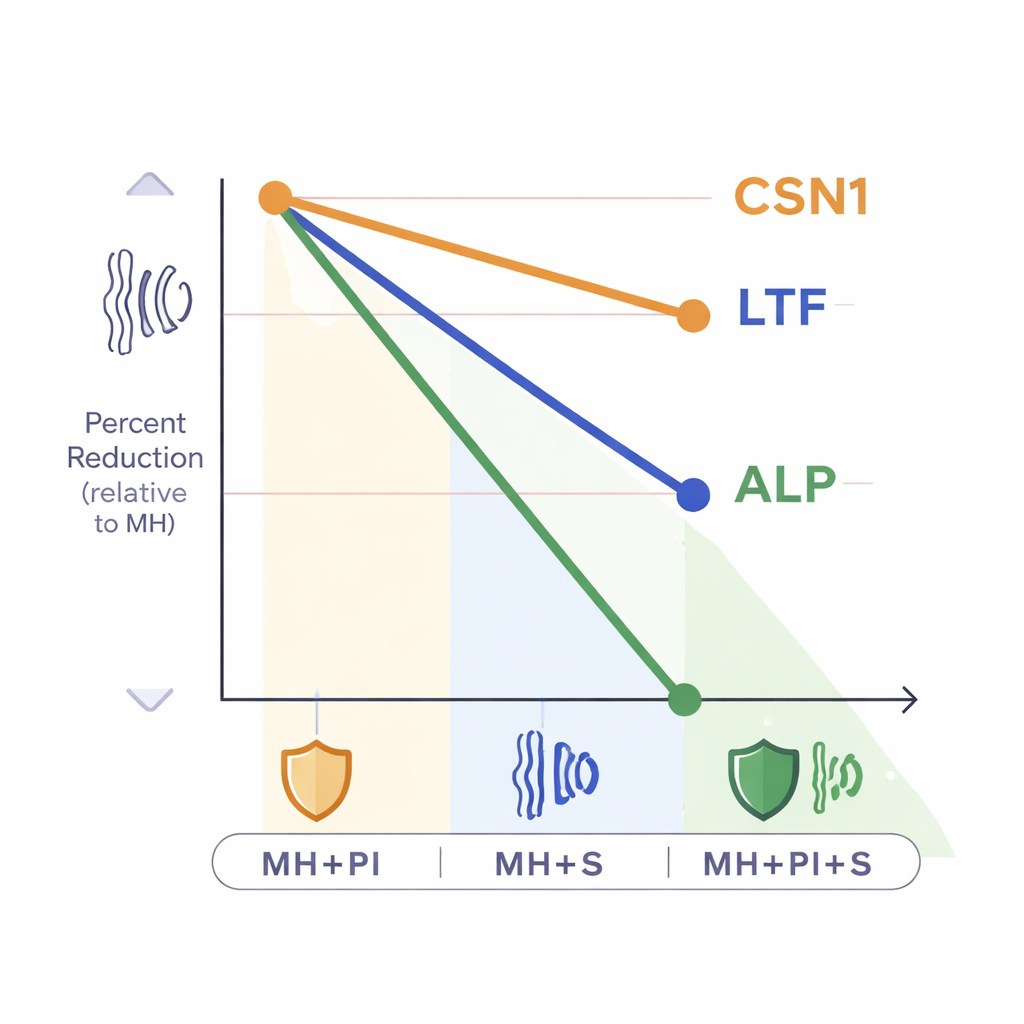
Wenn Schutzmaßnahmen nach hinten losgehen
Warum würden Schritte, die helfen sollen—wie Proteaseinhibitoren und Sonikation—zu niedrigeren gemessenen Proteinwerten führen? Die Studie klärte die genauen molekularen Gründe nicht vollständig auf, deutet aber auf mehrere Möglichkeiten hin. Sonikation kann Hitze und starke physikalische Kräfte erzeugen, die Proteine teilweise schädigen oder die spezifischen Erkennungsstellen verändern, die ELISA-Antikörper ansprechen. Proteaseinhibitoren mögen zwar natürliche Enzyme blockieren, können aber selbst durch unspezifische Bindung oder Beeinflussung der Nachweischemie in das Messverfahren eingreifen. Unabhängig vom Mechanismus ist die Botschaft klar: Diese weit empfohlenen Zusatzschritte können ELISA-Werte systematisch absenken, und sie tun dies in unterschiedlichem Ausmaß für verschiedene Proteine.
Was das für Milchforschung und Diagnostik bedeutet
Für Landwirte, Tierärzte und Lebensmittelüberwacher dienen ELISA-Ergebnisse als Grundlage für Entscheidungen über Tiergesundheit, Milchqualität und Verarbeitungssicherheit. Diese Studie zeigt, dass die Wahl eines komplexeren Vorbereitungsprotokolls Zielproteine deutlich knapper erscheinen lassen kann, als sie tatsächlich sind. Im Eutergewebe von Rindern ergab die einfachste Methode—allein die mechanische Homogenisierung—tatsächlich die höchsten und vergleichbarsten Proteinkonzentrationen. Für Nicht-Spezialisten lautet die Schlussfolgerung klar: Bevor man Proteinwerte als Hinweis auf Krankheit, Milchqualität oder Therapieerfolg interpretiert, müssen Forschende sehr sorgfältig standardisieren, wie Proben gehandhabt werden. Andernfalls könnten Unterschiede in Testergebnissen eher die Rauheit der Laborvorbereitungsschritte widerspiegeln als die tatsächliche Biologie im Inneren der Kuh.
Zitation: Szprynca, A., Czopowicz, M., Zalewska, M. et al. Effect of sonication and protease inhibitors on Elisa quantification of selected proteins in bovine udder tissue homogenates. Sci Rep 16, 7366 (2026). https://doi.org/10.1038/s41598-026-38653-x
Schlüsselwörter: ELISA-Probenvorbereitung, Rinder-Mastitis, Eutergewebe-Proteine, Auswirkungen der Sonikation, Proteaseinhibitoren