Clear Sky Science · de
Steigerung der Wirksamkeit photothermischer Therapie durch tartrazininduzierte optische Klarstellung biologischer Gewebe
Lichtbasierte Krebstherapien wirksamer machen
Ärzte setzen zunehmend Licht ein, um Tumore tief im Körper zu erwärmen und zu zerstören — eine Strategie, die als photothermische Therapie bekannt ist. Ein zentrales Problem bleibt jedoch bestehen: Unser Gewebe streut Licht, sodass nur ein Bruchteil der Energie das Ziel erreicht, während gesunde Bereiche überhitzt werden können. Diese Studie untersucht einen unerwarteten Helfer — ein gebräuchlicher gelber Lebensmittelfarbstoff namens Tartrazin — der Gewebe vorübergehend transparenter für Therapielicht machen und damit wärmebasierte Krebsbehandlungen sicherer und effektiver machen kann.
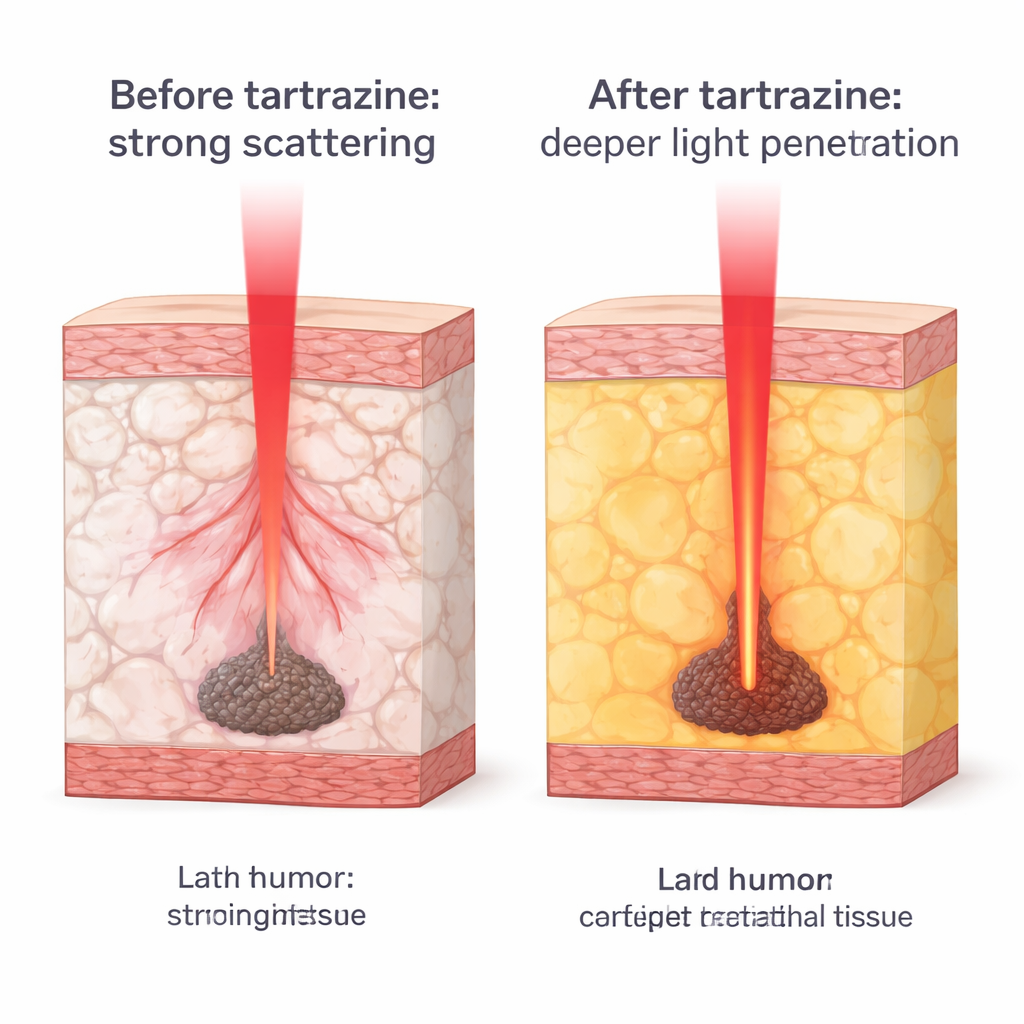
Ein Lebensmittelfarbstoff mit versteckter Fähigkeit
Tartrazin wird häufig zur Einfärbung von Lebensmitteln und Getränken verwendet und hat bei diätetischen Dosen eine gut dokumentierte Sicherheitsbilanz. Die Forschenden bauen auf jüngeren physikalischen Arbeiten auf, die zeigen, dass Tartrazin gelöst in Wasser das Verhalten von Licht in diesem Medium bei den nahinfraroten Wellenlängen verändert, die typischerweise in medizinischen Behandlungen genutzt werden. Anstatt Gewebe wie viele traditionelle „Klarungsmittel“ zu zerstören oder zu dehydrieren, passt Tartrazin subtil an, wie Licht in den wässrigen Räumen zwischen Fetten und Proteinen gebrochen wird. Indem es die optischen Eigenschaften dieser Komponenten einander ähnlicher macht, reduziert der Farbstoff die Menge an Licht, die umhergeworfen und gestreut wird.
Wolkiges Gewebe in ein klareres Fenster verwandeln
Um diese Idee zu testen, stellte das Team zunächst kontrollierte „Gewebephantome“ her — Gelblöcke mit winzigen Kunststoffkügelchen, die das Streuverhalten echten Gewebes nachahmen. Mithilfe von Computersimulationen und Experimenten zeigten sie, dass das Hinzufügen von Tartrazin die Streuung um bis zu etwa zwei Drittel reduzieren kann, besonders in Proben mit größeren, dicht gepackten Partikeln, die echten biologischen Strukturen ähneln. Bei sorgfältig gewählten Konzentrationen erhöhte Tartrazin die Durchlässigkeit des Therapielichts durch diese Phantome, ohne sie durch die eigene Farbe des Farbstoffs zu stark zu verdunkeln. Der optimale Bereich lag bei etwa 0,3–0,5 Mol pro Liter Farbstoff, in dem das Verhältnis von verringerter Streuung zu zusätzlicher Absorption am günstigsten war.
Von Modellgelen zu echtem Tiergewebe
Die Forschenden gingen dann von künstlichen Gelen zu Schnitten aus Hühnerfleisch über, die lebendem Gewebe näher kommen. Nachdem sie die Proben in Tartrazin eingeweicht hatten, maßen sie, wie viel sichtbares und nahinfrarotes Licht hindurchtreten konnte. Die behandelten Gewebe wurden deutlich transparenter und ließen bei bestimmten Wellenlängen bis zu etwa 1,7-fach mehr Licht durch. Wichtig war, dass diese Klarstellung reversibel war: Sobald die Tartrazin-getränkten Gewebe zurück in reines Wasser gelegt wurden, kehrten sie allmählich in ihren ursprünglichen, undurchsichtigeren Zustand zurück. Bildtests zeigten, dass feine Muster hinter dem behandelten Gewebe schärfer und mit höherem Kontrast erschienen, was demonstriert, dass Licht geradliniger statt in alle Richtungen gestreut durchging.
Mehr Wärme genau dort abliefern, wo sie gebraucht wird
Bessere Lichtdurchdringung ist nur relevant, wenn sie zu besseren Behandlungsergebnissen führt. Um das zu überprüfen, baute das Team ein realistisches Tumormodell mit 3D-gedruckten Gerüsten, die mit humanen Glioblastom-(Hirntumor-)Zellen besetzt waren, und platzierte dann tartrazin-behandelte oder unbehandelte „Gewebeschichten“ zwischen einem nahinfraroten Laser und den Tumormodellen. Mit Tartrazin auf dem Weg erreichte mehr Laserenergie die Tumorregion und erhöhte die Temperaturen um bis zu etwa 10 Grad Celsius gegenüber unbehandelten Versuchsaufbauten. Diese stärkere, gleichmäßigere Erwärmung verschob das Ergebnis von moderaten Effekten zu einer starken Tumorzellabtötung. Unter Tartrazin-Behandlung führten selbst mittlere Laserleistungen zu deutlichen Anstiegen an Krebszelltod, vermehrter programmierter Zelltod (Apoptose) und einem Anstieg schädigender reaktiver Sauerstoffmoleküle — alles Merkmale einer effektiven photothermischen Therapie.
Warum das für zukünftige Behandlungen wichtig ist
Insgesamt legt die Studie nahe, dass das vorübergehende „Klarstellen“ von Gewebe mit einem lebensmittelsicheren Farbstoff lichtbasierte Krebstherapien unterstützen könnte, indem tiefere Ziele mit geringeren Laserleistungen, kürzeren Behandlungszeiten oder beidem erreicht werden. Da Tartrazin hauptsächlich wirkt, indem es sanft die Lichtausbreitung im Gewebe anpasst — statt es chemisch zu schädigen — sind seine Effekte reversibel und potenziell sicherer als viele vorhandene Klarungsmittel. Zwar sind weitere Tier- und Sicherheitsstudien erforderlich, doch deutet diese Arbeit auf einen einfachen, kostengünstigen Weg hin, den Körper von einem lichtstreuenden Hindernis in einen kooperativeren Partner zu verwandeln und so die photothermische Therapie präziser und schonender für das umliegende gesunde Gewebe zu machen.
Zitation: Minopoli, A., Evangelista, D., Marras, M. et al. Enhancing photothermal therapy effectiveness via tartrazine-induced optical clearing of biological tissues. Sci Rep 16, 7553 (2026). https://doi.org/10.1038/s41598-026-38616-2
Schlüsselwörter: photothermische Therapie, Tartrazin, optische Klarstellung, lichtbasierte Krebstherapie, Gewebetransparenz