Clear Sky Science · de
DNMT3A p.R882C getriebene Proliferation und anti-apoptotische Effekte in Pankreaskarzinomzellen
Warum diese Forschung für Bauchspeicheldrüsenkrebs wichtig ist
Bauchspeicheldrüsenkrebs ist dafür bekannt, spät entdeckt zu werden, schnell zu streuen und schlecht auf Therapien anzusprechen. Die meisten Patientinnen und Patienten erhalten die Diagnose Pankreas duktales Adenokarzinom (PDAC), eine besonders aggressive Form der Erkrankung. Diese Studie betrachtet eine winzige Veränderung in einem einzelnen Gen, DNMT3A, und stellt eine große Frage: Kann diese subtile Alteration erklären, warum manche Pankreastumoren schneller wachsen und dem Zelltod widerstehen? Das Verständnis solcher Veränderungen könnte den Weg für frühere Diagnosen und präzisere, zielgerichtete Therapien ebnen.
Ein genauerer Blick auf einen tödlichen Krebs
PDAC macht mehr als 90 % der Pankreaskarzinome aus und hat eine Fünfjahresüberlebensrate von unter 13 %. Häufig wird er durch bekannte Krebsgene wie KRAS und TP53 angetrieben, doch profitieren viele Patientinnen und Patienten weiterhin nicht von aktuellen zielgerichteten Therapien. Neuere Arbeiten deuten darauf hin, dass nicht nur Genmutationen, sondern auch „epigenetische“ Veränderungen — chemische Markierungen der DNA, die steuern, welche Gene ein- oder ausgeschaltet werden — eine Schlüsselrolle spielen. DNMT3A ist eines der zentralen Enzyme, das diese chemischen Markierungen setzt, und Defekte in diesem Gen wurden bereits mit Blutkrebserkrankungen wie der akuten myeloischen Leukämie in Verbindung gebracht.
Auf der Suche nach gefährlichen DNA-Veränderungen
Die Forschenden sammelten Tumorproben und angrenzendes nicht‑krebsartiges Gewebe von drei Patientinnen bzw. Patienten mit mäßig bis schlecht differenziertem PDAC. Sie verwendeten Whole‑Exome‑Sequencing, eine Technik, die alle protein‑kodierenden Regionen des Genoms liest, und wandten strenge Computerfilter an, um harmlose DNA‑Varianten von solchen zu trennen, die das Zellverhalten wahrscheinlich schädigen. Aus Hunderten von Veränderungen reduzierten sie die Liste auf 68 hochriskante Alterationen. Unter diesen fiel eine seltene Variante in DNMT3A, bekannt als p.R882C, auf, weil sie in großen Populationsdatenbanken nahezu nicht vorkommt und von mehreren Vorhersagewerkzeugen konsistent als schädlich eingestuft wurde.
Was diese Mutation in Zellen bewirkt
DNMT3A ist ein 912 Aminosäuren langes Protein, das hilft, DNA‑Methylierungsmuster zu etablieren — chemische Tags, die wie An‑ oder Ausschalter für Gene wirken. Die Veränderung p.R882C liegt in einer entscheidenden Funktionsregion von DNMT3A, wo sie die Aktivität des Enzyms stören könnte. Mittels 3D‑Computermodellen stellte das Team fest, dass sich die Gesamtstruktur des Proteins nicht dramatisch veränderte, was darauf hindeutet, dass das Problem eher in der Funktionsweise des Enzyms als in dessen Faltung liegen könnte. Um dies zu testen, erzeugten sie Pankreaskarzinomzelllinien (PANC‑1 und PaTu 8988t), die entweder normales DNMT3A oder die p.R882C‑Variante produzierten, und verglichen diese mit Zellen, die ein leeres Kontrollvektor trugen.
Schnelleres Wachstum, mehr Bewegung, weniger Zelltod
Überraschenderweise veränderte die p.R882C‑Mutation nicht die Menge an DNMT3A‑RNA oder ‑Protein; die Enzymmenge blieb in etwa gleich. Ihre Anwesenheit hatte jedoch auffällige Effekte auf das Zellverhalten. In Kolonie‑Bildungs‑ und Wachstumsassays bildeten Zellen mit dem mutierten DNMT3A mehr Kolonien und zeigten stärkere Wachstumssignale als jene mit der normalen Variante. Wundheilungs‑ und Transwell‑Tests, die messen, wie schnell Zellen sich bewegen, zeigten, dass die mutierten Zellen schneller migrierten. Bei der Untersuchung des programmierten Zelltods (Apoptose) mittels Durchflusszytometrie wiesen Zellen mit der p.R882C‑Mutation deutlich weniger sterbende Zellen auf, sowohl in frühen als auch in späten Apoptosephasen, was einen deutlichen Überlebensvorteil anzeigt.
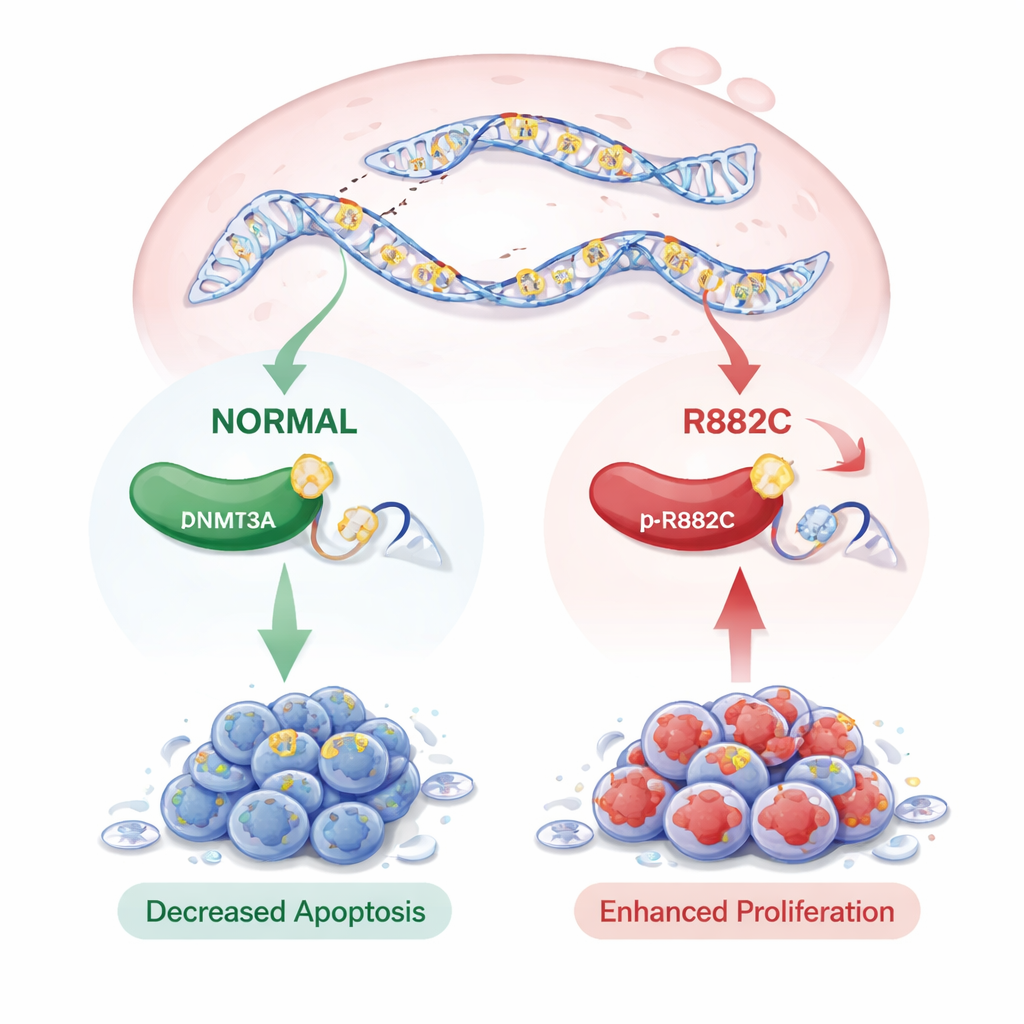
Was das für die zukünftige Versorgung bedeuten könnte
In der Zusammenführung dieser Ergebnisse legt die Studie nahe, dass die seltene DNMT3A p.R882C‑Mutation Pankreaskarzinomzellen dabei unterstützt, schneller zu wachsen, sich leichter zu bewegen und der Selbstzerstörung zu widerstehen — Eigenschaften, die zum Voranschreiten des Krebses beitragen können. Obwohl die Mutation die DNMT3A‑Menge nicht erhöht, verändert sie vermutlich die Aktivität des Enzyms und damit das Muster der DNA‑Markierungen im Genom, ähnlich wie in bestimmten Blutkrebserkrankungen beobachtet. Die Autorinnen und Autoren weisen darauf hin, dass diese Veränderung selten ist und in öffentlichen Datensätzen noch keine klaren Zusammenhänge mit dem Überleben von Patientinnen und Patienten zeigte, zum Teil weil verfügbare Studien klein sind und DNMT3A oft nicht erfasst wird. Dennoch hebt das Auffinden dieser Mutation in PDAC einen potenziell wichtigen neuen Akteur bei der Krankheit hervor und öffnet die Möglichkeit, dass DNMT3A p.R882C künftig als Risikomarker oder als Ziel für maßgeschneiderte Therapien dienen könnte.
Zitation: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
Schlüsselwörter: Pankreaskarzinom, DNMT3A-Mutation, PDAC, DNA-Methylierung, zielgerichtete Therapie