Clear Sky Science · de
Genomeditierung in verschiedenen Dictyostelia-Arten ermöglicht vergleichende funktionelle Genetik sozialer Amöben
Wie Einzelzellen zusammenarbeiten
Meist leben Amöben als winzige Einzelgänger im Boden und ernähren sich von Bakterien. Einige von ihnen, die sogenannten sozialen Amöben, können sich jedoch plötzlich zu einem vielzelligen Körper mit einer primitiven „Spitze“ und einem „Stiel“ zusammenschließen. Dieser Formwandel gibt Forschern einen seltenen Einblick darin, wie einfache Zellen Kooperation und Spezialisierung erlernen – Schlüsselereignisse in der Entstehung komplexen Lebens. Die neue Studie beschreibt ein Genom‑Editier‑Werkzeug, das es Forschern endlich erlaubt, diese Verhaltensweisen nicht nur in einem Laborfavoriten, sondern über mehrere weit entfernte Amöbenarten hinweg zu untersuchen.
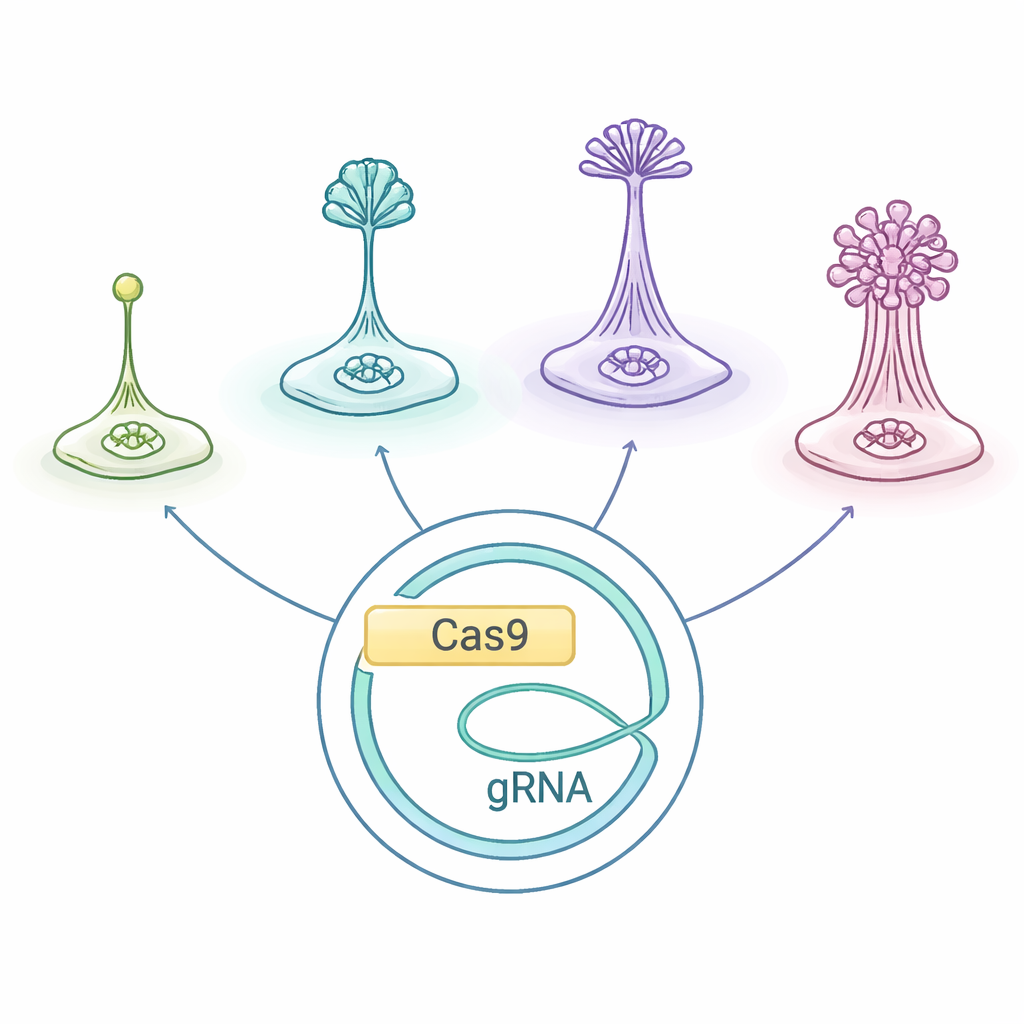
Kleine Lebewesen mit großem Sozialleben
Die sozialen Amöben, zusammengefasst als Dictyostelia, leben als Einzellen, solange Nahrung reichlich vorhanden ist. Bei Nahrungsmangel senden sie chemische Notrufe aus und kriechen aufeinander zu, wobei sie sich zu einem Hügel zusammenschließen, der ein miniaturisiertes „Fruchtkörperchen“ bildet: eine Säule aus aufopfernden Stielzellen, die widerstandsfähige Sporen in die Luft tragen. Verschiedene Dictyostelia‑Linien bauen diese Strukturen auf unterschiedliche Weise und mit unterschiedlichen Zelltypen, was sie zu einem natürlichen Labor macht, um zu fragen, wie vielzellige Körper und Arbeitsteilung entstehen.
Eine Modellart reichte nicht aus
Bisher konzentrierte sich nahezu alle molekulare Arbeit auf eine einzige Art, Dictyostelium discoideum, weil sich ihre Gene relativ leicht manipulieren lassen. Mehr als hundert andere bekannte Arten – einige davon Vertreter früherer Verzweigungen im Dictyostelia‑Stammbaum – blieben weitgehend unerforscht. Diese übersehenen Arten haben unterschiedliche Lebensgeschichten, Signalwege und Körperpläne. Um zu verstehen, wie Multizellularität sich im Laufe der Zeit verändert hat, müssen Wissenschaftler dieselben Gene in vielen dieser Arten manipulieren und die Ergebnisse nebeneinander vergleichen.
CRISPR für eine vielfältige Amöbenfamilie
Die Forschenden passten ein für D. discoideum optimiertes CRISPR/Cas9‑System an und prüften, ob es im gesamten Dictyostelia‑Stammbaum funktioniert, einschließlich früh abgespaltener und stärker abgeleiteter Arten. Sie verwendeten ein Plasmid – ein zusätzliches zirkuläres DNA‑Stück –, das die Anweisungen für die Cas9‑„Molekularschere“, die Guide‑RNA, die Cas9 zu einem ausgewählten Gen führt, und ein Medikamentresistenz‑Marker enthält. Das Einbringen dieses Plasmids in verschiedene Amöben erlaubte dem Team, zwei gut untersuchte Gene, stlA und pkaC, zu zerschneiden, die für die Signale wichtig sind, die Aggregation und die richtige Bildung des Fruchtkörpers koordinieren. Bei der Bodenamöbe Polysphondylium violaceum erzeugte diese Strategie zuverlässig Mutanten mit klaren Entwicklungsdefekten und zeigte damit, dass das übernommene System außerhalb des üblichen Modells funktionieren kann.
Gene über Arten hinweg testen
Als Nächstes untersuchte das Team weiter entfernte Verwandte, darunter Heterostelium pallidum aus Gruppe 2 und Cavenderia fasciculata aus Gruppe 1 – Linien, die sich früher in der Evolution abgespalten haben. Mit demselben Plasmiddesign störten sie das pkaC‑Gen in beiden Arten und stellten fest, dass die Mutanten nicht aggregierten und keine normalen Fruchtkörper bildeten, ähnlich den schwerwiegenden Defekten bei D. discoideum. Da die durch diese Methode erzeugten CRISPR‑Mutationen keine sperrigen Selektionskassetten hinterlassen, waren die resultierenden Stämme „markierungsfrei“. Dadurch war es einfach, eine Version des Gens aus D. discoideum wieder einzuführen und zu testen, ob sie die lokale Version ersetzen kann. In allen Fällen konnte das fremde pkaC den frühen Aggregationsschritt retten, aber nicht die spätere Ausformung eines reifen Fruchtkörpers – ein Hinweis darauf, dass das grundlegende Signalisierungs‑Werkzeug gemeinsam ist, während die fein abgestimmte Steuerung von Timing und Position artspezifisch evolviert ist.
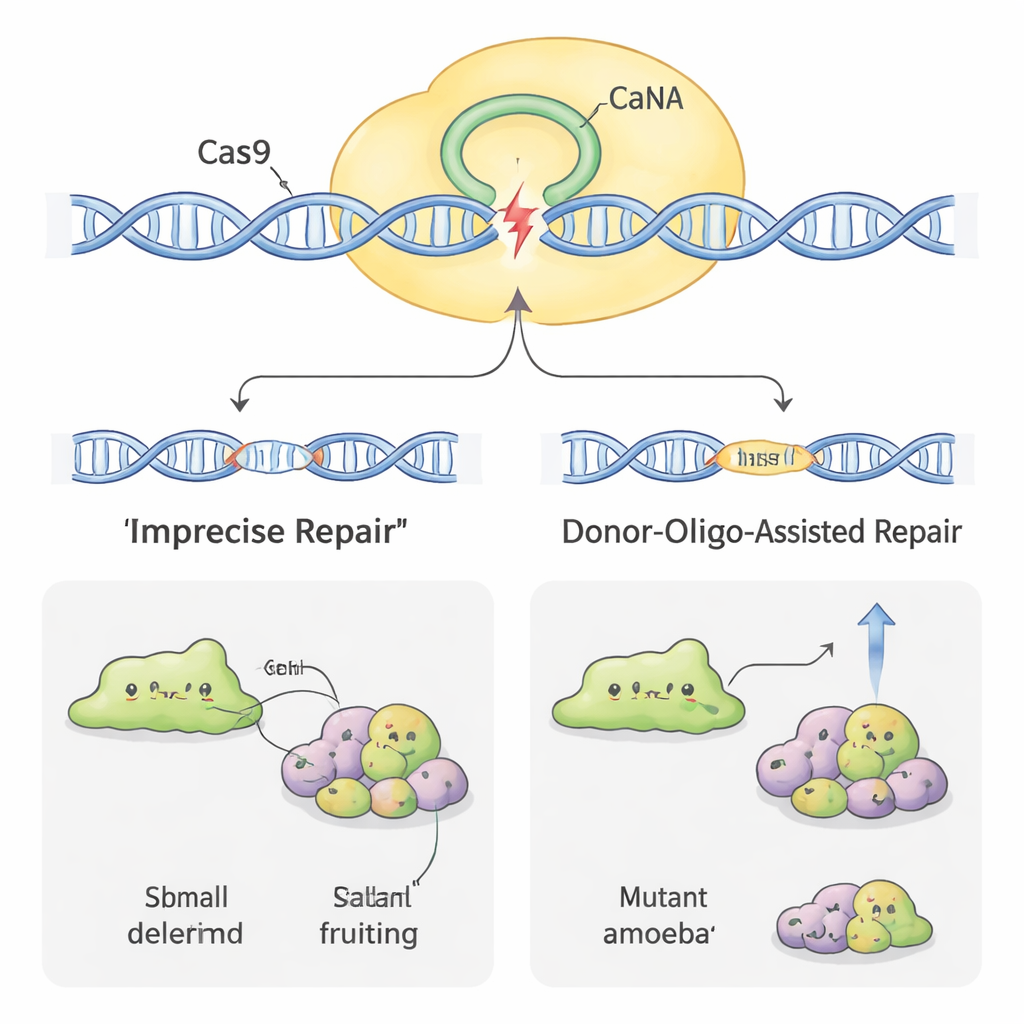
Effizienteres Editieren
Nicht alle Amöben ließen sich gleichermaßen leicht genomisch editieren. Bei einigen Arten, etwa H. pallidum, war die Anfangsrate des Erfolgs sehr niedrig. Um die Effizienz zu steigern, griffen die Wissenschaftler auf einen weiteren Trick zurück: Sie fügten kurze „Donor“‑DNA‑Stücke zusammen mit dem CRISPR‑Plasmid hinzu. Diese Donoren tragen einen kleinen Tag und ein Stoppsignal, flankiert von kurzen Regionen, die zum Zielgen passen. Wenn die Zelle den Cas9‑Schnitt unter Verwendung des Donors als Vorlage repariert, wird das Gen zuverlässig auf eine erkennbare Weise gebrochen. Bei D. discoideum erhöhte dies den Anteil defekter Klone und ermöglichte es dem Team sogar, Mutanten ohne kontinuierliche Medikamentenselektion zu gewinnen. Beim störrischeren H. pallidum erhöhte die Kombination von Donor‑DNA mit einigen Tagen Medikamentenbehandlung die Mutationsraten fast um eine Größenordnung und machte zuvor seltene Ereignisse nahezu routinemäßig.
Ein Fenster in die Ursprünge der Komplexität öffnen
Für Nicht‑Spezialisten mögen die Details zu Plasmiddesigns und Reparaturvorlagen technisch klingen, doch der Gewinn ist weitreichend: ein flexibles CRISPR‑Werkzeug, das in mehreren Zweigen des Stammbaums sozialer Amöben funktioniert. Damit können Wissenschaftler nun vergleichen, wie dasselbe Gen die Entwicklung in verschiedenen Arten beeinflusst und wie subtile Änderungen in Genregulation oder Proteinstruktur zur Entstehung neuer Zelltypen und Körperpläne beitragen. Mit anderen Worten: Diese Arbeit stattet Forschende mit den genetischen Werkzeugen aus, um – in lebenden Details – zu beobachten, wie die Evolution einzelne Zellen umgestaltet hat, um kooperative vielzellige Gesellschaften zu bilden.
Zitation: Oishi, S., Doi, S., Sekida, T. et al. Genome editing across Dictyostelia species enables comparative functional genetics of social amoebas. Sci Rep 16, 7457 (2026). https://doi.org/10.1038/s41598-026-38605-5
Schlüsselwörter: soziale Amöben, CRISPR-Genomeditierung, Evolution der Multizellularität, Dictyostelium, Zell‑Differenzierung