Clear Sky Science · de
PLOD2 fördert Proliferation, Migration und Invasion von kolorektalen Krebszellen über den PI3K‑AKT‑GSK3β‑Signalweg
Warum die Nachbarschaft um einen Tumor wichtig ist
Kolorektales Karzinom zählt zu den weltweit häufigsten Krebserkrankungen, und viele Menschen werden erst in fortgeschrittenen Stadien diagnostiziert. Diese Studie blickt über die Krebszellen selbst hinaus und untersucht ihre umgebende „Nachbarschaft“ aus unterstützendem Gewebe. Die Forschenden konzentrieren sich auf ein wenig bekanntes Enzym namens PLOD2 und zeigen, wie es kolorektalen Tumoren durch Veränderungen der Gewebeumgebung und durch Beeinflussung zentraler Wachstumssignale in den Zellen beim Wachsen und Ausbreiten hilft.
Ein verborgener Baumeister im Gerüst des Tumors
Unsere Organe werden von einem Netz aus Proteinen getragen, der extrazellulären Matrix, wobei Kollagen die wichtigste Strukturkomponente bildet. PLOD2 ist ein Enzym, das Kollagen chemisch modifiziert und so dessen Quervernetzung und Bildung starrer Fasern fördert. Das Team analysierte große genetische und proteomische Datenbestände und untersuchte anschließend Gewebeproben von 75 Patienten. Dabei zeigte sich, dass die PLOD2‑Spiegel in kolorektalem Tumorgewebe deutlich höher waren als im angrenzenden normalen Gewebe. Hohe PLOD2‑Level korrelierten mit fortgeschritteneren Tumoren, Lymphknotenbefall und perineuraler Invasion, und Patienten mit PLOD2‑reichen Tumoren hatten tendenziell eine kürzere Überlebenszeit. Diese Befunde machen PLOD2 zu einem starken Kandidaten als Marker für aggressivere Erkrankungsformen.
Wie PLOD2 Krebszellen aggressiver macht
Um über Korrelationen in Patientenproben hinauszukommen, veränderten die Forschenden kolorektale Krebszelllinien im Labor genetisch. In einer Zelllinie erhöhten sie die PLOD2‑Produktion; in einer anderen schalteten sie sie aus. Zellen mit erhöhtem PLOD2 wuchsen schneller, bildeten mehr Kolonien und schlossen künstliche „Wunden“ in Kultur schneller, was erhöhte Beweglichkeit zeigte. Sie wanderten außerdem leichter durch poröse Membranen und invasierten eher durch ein Gel, das Gewebebarrieren nachahmt, als Kontrollzellen. Bei stillgelegtem PLOD2 schwächten sich all diese Eigenschaften ab. Zusammen zeigen diese Experimente, dass PLOD2 das Wachstum, die Migration und die Invasion von Krebszellen aktiv antreibt, statt nur ein Beifahrer zu sein.
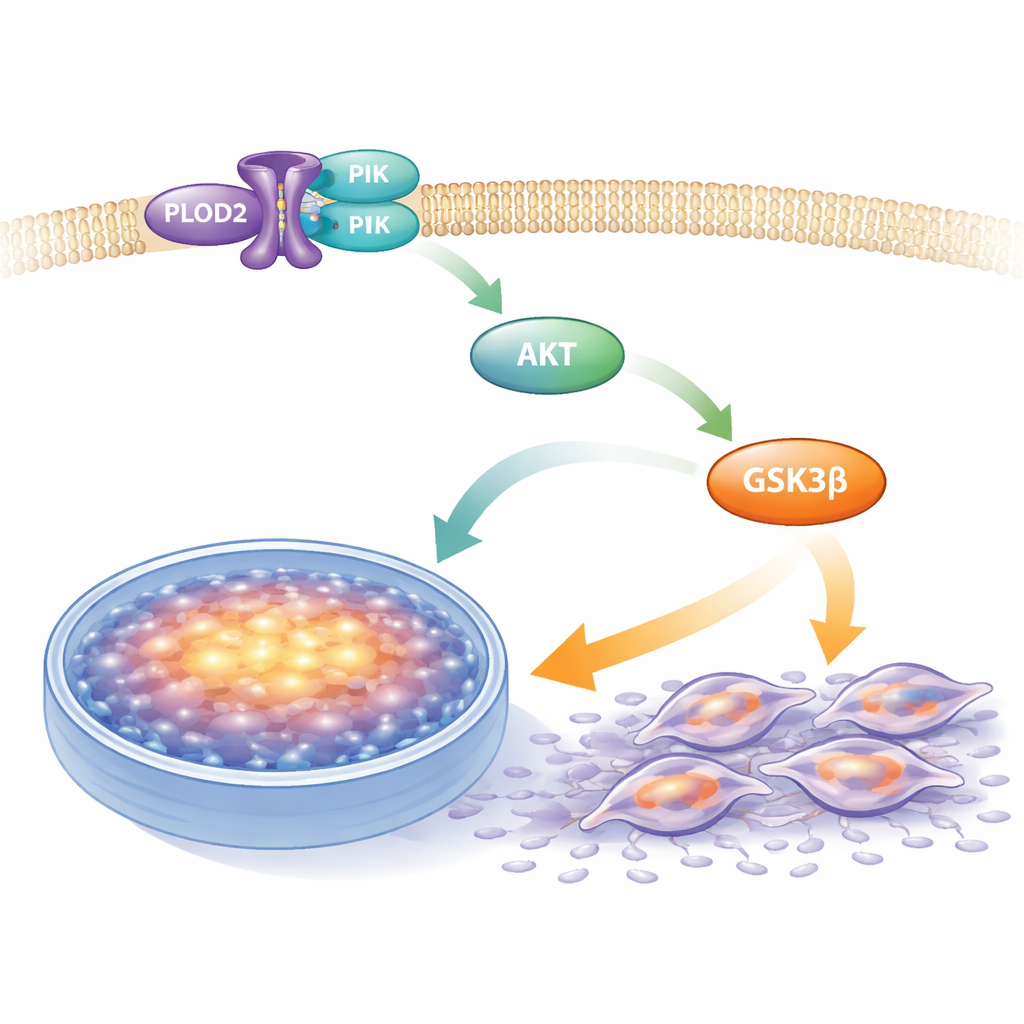
Ein krebsförderndes Signalsystem einschalten
Innerhalb von Krebszellen werden viele Vorgänge durch vernetzte Signalwege gesteuert. Eine zentrale Kaskade, die allgemein als PI3K–AKT–GSK3β‑Weg bekannt ist, unterstützt Überleben, Zellteilung und Anpassung des Stoffwechsels. Mittels Datenanalyse und biochemischer Tests fanden die Forschenden heraus, dass PLOD2 eng mit diesem Weg verknüpft ist. Sie zeigten, dass PLOD2 physisch an PI3K bindet, das als „Startenzym“ der Kette gilt. Bei hohen PLOD2‑Spiegeln stiegen die aktivierten (phosphorylierten) Formen von PI3K, AKT und GSK3β an, obwohl die Gesamtmengen der Proteine unverändert blieben. Wurde PLOD2 reduziert, nahm die Aktivierung dieses Weges ab, was darauf hindeutet, dass PLOD2 wie ein Schalter wirkt, der dieses Wachstums‑ und Beweglichkeitssystem einschaltet.
Den Signalweg mit chemischen Werkzeugen prüfen
Um zu bestätigen, dass die schädlichen Effekte von PLOD2 von diesem Signalweg abhängen, setzten die Forschenden Wirkstoffe ein, die PI3K entweder blockieren oder aktivieren. In Zellen mit PLOD2‑Überproduktion dämpfte ein PI3K‑Inhibitor die Aktivierung von AKT und GSK3β und verlangsamte Zellwachstum, -bewegung und -invasion. In Zellen, in denen PLOD2 ausgeschaltet war, stellte ein PI3K‑Aktivator die Signalaktivität wieder her und rettete teilweise die Fähigkeit der Zellen zur Proliferation und Migration. Obwohl die Wiederherstellung nicht vollständig war — was nahelegt, dass PLOD2 auch andere Wege beeinflussen könnte — stützen diese Experimente stark die Idee, dass PLOD2 die Malignität vornehmlich durch Anknüpfung an die PI3K–AKT–GSK3β‑Achse fördert.
Was das für Patienten bedeutet
Für Nicht‑Spezialisten lassen sich diese molekularen Details auf eine einfache Kernbotschaft reduzieren: PLOD2 hilft kolorektalen Krebszellen, ihre Umgebung zu verhärten und umzubauen, und tritt gleichzeitig als Gaspedal für wichtige interne Wachstumsschaltungen in Erscheinung. Durch beides zusammen macht es Tumoren wahrscheinlicher, aggressiv zu wachsen und sich auszubreiten. Die Studie legt nahe, dass die Messung von PLOD2 helfen könnte, Hochrisikopatienten zu identifizieren, und dass Wirkstoffe, die direkt PLOD2 angreifen — oder die Signalkette, die es auslöst — eines Tages Teil gezielterer Therapien gegen kolorektalen Krebs werden könnten. Weitere Arbeiten in Tiermodellen und größeren Patientengruppen sind erforderlich, aber PLOD2 tritt nun als vielversprechender neuer Ansatzpunkt bei einer schwer zu behandelnden Krankheit hervor.
Zitation: Fang, H., Zheng, J., Ren, S. et al. PLOD2 promotes proliferation, migration and invasion of colorectal cancer cells via PI3K-AKT-GSK3β signaling pathway. Sci Rep 16, 8118 (2026). https://doi.org/10.1038/s41598-026-38593-6
Schlüsselwörter: kolorektales Karzinom, PLOD2, tumormikroumgebung, PI3K AKT Signalgebung, Krebsmetastasen