Clear Sky Science · de
Isofluran verschärft bestehende Proteotoxizität bei erwachsenen Nematoden durch Unterdrückung der mitochondrialen Fitness
Warum das für Operationen und Gehirngesundheit wichtig ist
Viele ältere Menschen erleben nach Operationen Verwirrung und Gedächtnisprobleme, ein Zustand, der als postoperatives Delir bekannt ist. Diese Studie stellt eine einfache, aber drängende Frage: Kann das Narkosegas, das Patienten in Bewusstlosigkeit hält, bereits anfällige Gehirne weiter schwächen? Anhand winziger Würmer als Modell für den Menschen zeigen die Forscher, dass ein weit verbreitetes Narkotikum, Isofluran, bestehende Proteinschäden in Nerven- und Muskelzellen verschlimmern kann, indem es die Gesundheit der Mitochondrien — den Energieerzeugern der Zelle — untergräbt. Die Ergebnisse deuten auf neue Ansätze hin, wie gefährdete Patienten vor dem Eingriff geschützt werden könnten.
Ein Narkotikum, das nur zuschlägt, wenn Zellen bereits belastet sind
Nicht alle Gehirne reagieren gleich auf Anästhesie. Das Team arbeitete mit dem Nematoden C. elegans, einem mikroskopisch kleinen Wurm, dessen Biologie viele Kernmechanismen mit dem Menschen teilt. Einige Würmer waren normal, andere wurden so verändert, dass sie klebrige, krankheitsbezogene Proteine produzieren, die zum Verklumpen neigen und Zustände wie die Huntington‑Krankheit nachahmen. Wenn normale Würmer Isofluran für einige Stunden einatmeten, blieben ihre Beweglichkeit und das Proteingleichgewicht noch Tage später weitgehend erhalten. Bei Würmern, die bereits durch verklumpende Proteine belastet waren, führte dieselbe Narkoseeinwirkung jedoch zu einem klaren und anhaltenden Rückgang der Beweglichkeit — ein Hinweis darauf, dass ihre Zellen Schwierigkeiten hatten, damit fertigzuwerden. Anders gesagt wirkte Isofluran wie ein zusätzlicher Stoß auf ein System, das schon kurz vor dem Zusammenbruch stand.
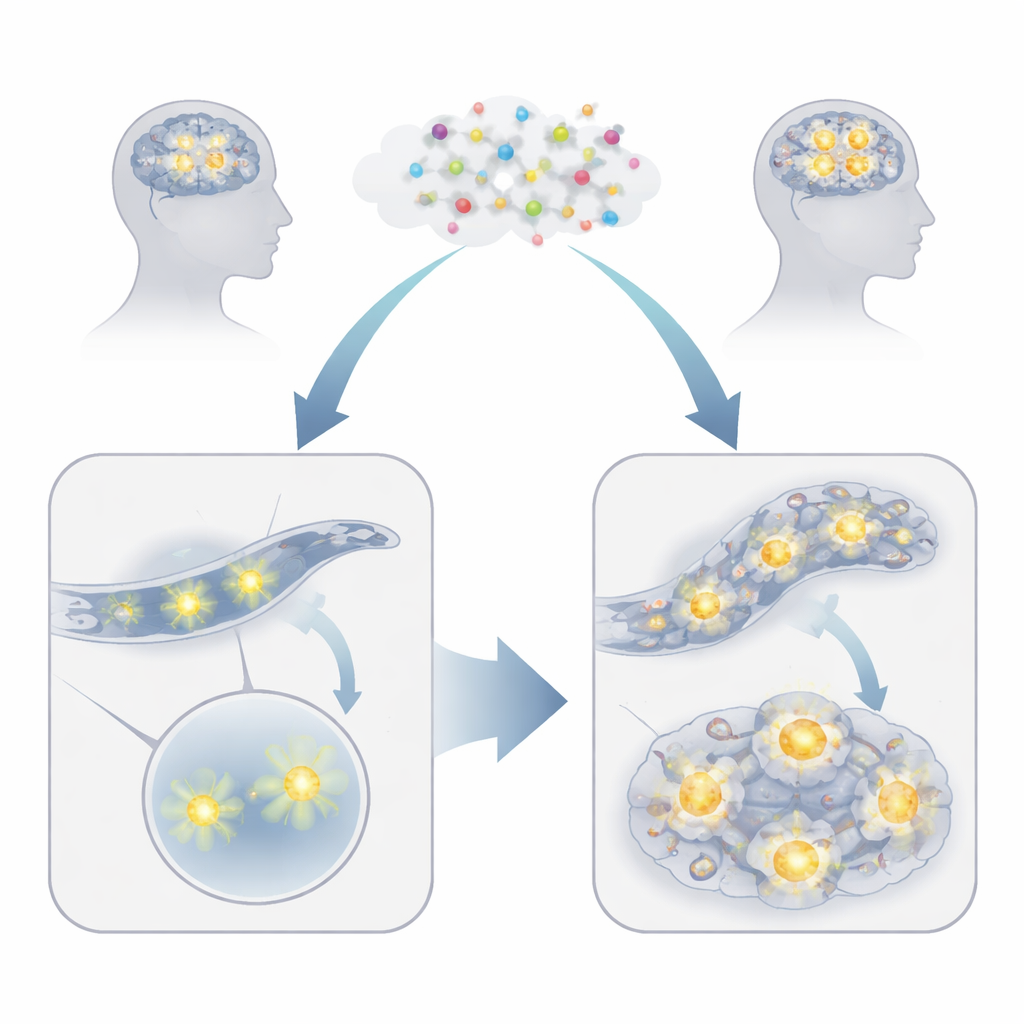
Verborgene Veränderungen in Proteinclustern und Genaktivität
Genauer betrachtet fanden die Forscher, dass anesthetisierte, verwundbare Würmer mehr sichtbare Proteinfoki bildeten — helle Punkte, an denen sich die klebrigen Proteine sammeln — und paradoxerweise gleichzeitig weniger große, detergenzresistente Proteinaggregate aufwiesen. Dieses Muster deutet auf eine Verschiebung hin zu kleineren, toxischeren Proteinversammlungen statt zu harmlosen, dicht gepackten Klumpen. Gleichzeitig stellten die Zellen der Würmer ihre Genaktivität um. Hunderte Gene, die an Stressreaktionen, Stoffwechsel und Proteinreinigung beteiligt sind, wurden nach Isofluran‑Exposition hoch- oder herunterreguliert, unabhängig davon, ob die Würmer die riskanten Proteine trugen. Einige Helfer, etwa bestimmte Faltungs‑Chaperone, waren erhöht, was zeigt, dass die Zellen Gefahr wahrnahmen und zu reagieren versuchten. Doch mindestens ein Chaperon, HSP‑16.41, verschlechterte in Anwesenheit von Isofluran die Lage tatsächlich, was verdeutlicht, wie ein Schutzmechanismus unter ungünstigen Bedingungen schädlich werden kann.
Mitochondrien im Fadenkreuz
Die auffälligsten Veränderungen zeigten sich, als das Team untersuchte, welche Proteine tatsächlich in unlösliche Klumpen übergingen. Bei Würmern mit vorbestehendem Proteinstress stammte ein großer Teil der neu aggregierten Proteine aus den Mitochondrien, besonders aus ihrer inneren Maschinerie und den Proteinimportkanälen. Als die Forscher tomm‑20, ein wichtiges Türprotein, das andere Proteine in die Mitochondrien einschleust, herunterregulierten, konnte Isofluran die Bewegungsstörungen weder in Muskel- noch in Nervenzellen weiter verschlimmern. Andere mitochondriale Komponenten, etwa die Komplex‑I‑Untereinheit GAS‑1, beeinflussten ebenfalls die Empfindlichkeit gegenüber dem Narkotikum. Zusammen deuten diese Befunde darauf hin, dass Mitochondrien eine zentrale Bühne sind, auf der die toxische Verbindung zwischen Anästhesie und Proteinschaden ausgetragen wird.
Wenn die zelluläre Reinigung zu weit geht
Zellen erhalten ihre Mitochondrien über einen Recyclingweg namens Mitophagie, der beschädigte Organellen zur Entfernung markiert. Das Team entdeckte, dass dieser Prozess, der üblicherweise schützend wirkt, sich zur zweischneidigen Angelegenheit wandeln kann. Isofluran‑Exposition erhöhte die Aktivität mehrerer Gene, die mit allgemeiner zellulärer Reinigung und mitochondrialem Recycling in Verbindung stehen. Das gezielte Herunterregulieren bestimmter Mitophagie‑Komponenten, insbesondere der Kinase PINK‑1 und der Cargo‑Rezeptoren SQST‑1, SQST‑2 und LGG‑1, schützte die Würmer jedoch tatsächlich vor den schädlichen Effekten des Narkotikums. Bei Würmern, die durch klebrige Proteine belastet waren, schien Isofluran das Gleichgewicht zugunsten übermäßiger mitochondrialer Entfernung zu verschieben, ohne ausreichende Ersatzbildung, sodass die Zellen mit weniger gesunden Kraftwerken zurückblieben. Diese Idee wird unterstützt von einem kleinen Molekül, VL‑004, das die mitochondriale Fitness zu verbessern scheint, die Mitochondrienzahl wiederherstellte und die Beweglichkeit der anesthetisierten, proteinbelasteten Würmer teilweise rettete.
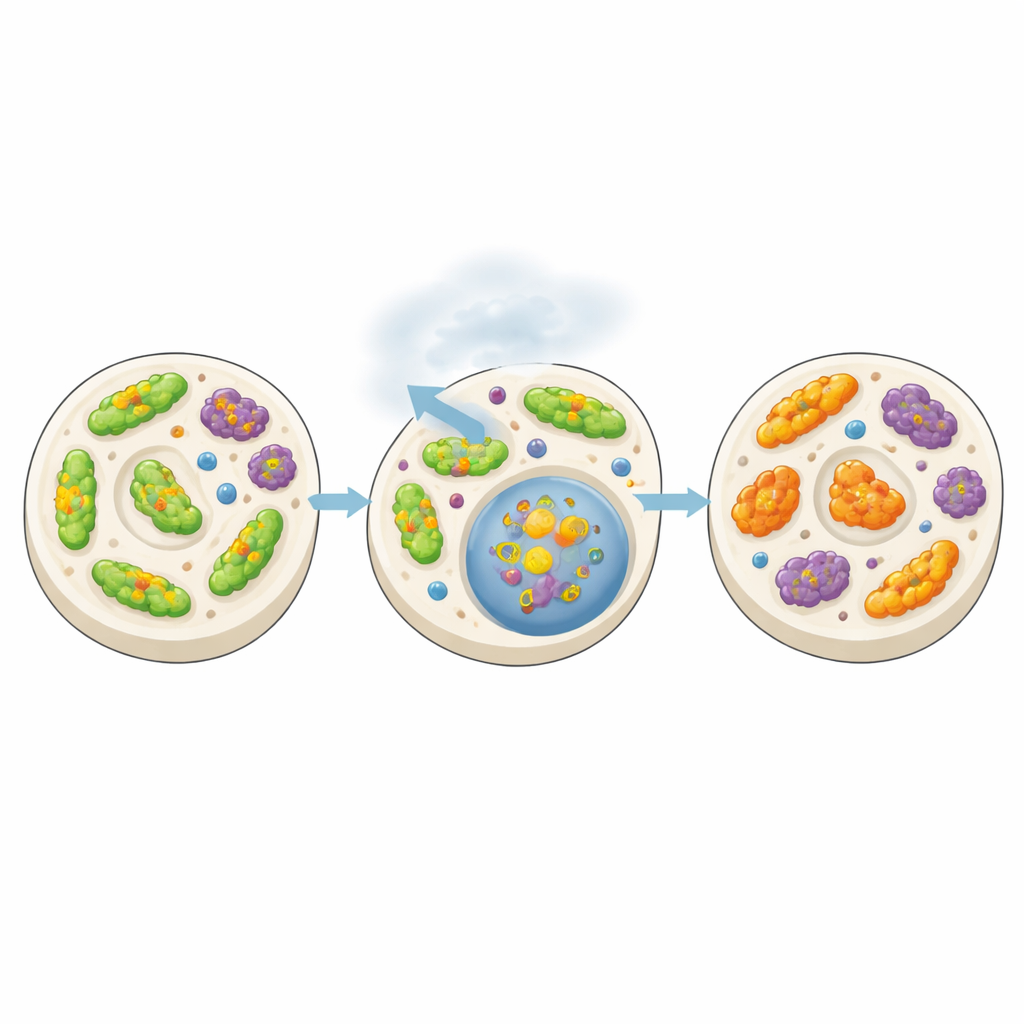
Was das für Patienten nach Operationen bedeuten könnte
Kurz gesagt legt diese Arbeit nahe, dass Isofluran Proteinschäden und funktionellen Abbau vertiefen kann, vor allem in Zellen, die bereits aufgrund altersbedingter oder vererbter Anfälligkeiten am Limit leben. Indem das Narkotikum die mitochondriale Reinigung überaktiviert und das Wachstum neuer Mitochondrien nicht ausreichend unterstützt, hinterlässt es diese Zellen energiearm und weniger fähig, toxische Proteinarten zu bewältigen. Zwar sind Würmer keine Menschen, doch die hier untersuchten Kernprozesse sind über Arten hinweg konserviert, und die Ergebnisse bieten eine mechanistische Brücke zwischen flüchtigen Narkotika, mitochondrialem Stress und langanhaltenden kognitiven Problemen nach Operationen. Die Studie eröffnet die Möglichkeit, dass eine gezielte Anpassung der mitochondrialen Fitness — beispielsweise mit Wirkstoffen wie VL‑004 oder durch Eingriffe in Mitophagie‑Wege — das Risiko eines postoperativen Delirs bei Patienten mit vorbestehenden kognitiven oder Protein‑Handhabungs‑Störungen verringern könnte.
Zitation: Elami, T., Zhu, H., Bruck-Haimson, R. et al. Isoflurane aggravates pre-existing proteotoxicity in adult nematodes by suppressing mitochondrial fitness. Sci Rep 16, 8098 (2026). https://doi.org/10.1038/s41598-026-38591-8
Schlüsselwörter: postoperatives Delir, Isofluran, Mitochondrien, Proteinaggregation, C. elegans