Clear Sky Science · de
Aktivierte T‑Zellen induzieren Apoptose in A549-Lungenadenokarzinomzellen über TRPV4-vermittelten Kalziumeinstrom
Warum diese Forschung für Lungenkrebs wichtig ist
Lungenkrebs gehört weiterhin zu den tödlichsten Krebserkrankungen, teilweise weil Tumoren oft Resistenzen gegen Standardbehandlungen wie Chemotherapie und Bestrahlung entwickeln. In den letzten Jahren hat die Nutzung des körpereigenen Immunsystems neue Hoffnungen geweckt. Diese Studie verfolgt einen neuen Ansatz: Sie zeigt, wie eine bestimmte Art von Immunzellen, sogenannte aktivierte T‑Zellen, Lungenkrebszellen zur Selbstzerstörung treiben können, indem sie über ein molekulares „Tor“ namens TRPV4 Kalzium in die Zellen einströmen lassen. Das Verständnis dieses Weges könnte Forschern helfen, wirksamere und präzisere Immuntherapien zu entwickeln.
Soldaten des Immunsystems treffen auf Lungen-Tumorzellen
Die Forschenden konzentrierten sich auf menschliche Lungenadenokarzinomzellen vom Typ A549, ein weit verbreitetes Modell für nicht‑kleinzelligen Lungenkrebs. Sie kombinierten diese Krebszellen mit Jurkat‑T‑Zellen, einem Modell für zytotoxische T‑Zellen, die im Körper normalerweise infizierte oder entartete Zellen suchen und zerstören. Durch chemische Aktivierung der Jurkat‑Zellen ahmte das Team den hoch alarmierten Zustand von T‑Zellen in einer echten Immunantwort nach. Anschließend mischten sie aktivierte oder inaktive T‑Zellen mit den Lungenkrebszellen in unterschiedlichen Verhältnissen und beobachteten über ein bis drei Tage, wie viele Krebszellen überleben und wie viele programmierter Zelltod (Apoptose) erleiden.
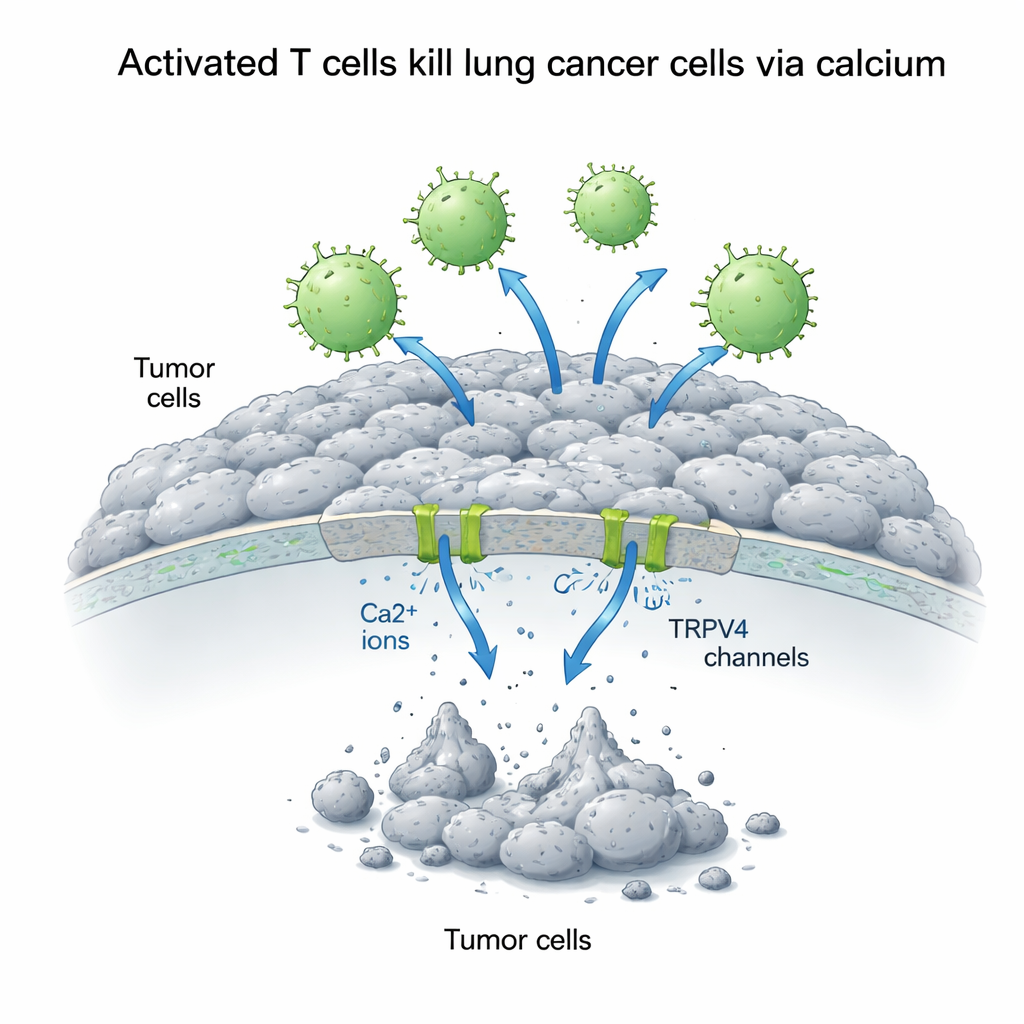
Kalzium als zweischneidiges Signal für Krebszellen
Intrazelluläres Kalzium fungiert als vielseitiger Signalschalter, der je nach Kontext entweder Wachstum fördern oder Zelltod auslösen kann. Die Forschenden erhöhten die Kalziumkonzentration außerhalb der A549‑Zellen und maßen, wie sich das auf den Kampf zwischen T‑Zellen und Tumorzellen auswirkte. Überraschenderweise förderte zusätzliches Kalzium allein das Wachstum der Lungenkrebszellen, was darauf hindeutet, dass Kalzium unter ruhigen Bedingungen Überlebenswege stärkt. In Anwesenheit aktivierter T‑Zellen kehrte sich das Ergebnis jedoch um: Höhere extrazelluläre Kalziumwerte verstärkten die T‑Zell‑vermittelte Abtötung deutlich. Über 72 Stunden sank das Überleben der Krebszellen auf weniger als ein Drittel der normalen Werte, wenn aktivierte T‑Zellen und zusätzliches Kalzium kombiniert wurden; inaktive T‑Zellen zeigten kaum Wirkung und konnten bei zugeführtem Kalzium sogar das Wachstum unterstützen.
Ein Kalzium‑„Tor“ in Verbindung mit Stress und Zelltod
Um zu verstehen, wie dieser Wechsel von Wachstum zu Tod zustande kommt, untersuchten die Forschenden TRPV4, einen Proteinkanal in der Zellmembran, der Kalziumeinströme ermöglicht. Mittels Proteinanalyse stellten sie fest, dass die TRPV4‑Spiegel deutlich anstiegen, wenn A549‑Zellen erhöhtem Kalzium ausgesetzt wurden — unabhängig davon, ob T‑Zellen vorhanden waren — und am höchsten waren, wenn Kalzium und aktivierte T‑Zellen zusammenwirkten. Zugleich zeigten die Krebszellen eindeutige Anzeichen oxidativen Stresses: das Gleichgewicht verschob sich weg von schützenden Antioxidantien (niedrigere gesamte antioxidative Kapazität) hin zu schädlichen Oxidantien (höherer Gesamtoxidationsstatus). Durchflusszytometrie, eine Technik, die Zellen mit fluoreszierenden Farbstoffen markiert, bestätigte, dass aktivierte T‑Zellen einen Anstieg sowohl früher als auch später Stadien der Apoptose auslösten, besonders bei hohem Kalzium. Zusammen deuten diese Beobachtungen auf eine Abfolge hin, in der TRPV4‑Kanäle mehr Kalzium einlassen, was zu chemischem Stress innerhalb der Zelle führt und sie in Richtung Zelltod treibt.
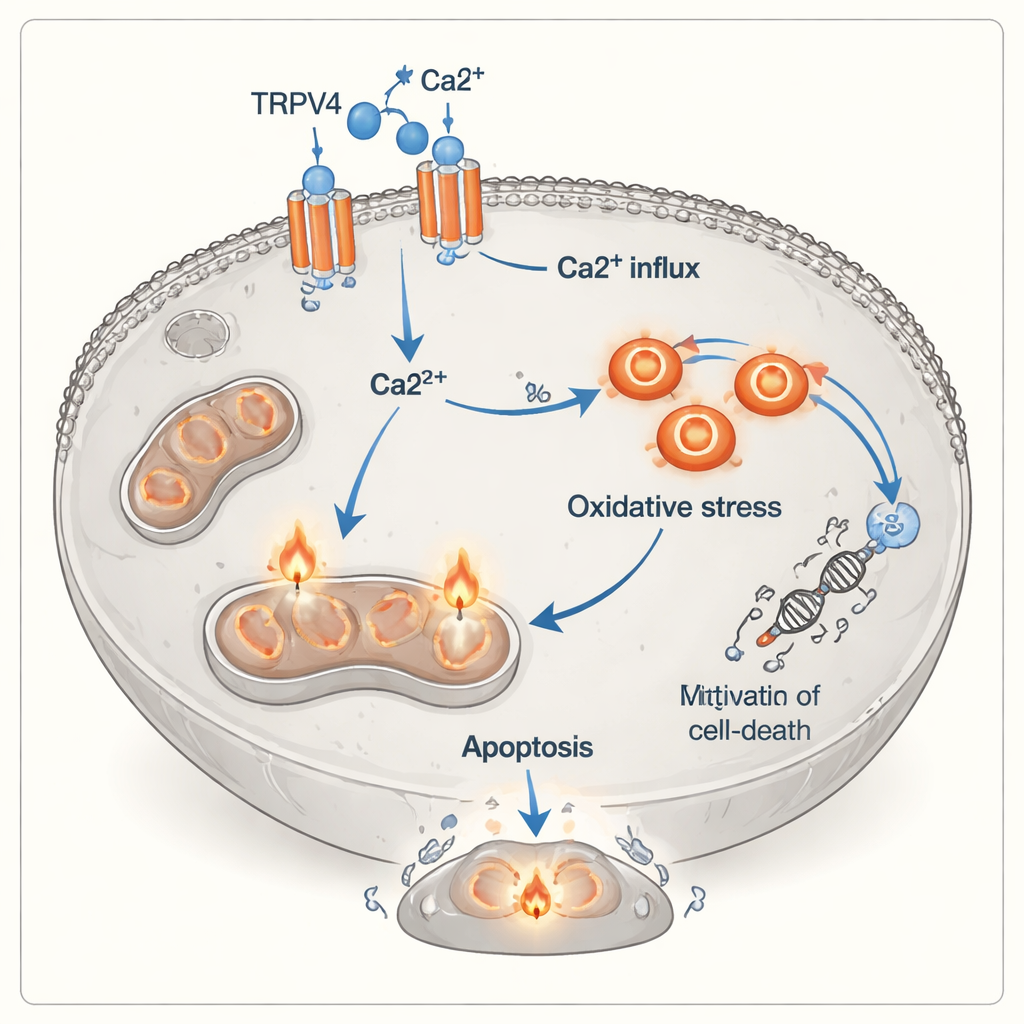
Eine neue Ebene, wie Immunzellen Tumoren töten
Klassischerweise zerstören zytotoxische T‑Zellen ihre Ziele durch Freisetzung toxischer Proteine oder durch Aktivierung von Todesrezeptoren auf der Tumorzelloberfläche. Diese Studie legt nahe, dass es einen weiteren, indirekteren Weg gibt: Signale aktivierter T‑Zellen — einschließlich entzündlicher Moleküle und direktem Zell‑zu‑Zell‑Kontakt — scheinen Lungenkrebszellen abhängiger von TRPV4 zu machen und anfälliger für Kalziumüberladung und oxidative Schäden. In diesem Sinne fungiert TRPV4 wie ein Sensibilisierungsschalter, der sonst wachstumsförderndes Kalzium in ein tödliches Signal verwandelt. Obwohl die Experimente in Zellkulturen und mit einer einzelnen Krebszelllinie durchgeführt wurden, heben sie eine potenziell wichtige Verbindung zwischen Immunangriff, Ionenkanälen und der inneren Stressmaschinerie von Tumorzellen hervor.
Welche Bedeutung das für zukünftige Therapien haben könnte
Für Nicht‑Spezialisten lautet die Schlussfolgerung: Der Erfolg von Immuntherapien könnte nicht nur davon abhängen, T‑Zellen stärker zu machen, sondern auch Krebszellen leichter angreifbar zu gestalten. Durch das gezielte Ansprechen von TRPV4 oder verwandten Kalziumkanälen könnten Ärztinnen und Ärzte eines Tages die Fähigkeit von T‑Zellen verbessern, Lungentumoren zu eliminieren, oder Therapien so abstimmen, dass gesunde Gewebe verschont bleiben. Die Arbeit befindet sich noch in einem frühen Stadium, und die Autorinnen und Autoren betonen die Notwendigkeit weiterer Experimente in Tiermodellen und komplexeren Systemen. Dennoch fügt die Entdeckung einer TRPV4–Kalzium–oxidativem Stress‑Achse ein vielversprechendes neues Ziel dem Werkzeugkasten zur Verbesserung immunbasierter Therapien gegen Lungenkrebs hinzu.
Zitation: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Schlüsselwörter: Immuntherapie bei Lungenkrebs, T‑Zellen, Kalziumsignalisierung, TRPV4‑Kanal, oxidativer Stress