Clear Sky Science · de
Fraktalanalyse der Gefäßarchitektur bei hepatozellulärem Karzinom zeigt regionale Unterschiede unabhängig von vaskulärer Invasion
Den Krebs durch seine Blutgefäße sehen
Ärztinnen und Ärzte wissen, dass Tumoren ein eigenes chaotisches Netzwerk von Blutgefäßen ausbilden und dass die Anordnung dieser Gefäße beeinflussen kann, wie wirksam Behandlungen sind. Bei Leberkrebs gehören Medikamente, die die Blutversorgung angreifen, bereits zur Standardtherapie, doch labormäßige Messungen zählen meist nur, wie viele Gefäße vorhanden sind, nicht wie sie angeordnet sind. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Lässt sich das „Muster“ der Tumorblutgefäße mit nur wenigen Zahlen erfassen, und unterscheiden sich diese Muster zwischen Tumor, dem umliegenden Gewebe und dem übrigen Lebergewebe?
Muster in verzweigten Netzwerken
Die Forschenden konzentrierten sich auf das hepatozelluläre Karzinom, den häufigsten primären Leberkrebs. Sie untersuchten Gewebeproben von 29 Patientinnen und Patienten, deren Leberpräparate so gefärbt wurden, dass die Innenauskleidung der Blutgefäße unter dem Mikroskop braun erscheint. Anstatt die Gefäße nur zu zählen, analysierten sie, wie die Gefäße gemeinsam Raum ausfüllen, mithilfe mathematischer Werkzeuge, die oft bei komplexen natürlichen Formen wie Küstenlinien oder Baumverzweigungen angewendet werden. Zwei zentrale Maße kamen zum Einsatz: eines, das beschreibt, wie „feingliedrig“ das Gefäßnetz ist, und ein anderes, das beschreibt, wie die leeren Räume zwischen den Gefäßen verteilt sind. Zusammen kondensieren diese Zahlen die visuelle Komplexität des Gefäßnetzes in eine Form, die sich zwischen verschiedenen Regionen der Leber vergleichen lässt.
Vom Mikroskopbild zur messbaren Karte
Dazu musste das Team zuerst die Gefäße zuverlässig vom umgebenden Gewebe auf großen digitalen Schnitten trennen. Sie bauten eine automatisierte Bildverarbeitungs-Pipeline, die die braun gefärbten Gefäße identifizierte, Störsignale entfernte und Gefäßinnenräume auffüllte, sodass klare Schwarz-Weiß-Karten der Gefäßnetze entstanden. Diese automatischen Segmentierungen wurden mit einem Leberpathologen abgeglichen und zeigten eine gute Übereinstimmung, insbesondere in den Aspekten, die für die globalen Maße der Gefäßorganisation wichtig sind. Die Schnitte wurden dann in viele kleinere Kacheln unterteilt, von denen jede einer von drei Regionen zugeordnet wurde: Tumor, unmittelbar den Tumor umgebendes Gewebe (peri-tumoral) oder entferntes, nicht-tumoröses Lebergewebe. Kacheln mit nekrotischem Gewebe oder größeren Artefakten wurden sorgfältig ausgeschlossen, da sie dichte, unrealistische Gefäßmuster vortäuschen können.
Worin sich Tumorregionen vom Rest unterscheiden
Über Tausende von Kacheln hinweg fand die Studie klare, statistisch starke Unterschiede in den Gefäßmustern zwischen den drei Leberregionen. Nicht-tumoröses Lebergewebe zeigte die höchste Komplexität und verhielt sich auf größeren Skalen fast wie ein raumfüllendes Netz. Peri-tumorales Gewebe lag mittig, während Tumorregionen durchgehend geringere Komplexität aufwiesen. Ein verwandtes Maß zur Anordnung der Zwischenräume zwischen Gefäßen stieg ebenfalls von nicht-tumorös über peri-tumoral zu tumoral an, was darauf hindeutet, dass tumorassoziierte Gefäße stärker gehäuft und räumlich korrelierter sind. Entscheidend war: Ob der Tumor bereits in benachbarte Blutgefäße eingedrungen war — ein klinisch wichtiges Warnzeichen — veränderte diese Gesamtmuster nicht messbar. Die Architektur des Gefäßnetzes wurde vor allem durch die Anwesenheit des Tumors selbst geprägt, nicht durch diesen Invasionsschritt.
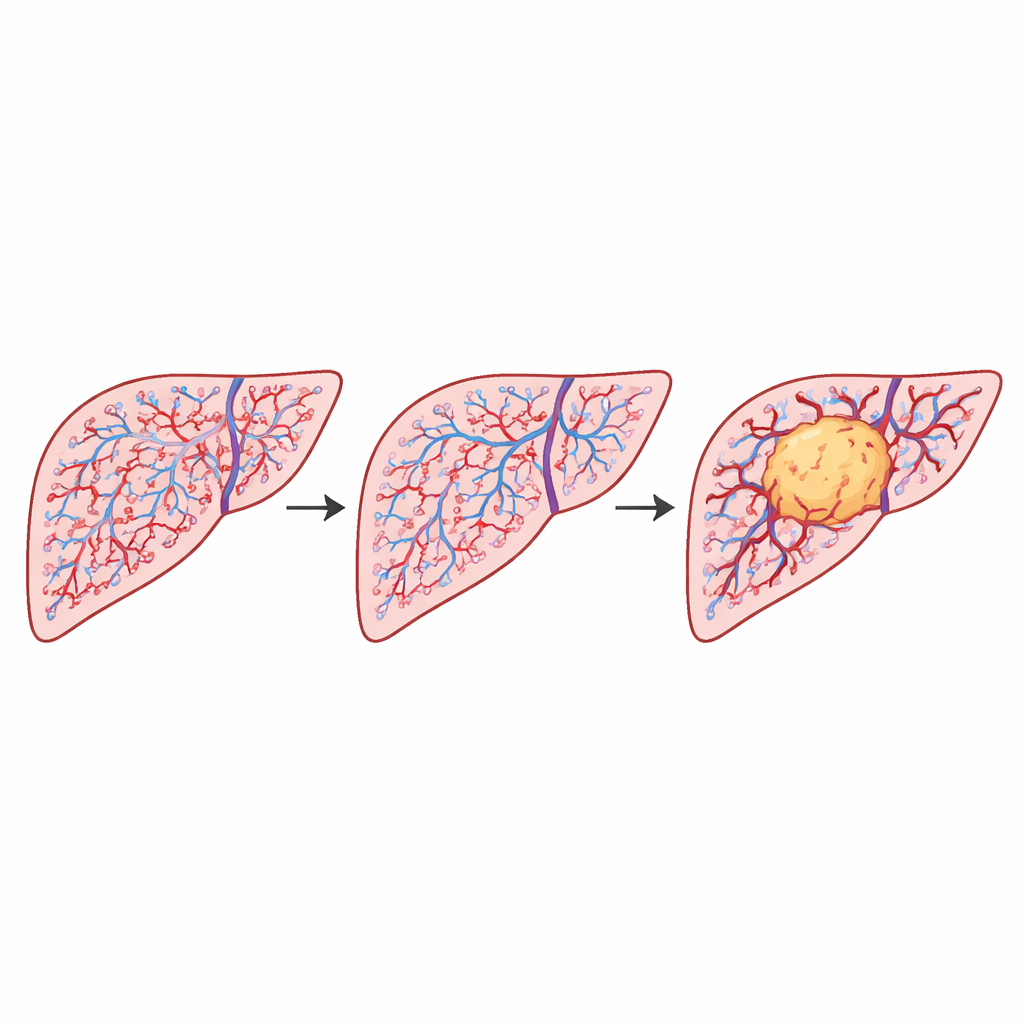
Warum Form und Größe der Gefäße wichtig sind
Um die hinter diesen numerischen Unterschieden liegenden Ursachen zu verstehen, betrachteten die Autorinnen und Autoren genauer die Formen und Größen einzelner Gefäße. In gesunder Leber zeigte sich eine deutliche Häufung vieler kleiner, runder Gefäße bei gleichzeitig wenigen größeren Gefäßen. In Tumorregionen war die Gesamtgefäßfläche ähnlich, doch die Gefäße verteilten sich gleichmäßiger über verschiedene Größen und waren häufiger länglich oder unregelmäßig geformt. Einfache Modelle zeigten, dass ein Netzwerk mit vielen winzigen, runden Gefäßen mehr kleine Quadrate benötigt, wenn man das Muster „überdeckt“, was das Komplexitätsmaß erhöht. Dagegen erscheint ein Netzwerk mit weniger kleinen Gefäßen und homogeneren Größen weniger verwoben, selbst wenn die gesamte Gefäßfläche ähnlich ist. Diese geometrische Verschiebung entspricht dem beobachteten Rückgang der Komplexität in Tumoren und erklärt, wie subtile Änderungen in der Verteilung von Gefäßformen das Gesamtgefäßmuster umgestalten können.
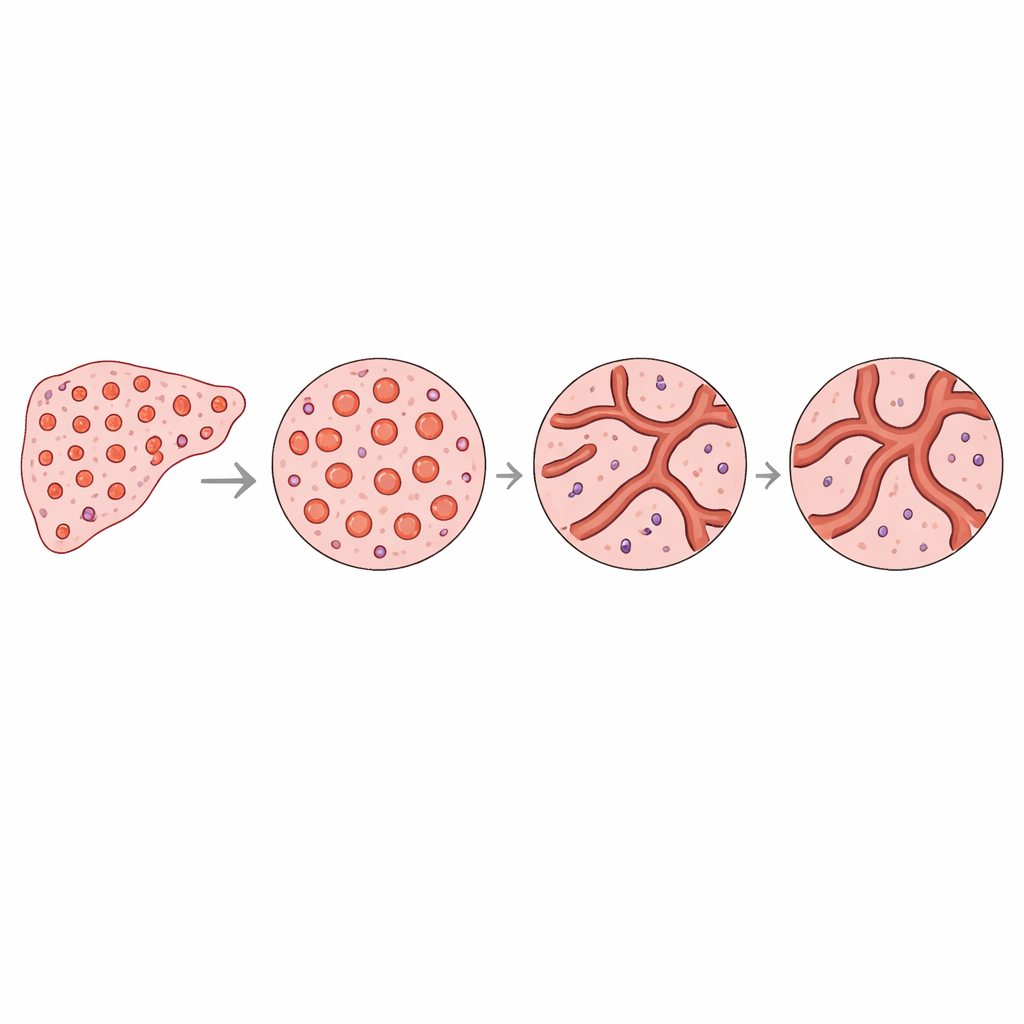
Was das für künftige Bildgebung bedeuten könnte
Für Nicht-Spezialisten ist die zentrale Erkenntnis, dass Lebertumoren nicht nur mehr Blutgefäße bilden; sie reorganisieren diese auf eine unterscheidbare, messbare Weise, die sich ins umgebende Gewebe ausbreitet. Diese Unterschiede lassen sich mit kompakten mathematischen Kennzahlen erfassen, die zusammenfassen, wie Gefäße und die Räume zwischen ihnen angeordnet sind. Die Arbeit legt nahe, dass künftig fortgeschrittene Bildgebungsverfahren diese Kennzahlen möglicherweise ohne Biopsie abschätzen könnten und so neue, nichtinvasive Biomarker liefern, mit denen sich die Ausdehnung des Tumoreinflusses und die Struktur seiner Blutversorgung beurteilen lassen. Zugleich zeigt die Studie, dass mikroskopische Invasion benachbarter Gefäße nicht zwangsläufig ein erkennbares Muster in der großskaligen Gefäßarchitektur hinterlässt, und unterstreicht damit, dass nicht alle gefährlichen Tumoreigenschaften allein über die Gefäßarchitektur sichtbar sind.
Zitation: Penney, J., Nardon, V., Beaufrere, A. et al. Fractal analysis of hepatocellular carcinoma vasculature shows regional differences independent of vascular invasion. Sci Rep 16, 11049 (2026). https://doi.org/10.1038/s41598-026-38580-x
Schlüsselwörter: Gefäßsystem von Leberkrebs, fraktale Gefäßarchitektur, hepatozelluläres Karzinom, Tumormikroumgebung, nichtinvasive Bildgebungs-Biomarker