Clear Sky Science · de
Histatin‑1 fördert die Expression von Markern, die mit der odontoblastären Differenzierung im Zahnmark und der apikalen Papille assoziiert sind
Warum Speichel helfen könnte, Ihre Zähne zu retten
Wenn ein Zahn durch Karies oder Verletzung stark beschädigt ist, versuchen Zahnärzte, ihn zu erhalten, indem sie das weiche Innengewebe, das sogenannte Zahnmark (Pulpa), schützen. Das Zukunftsziel der Zahnmedizin ist es, dem Zahn zu ermöglichen, sich selbst zu reparieren und die harte Dentinschicht wieder aufzubauen, anstatt sich nur auf Füllungen und Kronen zu verlassen. In dieser Studie wurde untersucht, ob ein natürliches Protein im menschlichen Speichel, Histatin‑1, Zellen in jungen Zähnen dazu anregen kann, sich in dentinbildende Zellen zu verwandeln und so die Reparatur von innen zu unterstützen.
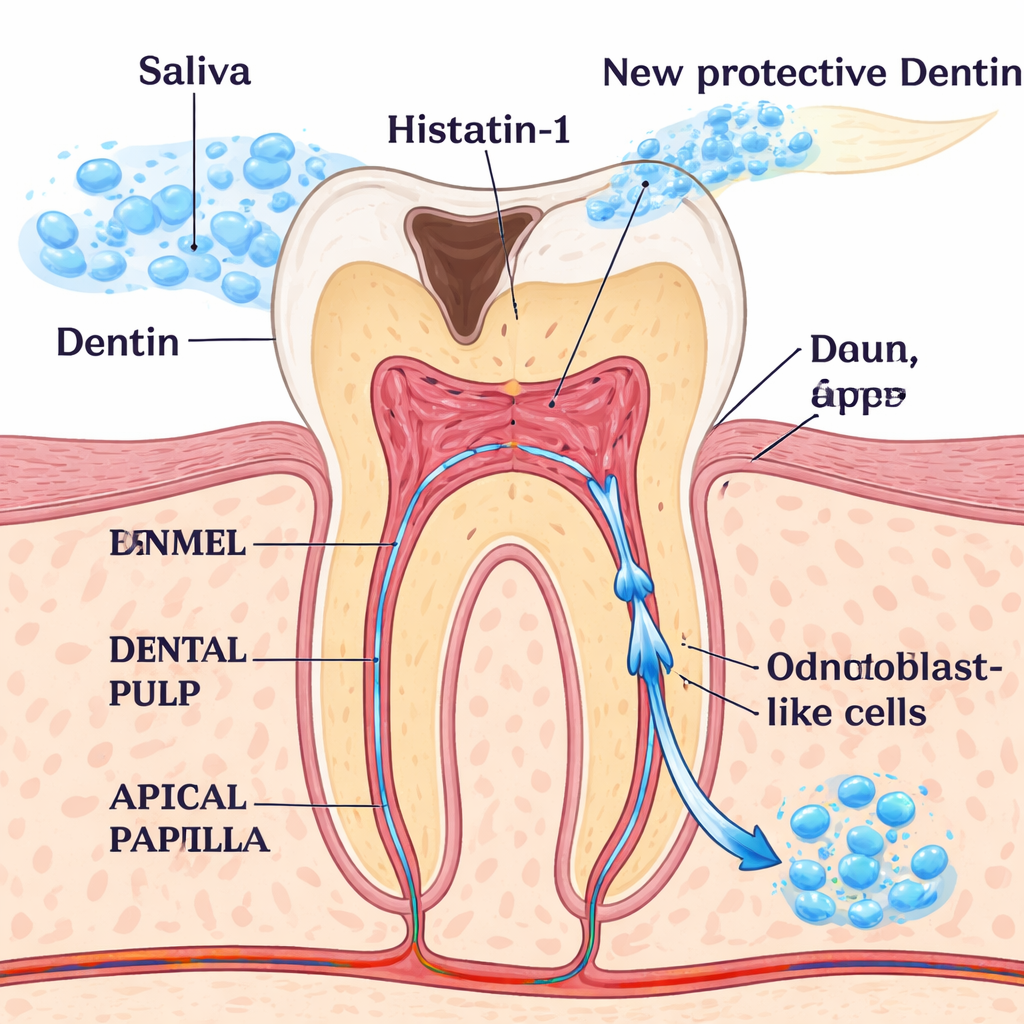
Versteckte Reparaturtruppen in jungen Zähnen
Im Inneren jedes Zahns enthalten das Zahnmark und eine benachbarte Region an der Wurzelspitze, die apikale Papille, vielseitige Zellen, die sich zu verschiedenen Zelltypen entwickeln können. Zu den wichtigsten gehören die Odontoblasten, spezialisierte Zellen, die Dentin bilden und erhalten, das schützende harte Gewebe unter dem Schmelz. Bei tiefen Kariesläsionen oder Traumata werden Odontoblasten geschädigt oder gehen verloren, und erfolgreiche regenerative Behandlungen hängen davon ab, ihre Funktion zu ersetzen. Wissenschaftler suchen seit Langem nach sicheren Signalen, die Pulpa‑ und Papillenzellen in Richtung eines odontoblastähnlichen Zustands lenken, damit sie den Zahn von innen wiederaufbauen können.
Ein Speicheleiweiß mit überraschenden Fähigkeiten
Histatin‑1 ist hauptsächlich als kleines Protein im Speichel bekannt, das Zähne vor Mikroben schützt und die Wundheilung unterstützt. Frühere Arbeiten zeigten, dass es auch Knochen‑verwandte Zellen zur Bewegung, Adhäsion und Mineralablagerung anregen kann, was darauf hindeutet, dass es die Bildung harter Gewebe im weiteren Sinne beeinflussen könnte. Die Autorinnen und Autoren dieser Studie fragten, ob Histatin‑1 speziell Pulpa‑ und apikale Papillenzellen aus noch unreifen bleibenden Zähnen eher in eine odontoblastähnliche Identität drängen kann als nur in einen generischen knochenähnlichen Zustand. Wenn ja, könnte dieses aus dem Speichel stammende Molekül zu einem natürlichen Werkzeug für gezielte zahnmedizinische Regeneration werden.
Pulpa‑Zellen zu Dentinbildnern machen
Um diese Idee zu testen, gewannen die Forscher frisch extrahierte unreife Molaren und teilten jedes Pulpa–Papillen‑Komplex in zwei Hälften, wobei eine Hälfte mit Histatin‑1 behandelt und die andere als Kontrolle belassen wurde. Nach einer Woche untersuchten sie beide Gewebe unter dem Mikroskop. Histatin‑1‑behandelte Proben zeigten mehr von zwei charakteristischen Dentinproteinen — DSPP und DMP1 — und mehr Zellen, die positiv für diese Marker färbten, insbesondere in der apikalen Papille. Als das Team die ansässigen mesenchymalen Zellen isolierte und in Kultur wuchs, erhöhte Histatin‑1 erneut die DSPP‑Spiegel und steigerte die Aktivität von Beta‑Catenin, einem Signalprotein, das die Reifung von Zahnzellen antreibt. Unter dem Mikroskop zeigten behandelte Zellen zudem Gestaltsmerkmale, die bei sich entwickelnden Odontoblasten zu sehen sind: mehr primäre Zilien — winzige, antennenartige Fortsätze — und ein stärker polarisiertes Golgi‑Apparat, was darauf hindeutet, dass die Zellen sich darauf vorbereiten, Dentinmatrix in eine Richtung zu sezernieren.
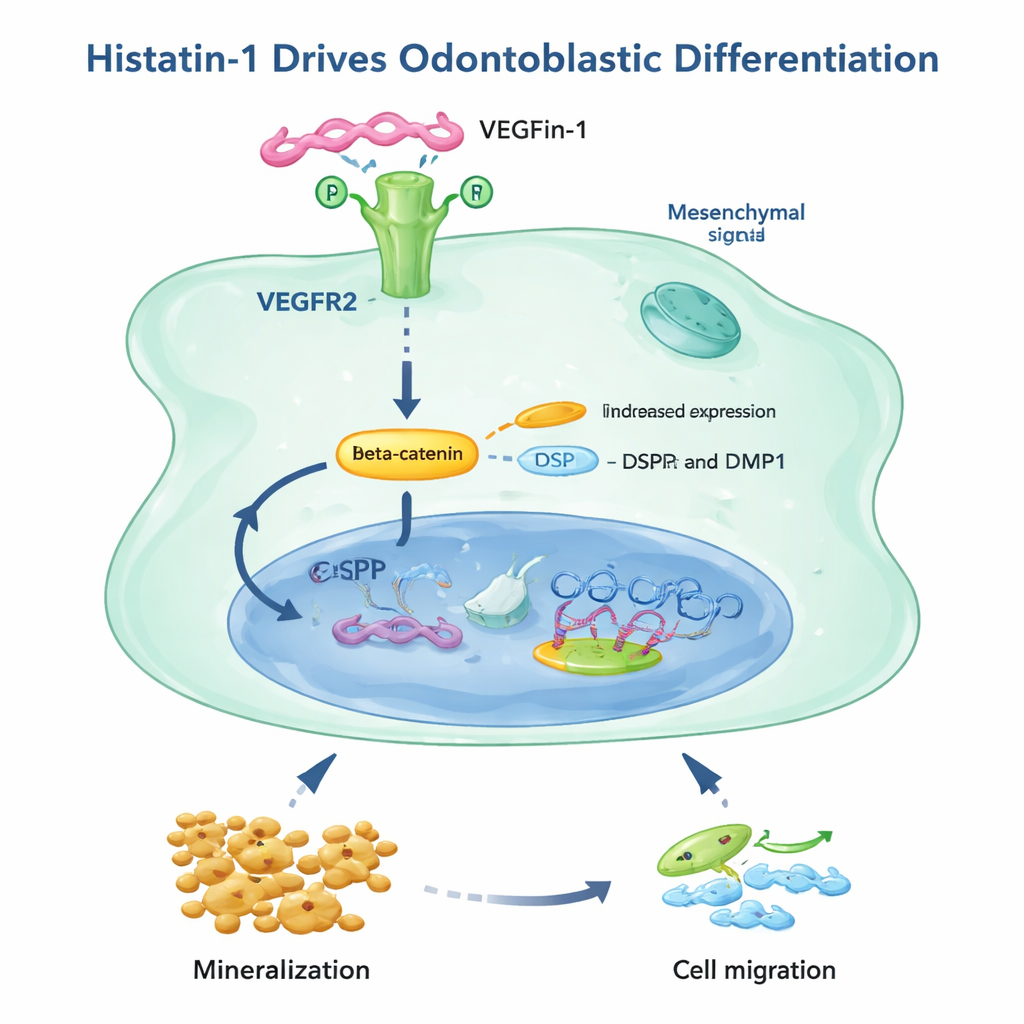
Wie Histatin‑1 das Signal übermittelt
Die Studie untersuchte weiter, wie Histatin‑1 seine Botschaft übermittelt. Frühere Arbeiten hatten auf einer Zelloberflächenrezeptor, VEGFR2, identifiziert, der Histatin‑1 binden kann. Hier bestätigten die Forschenden, dass sowohl Pulpa‑ als auch apikale Papillengewebe VEGFR2 exprimieren und dass Histatin‑1 dessen Spiegel erhöht. Das Blockieren von VEGFR2 mit einem spezifischen Wirkstoff oder die Verwendung einer veränderten Form von Histatin‑1, die sich nicht mehr an diesen Rezeptor binden kann, reduzierte deutlich die Fähigkeit von Histatin‑1, Mineralablagerungen in diesen Zellen auszulösen. Derselbe Rezeptor war auch entscheidend für die histatin‑1‑gesteuerte Zellbewegung in apikalen Papillenzellen, obwohl Pulpa‑Zellen offenbar einen zusätzlichen, VEGFR2‑unabhängigen Weg zur Migration besitzen. Insgesamt deuten die Befunde auf einen Weg hin, bei dem Histatin‑1 an VEGFR2 bindet, die Beta‑Catenin‑Signalgebung verstärkt, odontoblastäre Marker aktiviert und sowohl Mineralisierung als auch Bewegung wichtiger Reparaturzellen fördert.
Was das für die Zahnmedizin der Zukunft bedeuten könnte
Für Nicht‑Fachleute lautet die Kernbotschaft, dass eine natürliche Komponente des Speichels junge Zahnzellen anweisen kann, sich wie Dentinbildner zu verhalten — und zwar über eine definierte Signalroute. Obwohl diese Arbeit an Zell‑ und Gewebeproben und nicht an Patientinnen und Patienten durchgeführt wurde, macht sie Histatin‑1 zu einem vielversprechenden, offenbar gewebeverträglichen Kandidaten für regenerative dentalmedizinische Therapien. In Zukunft könnten maßgeschneiderte Gele, Spülungen oder pulpakappende Materialien mit Histatin‑1 eines Tages die körpereigenen Zellen des Zahns dazu leiten, in beschädigte Bereiche zu wandern und verlorenes Dentin wiederaufzubauen — eine biologischere Alternative zu traditionellen restaurativen Verfahren.
Zitation: Silva, P., Garrido, M., Tapia, H.A. et al. Histatin-1 promotes the expression of markers associated with odontoblastic differentiation in the dental pulp and apical papilla. Sci Rep 16, 7360 (2026). https://doi.org/10.1038/s41598-026-38578-5
Schlüsselwörter: Zahnregeneration, Histatin‑1, Odontoblasten, Zahnpulpa‑Stammzellen, Dentinreparatur