Clear Sky Science · de
Vergleich und Kombination von Xevinapant mit ATR- und PARP-Inhibition zur Radiosensibilisierung von HPV-negativen HNSCC-Zellen
Warum eine Verstärkung der Strahlentherapie wichtig ist
Die Strahlentherapie ist eine zentrale Behandlung für Tumore im Mund- und Rachenraum, doch viele Tumoren sind dagegen resistent, sodass Ärzte hohe Dosen einsetzen müssen, die normales Gewebe schädigen können. Diese Studie stellt eine praxisnahe Frage mit großen Folgen für Patientinnen und Patienten: Unter mehreren modernen Krebsmedikamenten, die Tumorzellen anfälliger machen sollen, welche funktionieren tatsächlich am besten zusammen mit Strahlung gegen schwer zugängliche, HPV-negative Kopf‑und‑Hals-Tumoren, die im Labor gezüchtet wurden?
Aktuelle Behandlung und ihre Grenzen
Patienten mit lokal fortgeschrittenem Plattenepithelkarzinom im Kopf‑Hals-Bereich werden häufig mit einer Kombination aus Strahlentherapie und dem Chemotherapeutikum Cisplatin behandelt oder operativ versorgt und anschließend bestrahlt. Obwohl dieses Vorgehen den Krebs kontrollieren kann, hinterlässt es oft schwere langfristige Nebenwirkungen wie Schluckstörungen, trockenen Mund, Hörprobleme und Nierenschäden. Viele ältere oder medizinisch gebrechliche Patientinnen und Patienten vertragen Cisplatin gar nicht. Das hat das Interesse an sogenannten Radiosensibilisierern geweckt – Arzneimitteln, die Tumorzellen leichter töten lassen, sodass die Behandlung effektiver oder potenziell schonender sein kann.
Ein vielversprechendes Medikament, das scheiterte
Ein solches Medikament, Xevinapant, wurde zunächst als Durchbruch gefeiert. Es ahmt ein natürliches Protein namens SMAC nach und blockiert Moleküle, die Krebszellen helfen, dem programmierten Zelltod zu entkommen. In früheren Studien verbesserte die Zugabe von Xevinapant zur Standard-Chemoradiation in einer Phase‑2-Studie die Ergebnisse bei Kopf‑Hals-Krebs, was Hoffnungen weckte, dass es ein neuer Behandlungsstandard werden könnte. Doch eine viel größere Phase‑3-Studie, TrilynX, wurde vorzeitig abgebrochen, nachdem Zwischenanalysen nicht nur keinen Nutzen, sondern sogar schlechteres Überleben und mehr Nebenwirkungen in der Xevinapant-Gruppe zeigten. Dieses unerwartete Scheitern machte eine dringende Neubewertung erforderlich, wie gut Xevinapant die Strahlentherapie tatsächlich unterstützt, und einen Vergleich mit anderen, neueren Strategien.
Drei Strategien im direkten Vergleich
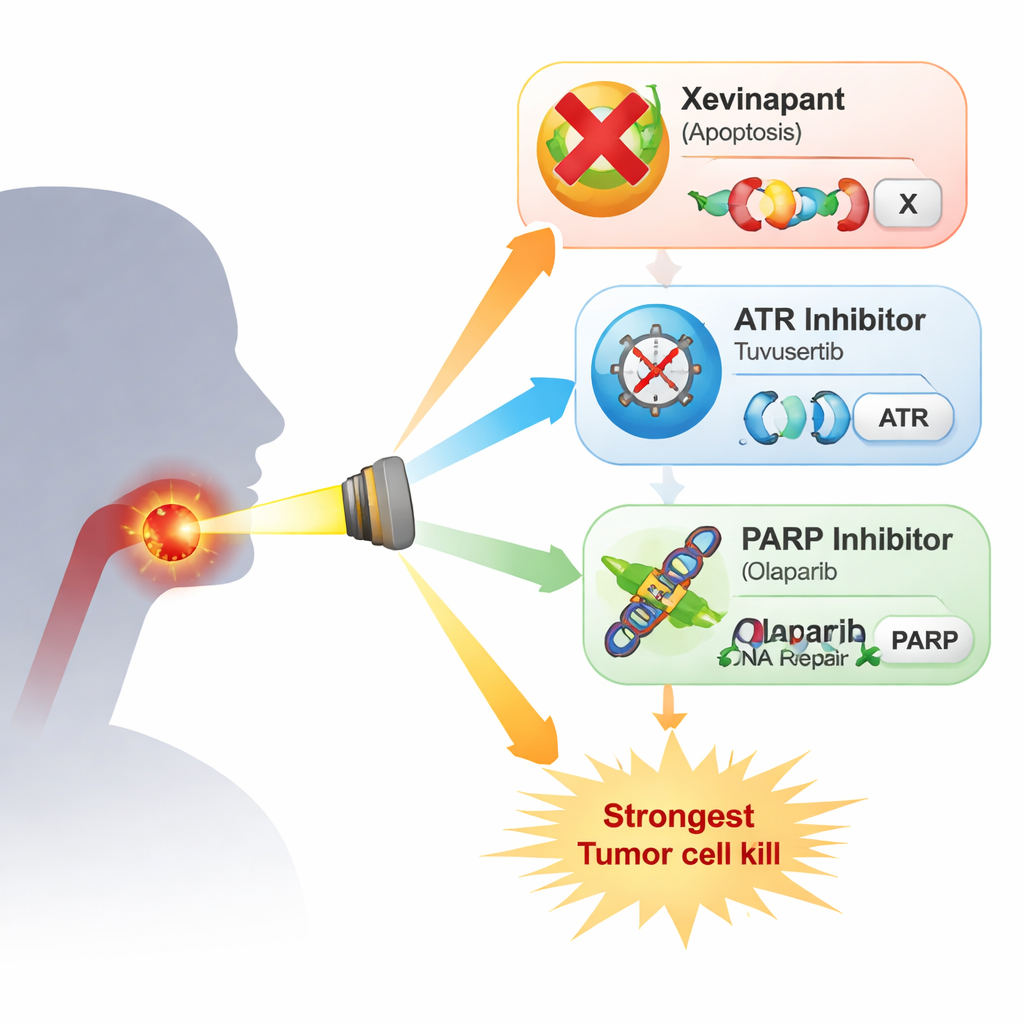
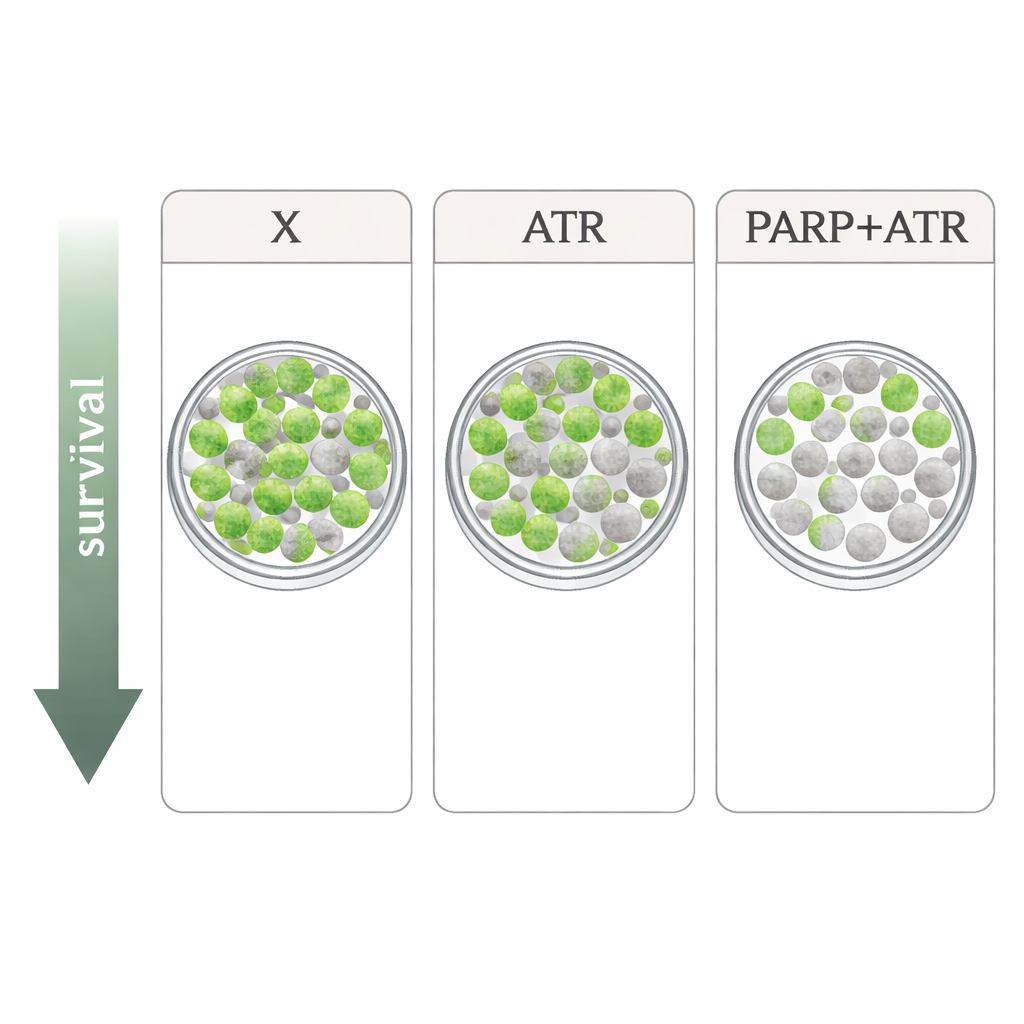
Die Forscher untersuchten vier strahlungsresistente, HPV-negative Kopf‑und‑Hals-Krebszelllinien. Sie verglichen Xevinapant mit zwei Medikamenten, die die DNA-Schadensantwort der Zelle angreifen: dem ATR-Inhibitor Tuvusertib und dem PARP-Inhibitor Olaparib, jeweils in Dosen, die in Patienten erreicht werden können. ATR und PARP sind Schlüsselfaktoren, die Zellen helfen, den Zellzyklus zu pausieren und DNA nach Schäden, zum Beispiel durch Röntgenstrahlung, zu reparieren. In einfachen Wachstumstests verlangsamte jedes Medikament allein die Proliferation nur mäßig, und die Muster variierten zwischen den Zelllinien. Kombiniert mit Strahlung in dem strengsten Test – der Bestimmung, wie viele Einzelzellen noch Kolonien bilden können – zeigte sich ein klareres Bild: Xevinapant fügte in mehreren Linien nur geringe oder keine zusätzliche Strahlenwirkung hinzu, während sowohl Tuvusertib als auch Olaparib die Strahlenwirkung durchweg verstärkten. Die stärkste Wirkung ergab sich aus der Kombination von ATR‑ und PARP‑Hemmung, die in drei der vier Zelllinien besonders starke Einbrüche im Kolonienüberleben bewirkte.
Zelltodsignale sind nicht alles
Da Xevinapant darauf abzielt, Zelltod auszulösen, maßen die Forschenden auch, wie viele Zellen nach der Behandlung, mit und ohne Strahlung, apoptotisch wurden oder lysierten. Diese Todesmarker stiegen in einigen Kontexten deutlich an – besonders in einer Zelllinie namens HSC4 und bei Kombinationen der Medikamente – korrelierten jedoch nicht zuverlässig damit, wie gut die Strahlung das langfristige Überleben tatsächlich unterdrückte. Mit anderen Worten: Kurzfristige Todesmessungen sagten die echte Radiosensibilisierung schlecht vorher. Diese Diskrepanz unterstreicht eine wichtige Lektion für die Wirkstoffentwicklung: Nur Assays, die Zellen lange genug verfolgen, um zu sehen, ob sie wieder nachwachsen können – etwa Kolonieformationstests – können richtig beurteilen, ob ein Radiosensibilisierer wirksam ist.
Was das für künftige Therapien bedeutet
Aus diesen Laborexperimenten lässt sich schließen, dass Xevinapant die Strahlentherapie bei HPV-negativen Kopf‑und‑Hals-Krebszellen zwar bis zu einem gewissen Grad verstärken kann, seine Wirkung jedoch schwächer und weniger konsistent war als Ansätze, die direkt die DNA-Schadensverarbeitung über ATR und PARP stören. Die Kombination von ATR‑ und PARP‑Inhibitoren erzielte den stärksten Effekt, was darauf hindeutet, dass sorgfältig dosierte Kombinationen dieser Mittel mit Strahlentherapie möglicherweise einen vielversprechenderen Weg bieten als die weitere Verfolgung von Xevinapant, zumindest bei diesem Tumortyp. Die Übertragung dieser Ergebnisse in die Klinik wird nicht einfach sein, da solche Medikamente auch normales, schnell teilendes Gewebe belasten und in frühen Studien bereits Dosisreduktionen erforderlich machten. Dennoch weist die Arbeit Kliniker und Forscher in Richtung DNA‑Reparatur‑gerichteter Strategien als überzeugendere Kandidaten, um die Strahlentherapie effektiver und potenziell sicherer für Patientinnen und Patienten zu machen, die keine Standardchemotherapie erhalten können.
Zitation: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Schlüsselwörter: Kopf- und Halskrebs, Strahlentherapie, DNA-Reparatur-Inhibitoren, Xevinapant, Radiosensibilisierung