Clear Sky Science · de
Thermoregulatorische Anpassungen an Kälte bei C3H/HeJ-Mäusen sind unabhängig von ADRB3-Signalgebung
Warum kälteliebende Mäuse für die menschliche Gesundheit wichtig sind
Sich warm zu halten mag nicht nach einem bahnbrechenden medizinischen Thema klingen, doch wie der Körper mit Kälte umgeht, hängt unmittelbar damit zusammen, wie er Energie nutzt und verbrennt. Diese Studie vergleicht zwei gängige Labormausstämme und stellt eine überraschend bedeutsame Frage: Schalten sie bei Kälte ihre internen „Öfen“ auf dieselbe Weise an wie Menschen? Die Antwort hilft zu erklären, warum einige in Mäusen erfolgreiche Anti-Adipositas-Medikamente beim Menschen versagten — und weist auf ein mausmodell hin, das dem Menschen im Stoffwechsel näherkommt.
Zwei Mausstämme, eine frostige Herausforderung
Die Forscher verglichen die standardmäßigen C57BL/6J-Mäuse, ein Arbeitspferd der metabolischen Forschung, mit einem seltener verwendeten Stamm namens C3H/HeJ. Beide Gruppen wurden zunächst bei etwa 30 °C gehalten, einer Temperatur, bei der Mäuse kaum Energie aufwenden müssen, um warm zu bleiben. Anschließend wurden die Tiere schrittweise auf 10 °C abgekühlt, und Körpergewicht, Nahrungsaufnahme sowie Energieverbrauch wurden in hochmodernen Stoffwechselkäfigen genau gemessen. Interessanterweise teilten beide Stämme nahezu denselben „Komfortpunkt“ für minimalen Energieverbrauch — rund 29–30 °C — was bedeutet, dass sie von einem ähnlichen Ausgangsniveau in die Kälte gingen.
Wenn die Kälte einsetzt, arbeitet ein Stamm härter
Sobald die Temperaturen sanken, erhöhten beide Mausstämme wie erwartet ihren Energieverbrauch. Die C3H-Mäuse verbrannten jedoch mehr Energie als die C57-Mäuse, obwohl sie ähnliche Nahrungsmengen aufnahmen. Dieser höhere Energieverbrauch war nicht nur eine kurzfristige Reaktion — er hielt sowohl in den ersten Stunden als auch an den folgenden Tagen der Kälteeinwirkung an. Dennoch waren die C3H-Mäuse am Ende leichter und verfügten insgesamt über weniger braunes Fett, was nahelegt, dass ihr vorhandenes Fettgewebe stärker arbeitete, anstatt einfach größer zu werden. Bluttests deuteten ebenfalls darauf hin, dass C3H-Mäuse mehr Brennstoff mobilisierten, etwa Glycerol, um die zusätzliche Wärmeproduktion zu speisen.
Braunes und weißes Fett schließen sich dem Wärme-Team an
Um die inneren Vorgänge zu untersuchen, untersuchte das Team das braune Fett — das klassische wärmeerzeugende Gewebe — sowie zwei Arten von weißem Fett. Bei C3H-Mäusen verstärkte Kälte die Aktivität von Genen, die mit Wärmeproduktion im braunen Fett verknüpft sind, und Schlüsselproteine, die Brennstoffverbrauch und mitochondriale Aktivität unterstützen, wurden stärker aktiviert. Die Mikroskopie zeigte strukturelle Veränderungen, die zu einem aktiveren Gewebe passen. Das weiße Fett erzählte eine ähnliche Geschichte: Besonders ein Depot um die Hoden, das normalerweise langsam in wärmeerzeugende Zellen umgewandelt wird, zeigte bei C3H-Mäusen eine auffällige Aktivierung. Das deutet darauf hin, dass in diesen Tieren nicht nur braunes Fett, sondern auch traditionell als Speicher dienendes Fett rekrutiert werden kann, um den Körper warm zu halten.
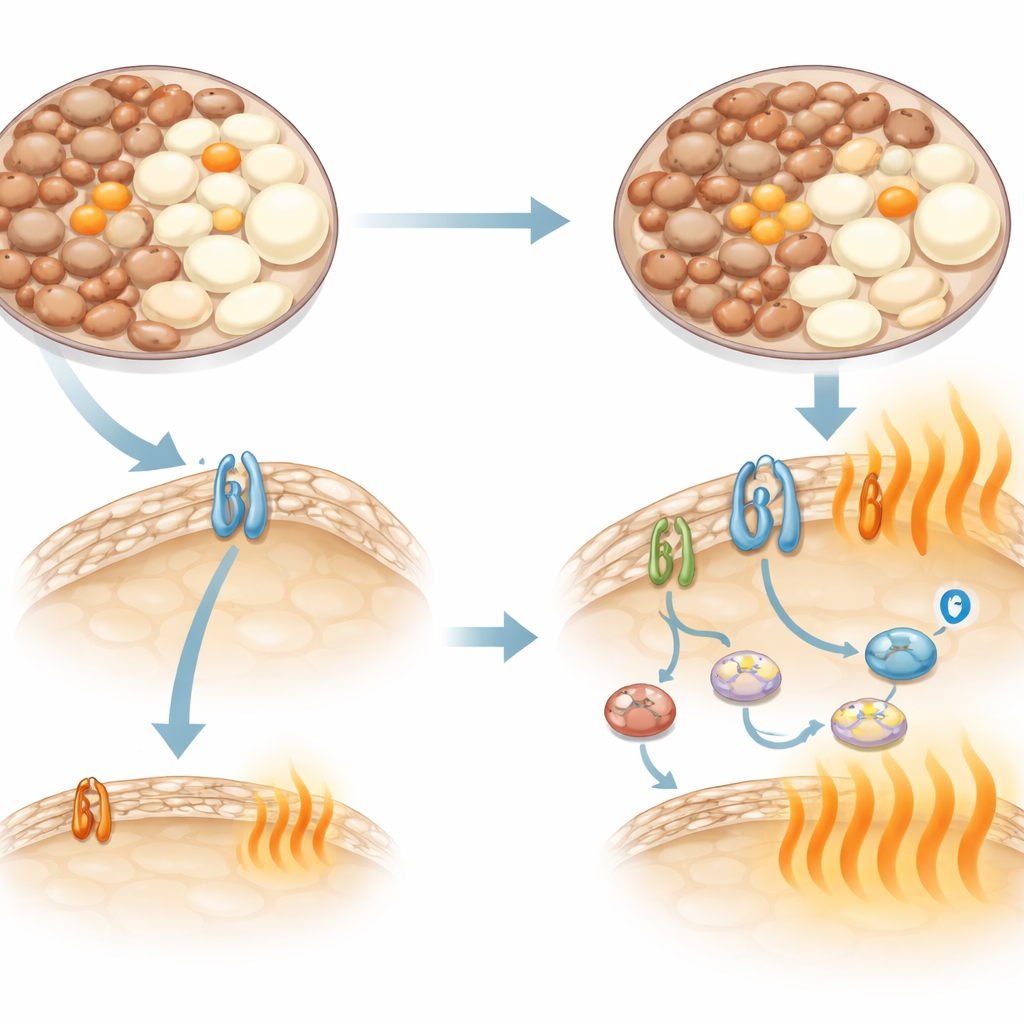
Eine andere Verdrahtung von Nervenimpulsen zum Fettgewebe
Die Wärmeproduktion im Fett wird normalerweise durch Nervenimpulse gesteuert, die über beta-adrenerge Rezeptoren auf Fettzellen wirken. Bei den standardmäßigen C57-Mäusen spielt ein Rezeptor namens Beta-3 eine wichtige Rolle, und Wirkstoffe, die ihn stimulieren, steigern den Energieverbrauch deutlich. Die Forscher bestätigten dies: Eine selektive Beta-3–zielgerichtete Verbindung verursachte bei C57-Mäusen einen großen, anhaltenden Anstieg des Energieverbrauchs. Bei C3H-Mäusen zeigte dasselbe Medikament jedoch nur eine schwache, kurzlebige Wirkung. Genuntersuchungen erklärten warum — diese Mäuse exprimierten den Beta-3-Rezeptor in ihrem Fettgewebe kaum. Dennoch erhöhten C3H-Mäuse ihren Energieverbrauch weiterhin, wenn beide Stämme Noradrenalin erhielten, ein natürliches Signal, das mehrere verwandte Rezeptoren aktiviert. Das Blockieren von Beta-1- und Beta-2-Rezeptoren beseitigte weitgehend die Stammunterschiede, was darauf hinweist, dass C3H-Mäuse stattdessen auf diese alternativen Rezeptoren und andere nicht-klassische wärmeerzeugende Wege angewiesen sind.
Was das für die Erforschung des menschlichen Stoffwechsels bedeutet
Menschen sind, ähnlich wie C3H-Mäuse, vorwiegend auf Beta-1- und Beta-2-Rezeptoren in ihrem braunen Fett angewiesen, nicht auf Beta-3. Das könnte erklären, warum auf Beta-3 ausgerichtete Wirkstoffe in typischen Mausstämmen wirkten, in klinischen Studien beim Menschen jedoch enttäuschten. Indem die Studie zeigt, dass C3H-Mäuse eine starke kälteinduzierte Wärmeproduktion mit nahezu fehlender Beta-3-Signalgebung erreichen können, hebt sie diese als ein dem Menschen ähnlicheres Modell hervor, um zu untersuchen, wie Fett Energie verbrennt. Für Leser lautet die Schlussfolgerung: Nicht alle Mäuse sind gleich — die Wahl des richtigen Stamms und der richtigen Haltungstemperatur kann die Relevanz präklinischer Forschung für die menschliche Gesundheit und für zukünftige Therapien gegen Adipositas und Stoffwechselkrankheiten deutlich erhöhen.
Zitation: Beji, S., Mouchiroud, M., Gélinas, Y. et al. Thermoregulatory adaptations to cold in C3H/HeJ mice are independent of ADRB3 signaling. Sci Rep 16, 7859 (2026). https://doi.org/10.1038/s41598-026-38538-z
Schlüsselwörter: braunes Fettgewebe, Kälteanpassung, adrenerge Signalgebung, Mausmodelle, Energieverbrauch