Clear Sky Science · de
Zielgerichtete HDAC8-Hemmung mit nicht‑Hydroxamat [1,2,4]triazolo[4,3-a]chinolin‑Verbindungen
Neue Hoffnung für eine Kinderkrebserkrankung
Das Neuroblastom ist ein aggressiver Kinderkrebs, der aus Nervenzellen entsteht und nach einer Ausbreitung oft schwer behandelbar ist. Diese Studie untersucht einen neuen Ansatz, um Neuroblastomzellen zu verlangsamen oder abzutöten, indem ein zentraler zellulärer Schalter namens HDAC8 abgeschaltet wird. Durch den Aufbau einer neuen Familie wirkstoffähnlicher Moleküle, die sehr selektiv diesen Schalter ansprechen, wollen die Forschenden Behandlungen entwickeln, die sowohl wirksamer gegen Tumore als auch schonender für den übrigen Körper sind.
Ein molekularer Schalter im Zentrum des Krebses
In unseren Zellen werden Gene ständig ein‑ und ausgeschaltet. Ein wichtiges Kontrollsystem beruht auf kleinen chemischen Markern, den Acetylgruppen, die an DNA‑assoziierte Proteine angehängt werden. Enzyme, die als Histon‑Deacetylasen (HDACs) bezeichnet werden, entfernen diese Marker, verdichten die DNA‑Verpackung und drosseln in der Regel die Genaktivität. HDAC8 ist ein Mitglied dieser Enzymfamilie und wurde mit mehreren Krebsarten, darunter Neuroblastom, in Verbindung gebracht. Wenn HDAC8 überaktiv ist, können Krebszellen leichter wachsen, überleben und sich ausbreiten, was es zu einem attraktiven Ziel für neue Medikamente macht.
Beschränkungen älterer HDAC‑Medikamente
Mehrere HDAC‑blockierende Medikamente sind bereits für einige Blutkrebserkrankungen zugelassen, treffen jedoch häufig viele HDAC‑Typen gleichzeitig. Die meisten dieser Wirkstoffe nutzen eine Hydroxamat‑Chemiegruppe, um ein Metallion in der aktiven Stelle des Enzyms zu greifen. Obwohl wirksam, bindet diese Gruppe Metalle so stark, dass sie Nebenwirkungen verursachen und die Fähigkeit des Medikaments einschränken kann, zwischen verschiedenen HDACs zu unterscheiden. Folglich können Patienten Toxizität erleben, und normale Zellen werden neben Krebszellen geschädigt. Forscher haben daher nach alternativen chemischen Designs gesucht, die die krebsbekämpfenden Vorteile erhalten und gleichzeitig unerwünschte Schäden reduzieren.
Entwurf einer neuen Klasse zielgerichteter Inhibitoren
In dieser Arbeit entwarf und synthetisierte das Team 21 neue Verbindungen, die auf einem Triazolochinolin‑Gerüst basieren und über eine flexible Verbindung an einen „alpha‑Amin‑Amid“-Bereich gebunden sind, der das Zinkatom in der aktiven Stelle von HDAC8 binden kann. Mit computerunterstütztem Design wählten sie diese Architektur, um in einen engen „Acetat‑Freisetzungskanal“ zu passen, der für HDAC8 einzigartig ist und zur hohen Spezifität beiträgt. Detaillierte Docking‑Studien und Molekulardynamik‑Simulationen zeigten, dass mehrere der neuen Moleküle – insbesondere die mit der Bezeichnung 9m und 9r – stabile, langlebige Interaktionen in der HDAC8‑Tasche ausbilden und so stark binden wie oder stärker als ein gut bekannter Referenzinhibitor. Wichtig ist, dass biochemische Tests bestätigten, dass die besten Verbindungen HDAC8 stark blockieren, während andere Mitglieder der HDAC‑Familie weitgehend verschont bleiben.
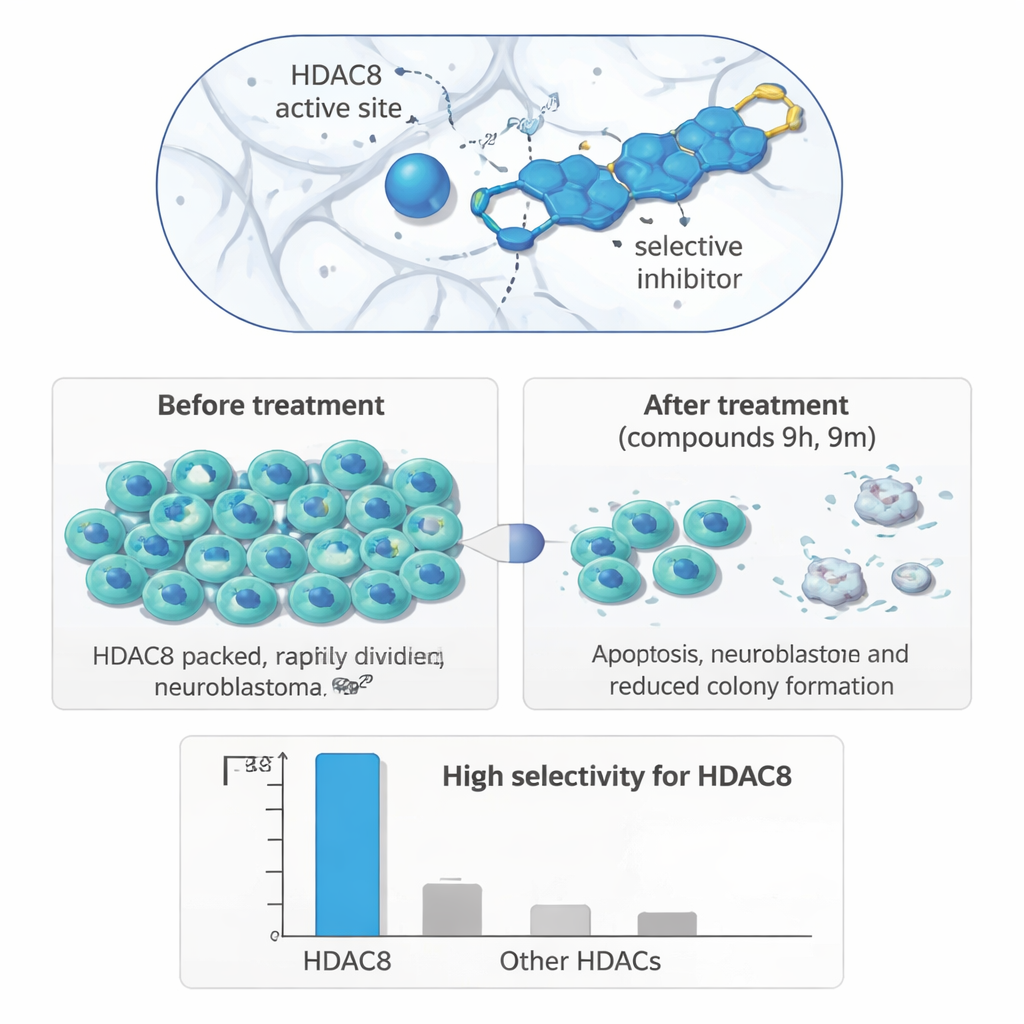
Vom Reagenzglas zu Tumorzellen
Um zu prüfen, ob diese präzise Enzymzielsteuerung in nützliche biologische Effekte übersetzt wird, testeten die Forschenden ihre Verbindungen an einer Reihe menschlicher Zelllinien. In Neuroblastomzellen (IMR‑32) stachen zwei Moleküle, 9h und 9m, deutlich hervor: Sie verminderten das Zellwachstum in Mikromolar‑Konzentrationen und wirkten dabei stärker in Neuroblastomzellen als in Brust‑ oder Darmkrebszellen oder in nicht‑krebserregenden Nierenzellen. Langzeit‑Kolonie‑Bildungsversuche zeigten, dass behandelte Neuroblastomzellen nach Medikamentenexposition einen großen Teil ihrer Fähigkeit zur Wiedervermehrung verloren. In einem Wundheilungs‑Assay, der verfolgt, wie schnell Zellen eine Kerbe in einer Zellschicht schließen, verlangsamten beide Verbindungen die Bewegung der Neuroblastomzellen, was auf ein reduziertes metastatisches Potenzial hindeutet.
Untersuchen, wie die Verbindungen Krebszellen töten
Flowzytometrie‑Experimente zeigten, dass 9h und 9m in Neuroblastomzellen programmierte Zellsterblichkeit (Apoptose) auslösen und eine Anhäufung von Zellen in einer Zellzyklusphase verursachen, die mit DNA‑Schaden oder Tod verbunden ist (Sub‑G1). Um zu bestätigen, dass diese Effekte wirklich aus der HDAC8‑Blockade stammen, maß das Team den Acetylierungszustand eines Proteins namens SMC3, eines bekannten HDAC8‑Zielproteins, das an der Zusammenhaltung von Schwesterchromatiden während der Zellteilung beteiligt ist. Wenn HDAC8 gehemmt wird, reichert sich acetyliertes SMC3 an. Nach Behandlung mit 9h oder 9m stiegen die Pegel von acetyliertem SMC3 stark an, während die Gesamtmenge an SMC3‑Protein unverändert blieb – ein starkes Indiz dafür, dass diese Verbindungen HDAC8 in lebenden Zellen direkt treffen und seine normale Funktion in der Chromosomenkontrolle stören.
Was das für künftige Therapien bedeuten könnte
Chemie, Computermodellierung, Enzymtests und zellbasierte Experimente ergeben zusammen ein stimmiges Bild: Die neu entwickelten Triazolochinolin‑Verbindungen sind potente, hochspezifische Blocker von HDAC8, die das Wachstum und die Ausbreitung von Neuroblastomzellen eindämmen können, während andere HDAC‑Enzyme geschont werden. Da sie die konventionelle Hydroxamatgruppe meiden, könnten sie einen sichereren Weg bieten, HDAC8 als therapeutisches Ziel zu nutzen. Obwohl noch viel Arbeit nötig ist – insbesondere Studien an Tieren und schließlich klinische Prüfungen – legt diese Forschung eine solide Grundlage für die Entwicklung präziserer Medikamente gegen das kindliche Neuroblastom und möglicherweise weitere durch HDAC8 getriebene Erkrankungen.
Zitation: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Schlüsselwörter: HDAC8‑Inhibitoren, Neuroblastom, epigenetische Therapie, Triazolochinolin, zielgerichtete Krebsmedikamente