Clear Sky Science · de
GluN2A-vermittelte Ströme und Calciumsignal in aus humanen iPS-Zellen gewonnenen Neuronen
Warum kleine, im Labor gezüchtete Gehirnzellen wichtig sind
Wissenschaftler wenden sich zunehmend im Labor gezüchteten menschlichen Gehirnzellen zu, um zu untersuchen, wie unser Gehirn sich entwickelt und was bei Erkrankungen wie Autismus, Epilepsie und Alzheimer schiefläuft. Diese Studie stellt eine einfache, aber entscheidende Frage: Reifen diese im Labor hergestellten Neuronen heran und verdrahten sich so, dass sie dem menschlichen Gehirn wirklich ähneln—insbesondere in der Art, wie sie mit einem wichtigen chemischen Signal namens Glutamat umgehen? Die Antwort zeigt, wie man realistischere „Mini-Gehirn“-Modelle baut und weist auf neue Wege hin, Gehirngesundheit und -krankheiten zu erforschen.
Neuronen aus umprogrammierten Zellen herstellen
Die Forscher starteten mit humanen induzierten pluripotenten Stammzellen—gewöhnliche Zellen, die zurück in einen Stammzellzustand „umprogrammiert“ wurden. Von dort lenkten sie die Zellen zu neuronalen Vorläuferzellen und schließlich zu Netzwerken aus Neuronen und unterstützenden Astrozyten, die den sich entwickelnden menschlichen Kortex nachahmen. Sie verglichen zwei weit verbreitete Protokolle bzw. Kulturbedingungen. Eines, genannt BrainPhys-Medium, ist darauf ausgelegt, aktive, elektrisch reagierende Neurone zu fördern und erzeugt tendenziell mehr Astrozyten. Das andere, ein traditionelleres Neural-Maintenance-Medium, begünstigt Neurone mit weniger Astrozyten. Über sechzig Tage verfolgte das Team, wie sich diese Kulturen im Aussehen, in der Genaktivität und in den Zelltypen veränderten, und fand, dass in BrainPhys gehaltene Kulturen elaboriertere Neuronenformen und ein Verhältnis von Neuronen zu Astrozyten entwickelten, das dem des echten menschlichen Gehirns näherkommt.
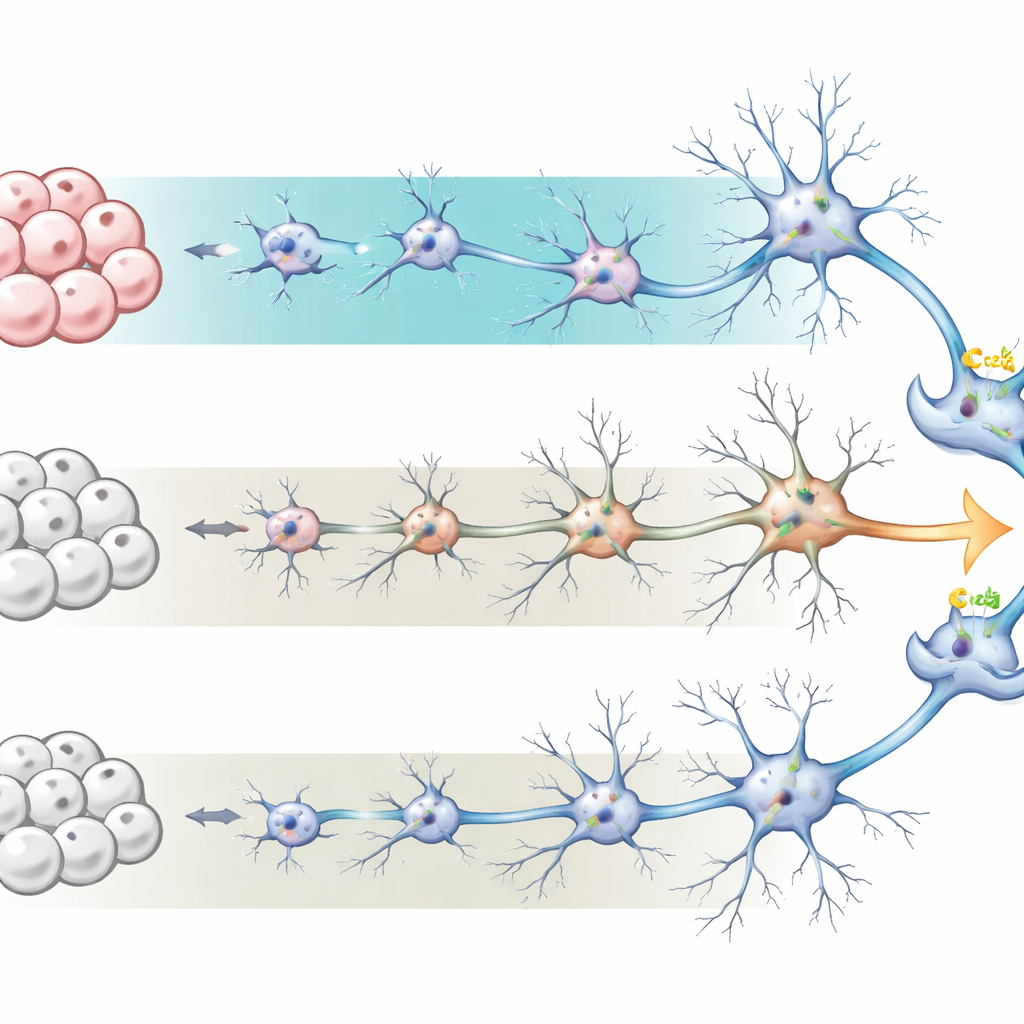
Anzeichen dafür, dass die Zellen erwachsen werden
Um einzuschätzen, wie „reif“ die Neurone waren, maß das Team die globale Genaktivität mittels RNA-Sequenzierung an Tag 60. In BrainPhys gezüchtete Zellen zeigten fast zweitausend Gene mit unterschiedlich starker Expression im Vergleich zum Standardmedium, viele davon verknüpft mit Neurondifferenzierung, Synapsenbildung und elektrischer Aktivität. Gene, die mit Astrozytenfunktion und Entzündungsreaktionen assoziiert sind, waren ebenfalls erhöht, was die größere Astrozytenpopulation widerspiegelt. Zusammen deuten diese Muster darauf hin, dass die BrainPhys-Kulturen spätere Entwicklungsstadien des Gehirns besser nachbilden, mit feineren Kommunikationspunkten zwischen Neuronen und einer unterstützenden Umgebung, die lebendem Gewebe näherkommt.
Wichtige Schalter in der chemischen Kommunikation
Ein Kennzeichen der Gehirnreifung ist ein Wechsel in der Zusammensetzung der NMDA-Rezeptoren—molekulare Tore auf Neuronen, die als Reaktion auf Glutamat öffnen und beim Aufbau lernbezogener Verbindungen helfen. Früh in der Entwicklung dominiert eine Untereinheit namens GluN2B; später übernimmt GluN2A, was beeinflusst, wie lange und wie stark die Rezeptoren geöffnet bleiben. Mittels Mikroskopie zeigte das Team, dass im Laufe der Zeit mehr NMDA-Rezeptoren in Synapsen, den Kontaktpunkten zwischen Neuronen, lokalisiert wurden, besonders in BrainPhys-Kulturen. Gezielte Genmessungen ergaben einen Rückgang der „frühen“ GluN2B-Untereinheit und einen Anstieg der „späteren“ GluN2A-Untereinheit, was darauf hinweist, dass die Neurone diesen klassischen Entwicklungswechsel durchlaufen.
Ströme und Calciumverläufe innerhalb der Zellen verfolgen
Funktionelle Tests bestätigten, dass diese molekularen Veränderungen von Bedeutung sind. Mit feinspitzigen Elektroden zeichneten die Forscher elektrische Ströme auf, die durch NMDA ausgelöst wurden, eine Substanz, die selektiv NMDA-Rezeptoren aktiviert. Neurone aus beiden Kulturbedingungen zeigten robuste Ströme, doch die Blockade der GluN2A-Untereinheit reduzierte diese Ströme um etwa die Hälfte, was demonstriert, dass GluN2A nun eine wichtige Rolle im Signalfluss spielt. Das Team verfolgte anschließend Calcium, einen wichtigen intrazellulären Botenstoff, mithilfe eines fluoreszenten Farbstoffs. Bei NMDA-Exposition zeigte ein deutlich größerer Anteil der in BrainPhys gezüchteten Neurone starke Calciumanstiege, und die Amplitude des Signals war größer. Genanalysen legen dar, warum: BrainPhys-Kulturen reglementierten mehrere Komponenten von Calciumkanälen und -freisetzungswegen hoch und rüsteten die Zellen somit aus, NMDA-Rezeptoraktivierung in weitreichende, koordinierte Calciumantworten zu übersetzen.
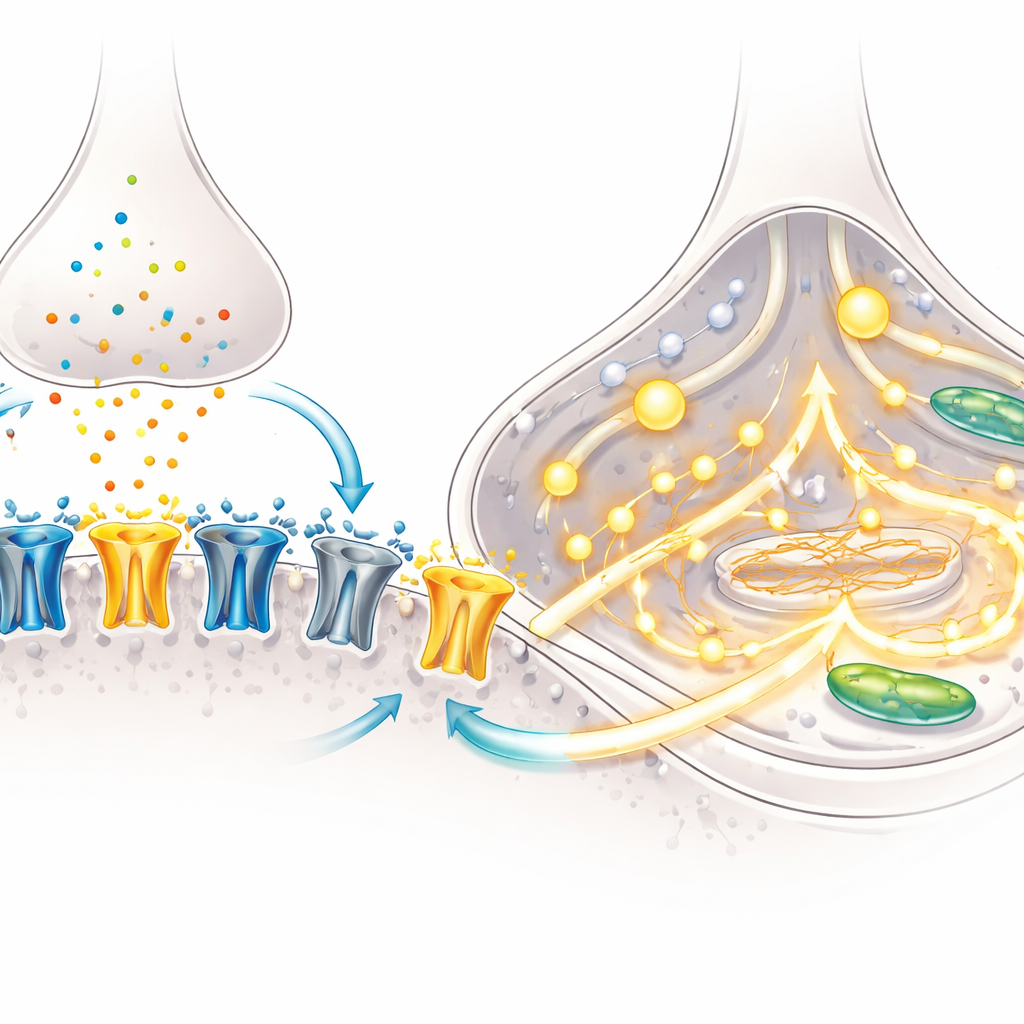
Was das für die Erforschung von Gehirnerkrankungen bedeutet
Zusammen zeigen diese Befunde, dass aus humanen Stammzellen gewonnene Neurone in nur zwei Monaten einen funktionell reifen Zustand erreichen können, besonders wenn sie unter Bedingungen gezüchtet werden, die aktive Netzwerke und ein realistisches Verhältnis von Neuronen zu Astrozyten begünstigen. In diesem Zustand dominiert die „erwachsen-ähnliche“ GluN2A-Untereinheit die NMDA-Rezeptorströme und trägt stark zur Calcium-Signalgebung bei, ähnlich wie im sich entwickelnden menschlichen Gehirn. Für Nichtfachleute ist die Schlussfolgerung, dass Forschern nun ein treueres Labormodell zur Verfügung steht, um zu untersuchen, wie menschliche exzitatorische Neurone heranreifen, sich vernetzen und auf Glutamat reagieren. Das ermöglicht es, zu erforschen, wie subtile genetische Veränderungen oder Krankheitsprozesse diese fein abgestimmten Schalter stören—einblicke, die von Epilepsie bis zu Alzheimer reichen und die Entwicklung sowie Prüfung zukünftiger Therapien leiten können.
Zitation: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Schlüsselwörter: NMDA-Rezeptoren, Stammzell-Neuronen, Gehirnentwicklung, Calcium-Signalgebung, synaptische Reifung