Clear Sky Science · de
Der duale G9a-Inhibitor und Histamin-H3-Rezeptor-Antagonist A-366 verbessert repetitive und soziale Verhaltensweisen und dämpft Neuroinflammation bei BTBR T + tf/J-Mäusen
Warum diese Mausstudie für Autismus wichtig ist
Familien mit Angehörigen im Autismus-Spektrum (ASD) sehen sich oft einem Flickenteppich von Behandlungen gegenüber, die jeweils nur einige Symptome lindern. Diese Studie untersucht eine neue experimentelle Verbindung namens A-366, die so entwickelt wurde, dass sie gleichzeitig auf zwei sehr unterschiedliche biologische Systeme wirkt. In einem weit verbreiteten Mausmodell für autismusähnliches Verhalten verringerte A-366 repetitive Handlungen, verbesserte die soziale Interaktion und beruhigte Entzündungsreaktionen im Gehirn. Das deutet darauf hin, dass künftig ein einzelnes Medikament mehrere Kernmerkmale von ASD gleichzeitig angehen könnte.
Eine Störung mit vielen beteiligten Prozessen
ASD ist keine einzelne Krankheit mit einer einzigen Ursache. Sie umfasst Schwierigkeiten in der sozialen Kommunikation, repetitive Verhaltensweisen und häufig weitere Herausforderungen wie Angst oder Aufmerksamkeitsprobleme. Hinter diesen äußeren Anzeichen verbirgt sich ein Netz aus Veränderungen in der Gehirnchemie und der Genregulation. Aktuelle Medikamente, etwa das Antipsychotikum Aripiprazol, zielen hauptsächlich auf Neurotransmittersysteme wie Dopamin und Serotonin und sind nur für assoziierte Symptome wie Reizbarkeit zugelassen. Gleichzeitig hat die Forschung gezeigt, dass die Art und Weise, wie DNA in Gehirnzellen verpackt und chemisch markiert ist – die Epigenetik – sich bei ASD verändert, ebenso wie die Aktivität der immunen und entzündlichen Reaktionen im Gehirn. Diese mehreren Ebenen legen nahe, dass ein Ansatz, der jeweils nur ein Ziel adressiert, zu eng gefasst sein könnte.
Gene-Schalter und Botenstoffe zugleich treffen
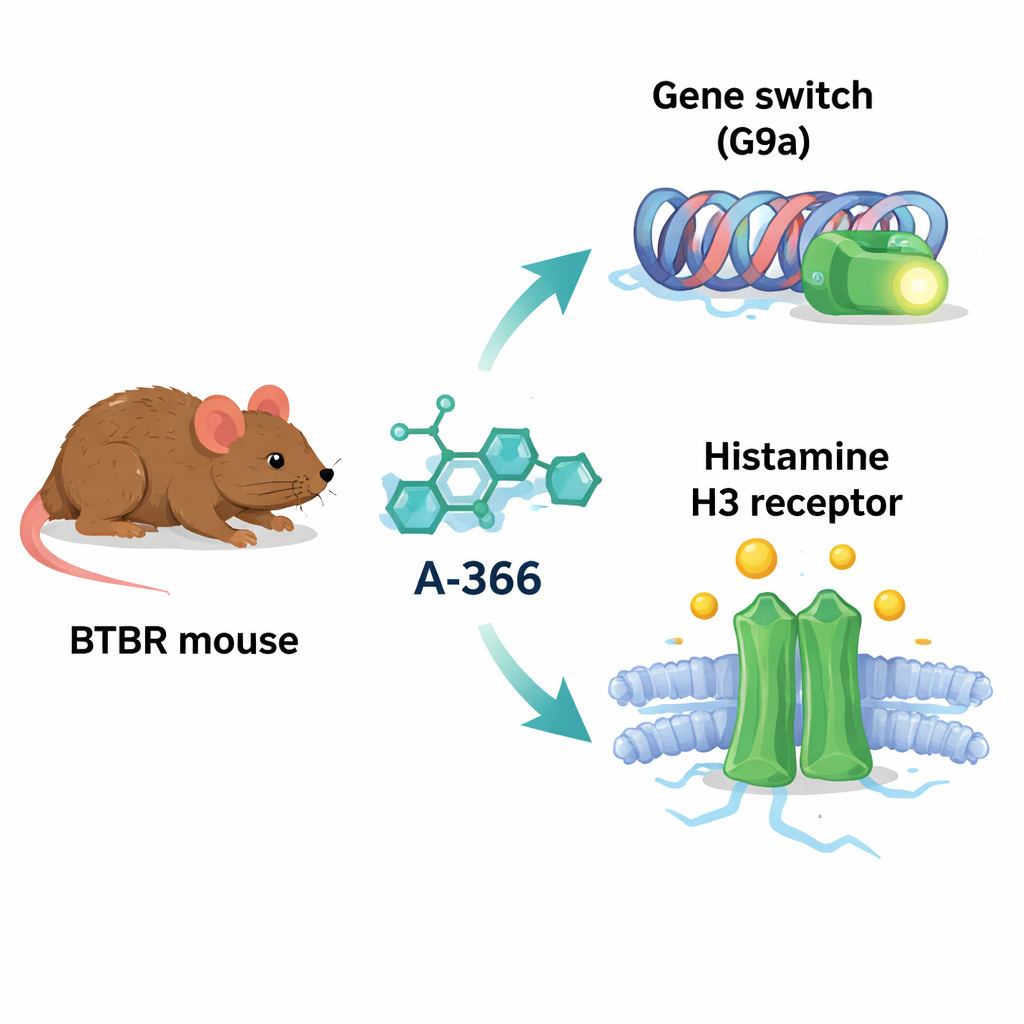
A-366 wurde ursprünglich entwickelt, um ein Protein namens G9a zu blockieren, ein Enzym, das chemische Markierungen an Histonproteinen anbringt und dadurch Gene in der Regel herunterreguliert. Bei mehreren Hirnstörungen sind G9a-Aktivität und seine Markierungen erhöht, wodurch möglicherweise Gene abgeschaltet werden, die für Lernen, Gedächtnis und eine gesunde neuronale Verschaltung wichtig sind. Interessanterweise ähnelt die chemische Struktur von A-366 auch der von Substanzen, die den Histamin-H3-Rezeptor blockieren – einem Schalter, der die Freisetzung von Histamin und anderen Transmittern kontrolliert und mit Aufmerksamkeit, Wachheit und Sozialverhalten in Verbindung gebracht wird. Aufgrund dieser Überschneidung vermuteten die Autorinnen und Autoren, dass A-366 als „Dualwirkstoff“ fungieren könnte: indem es schädliche Genabschaltungen durch G9a-Hemmung lockert und gleichzeitig das Histaminsignal durch Blockade des H3-Rezeptors erhöht.
A-366 im Test bei autismusähnlichen Mäusen
Das Team arbeitete mit BTBR T+tf/J-Mäusen, einer Linie, die von Natur aus geringe Sozialisierung, starkes repetitives Putzen und Graben sowie erhöhte Gehirn-Entzündungswerte zeigt – Merkmale, die zentrale Aspekte von ASD widerspiegeln. Männliche BTBR-Mäuse erhielten drei Wochen lang täglich Injektionen von A-366 in drei verschiedenen Dosen; ihr Verhalten wurde mit typischen C57-Mäusen sowie mit BTBR-Mäusen verglichen, die entweder mit Pitolisant (einem Standard‑H3-Rezeptorblocker) oder mit Aripiprazol behandelt wurden. In mehreren Tests verringerte A-366 dosisabhängig repetitives Graben, Zerreißen von Material und ausgiebiges Putzen und verbesserte die Leistung im Y‑Maze, einem Test des räumlichen Arbeitsgedächtnisses. In einem Drei-Kammer-Social-Test stellte A-366 nicht nur die Präferenz der Mäuse wieder her, Zeit mit einem Artgenossen statt in einem leeren Käfig zu verbringen, sondern hob bei der höchsten Dosis die Sozialwerte auf das Niveau typischer Mäuse und übertraf damit die Effekte von Pitolisant und Aripiprazol.
Entzündung dämpfen und Ziele bestätigen
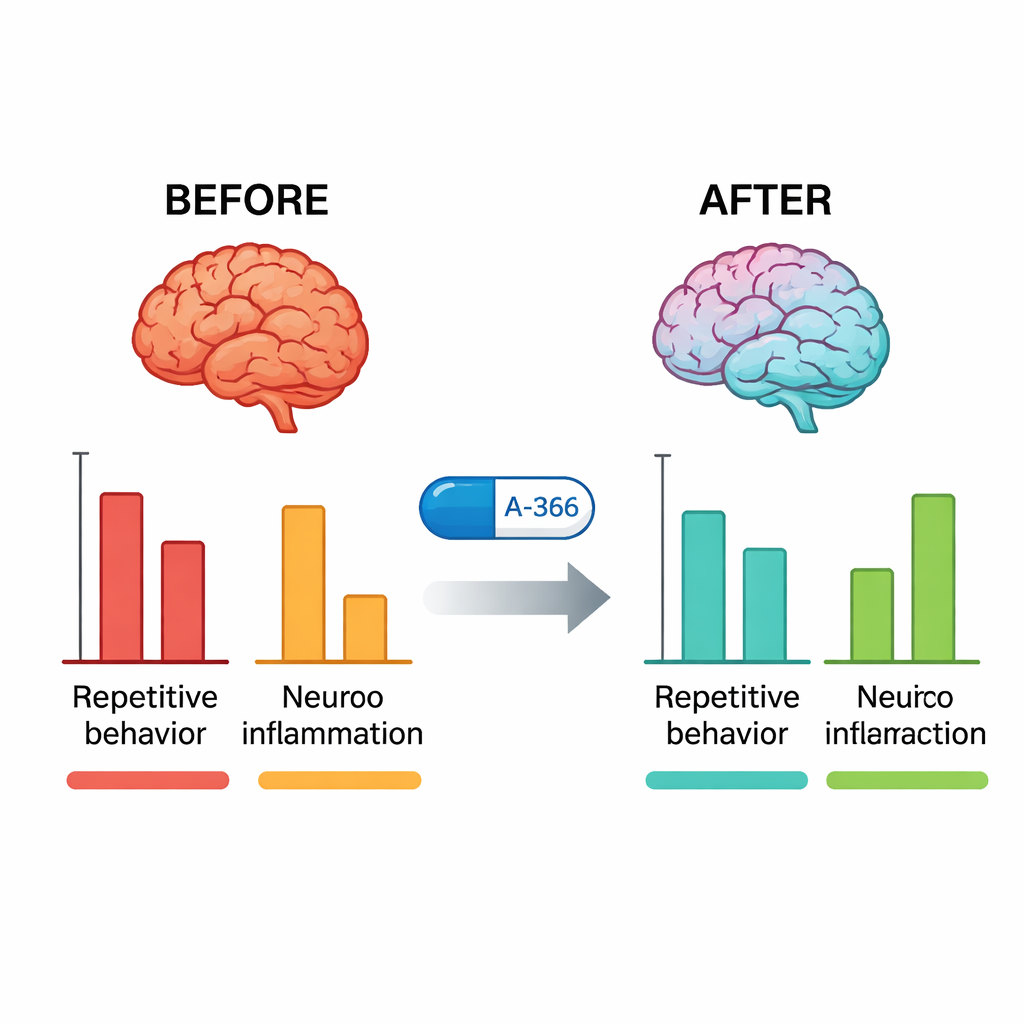
Nach den Verhaltenstests untersuchten die Forschenden die Gehirne der Mäuse. Bei unbehandelten BTBR-Mäusen war die G9a-Aktivität im Hippocampus und Kleinhirn deutlich höher als bei typischen Mäusen. Die Behandlung mit A-366 reduzierte diese Aktivität stark zurück in Richtung Normalwert, während Pitolisant allein dies nicht bewirkte, was bestätigt, dass A-366 wirklich sein epigenetisches Ziel adressiert. Gleichzeitig waren Schlüsselmoleküle der Entzündung – TNF-α, IL-6 und IL-1β – bei BTBR-Mäusen stark erhöht und wurden durch A-366 signifikant gesenkt, mehr noch als durch Aripiprazol. Als die Wissenschaftler zusätzlich zu A-366 ein Mittel gaben, das H3-Rezeptoren aktiviert (RAMH), kehrten sich die Verhaltens- und antiinflammatorischen Vorteile nur teilweise um, und der Rückgang der G9a‑Aktivität blieb bestehen. Dieses Muster stützt einen kombinierten Wirkmechanismus: stabile epigenetische Entlastung durch G9a‑Hemmung plus einen histaminvermittelten Beitrag durch H3‑Rezeptorblockade.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten legen diese Befunde nahe, dass es möglich sein könnte, Medikamente zu entwickeln, die zugleich an der „Software“ und am „Botensystem“ des Gehirns ansetzen. In diesem Mausmodell autismusähnlichen Verhaltens milderte A-366 repetitive Aktionen, verbesserte soziale Interaktion und reduzierte Anzeichen chronischer Gehirnentzündung, indem es schädliche Genabschaltungen lockerte und gleichzeitig das Histaminsignal anpasste. A-366 selbst wurde ursprünglich für andere Erkrankungen entwickelt und müsste vor einer Anwendung am Menschen optimiert und umfassend auf Sicherheit geprüft werden. Dennoch liefert es eine Blaupause für eine neue Klasse von Mehrfachziel‑Wirkstoffen, die auf die komplexe Biologie von ASD abzielen, bei der die Behandlung nur eines einzelnen Weges bislang nur begrenzte Erleichterung brachte.
Zitation: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Schlüsselwörter: Autismus-Spektrum-Störung, epigenetische Therapie, Histamin-H3-Rezeptor, Neuroinflammation, Mausmodell