Clear Sky Science · de
aFGF rettet durch hohen Blutzucker induzierte seneszente Fibroblasten und verbessert die Heilung diabetischer Wunden durch Regulation des SIRT1/STAT3-Signalwegs
Warum langsam heilende Wunden wichtig sind
Für viele Menschen mit Diabetes kann ein kleiner Schnitt am Fuß oder Bein zu einer hartnäckigen Wunde werden, die monatelang bestehen bleibt und manchmal zu Infektionen oder sogar Amputationen führt. Diese chronischen Geschwüre sind nicht nur ein Oberflächenproblem: Die Hautzellen, die das geschädigte Gewebe wiederaufbauen sollten, altern oft vorzeitig und verlieren ihre Funktion. Diese Studie untersucht einen vielversprechenden Weg, einige dieser Zellen mithilfe eines natürlich vorkommenden Reparatursignals zu »verjüngen«, mit dem Ziel, diabetische Wunden schneller und vollständiger zu verschließen.
Zellen, die zu früh altern
Gesunde Haut ist auf Fibroblasten angewiesen — Stütz-Zellen in den tieferen Hautschichten — die sich vermehren, in eine Wunde einwandern und ein neues Gerüst für Gewebe aufbauen. Bei Diabetes treiben chronisch hoher Blutzucker und zuckerbedingte geschädigte Moleküle diese Fibroblasten in einen Zustand, der als zelluläre Alterung oder Seneszenz bezeichnet wird. Seneszente Fibroblasten teilen sich kaum noch, produzieren weniger der für die Reparatur nötigen Strukturproteine und schütten stattdessen einen Cocktail von entzündungsfördernden Faktoren aus, der die anhaltende Entzündung nährt. Die Autoren zeigen, dass bei diabetischen Ratten die Haut um eine Wunde mehr dieser gealterten Fibroblasten und weniger der hilfreichen Matrixproteine enthält, was mit deutlich verlangsamter Heilung korreliert.
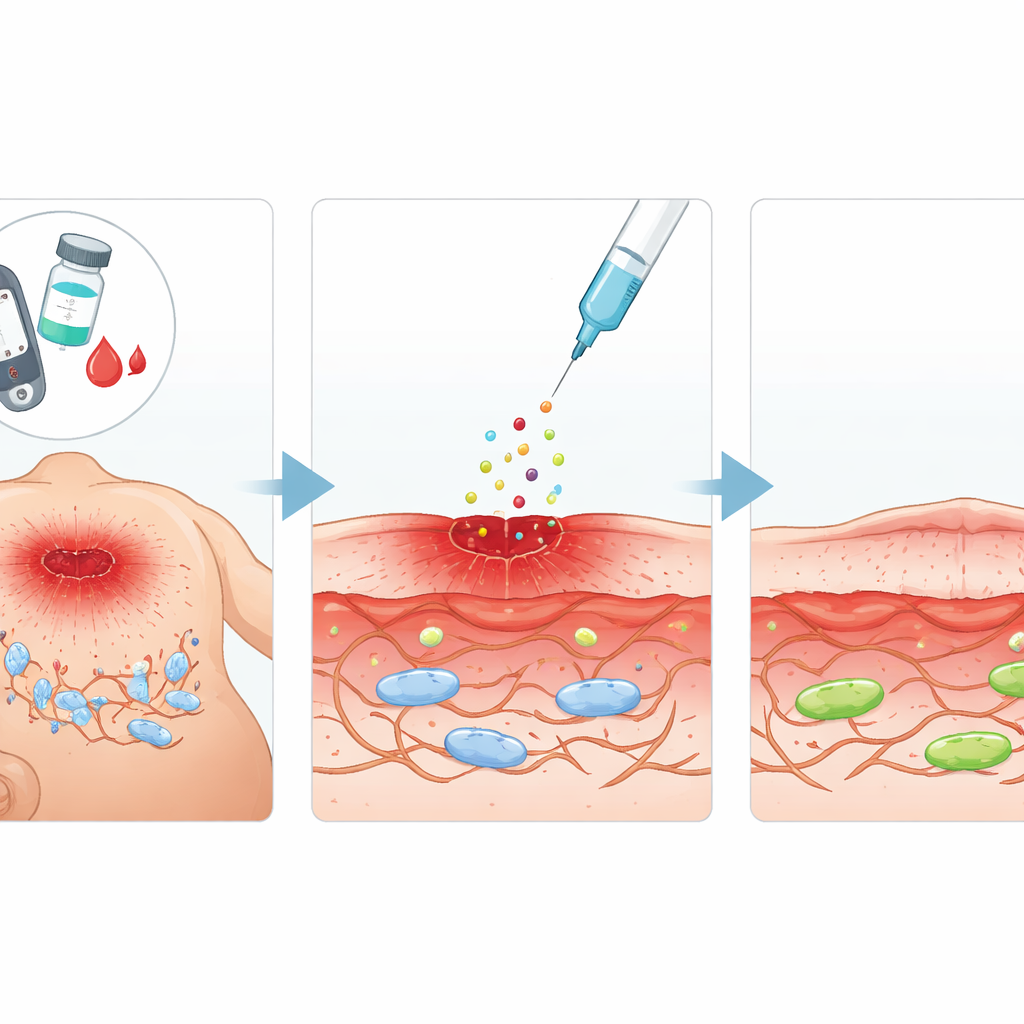
Ein vielversprechendes Reparatursignal
Das Team konzentrierte sich auf den sauren Fibroblasten-Wachstumsfaktor (aFGF), ein natürliches Protein, das bekanntermaßen Zellwachstum und Gewebereparatur fördert. Sie fragten, ob aFGF nicht nur die Aktivität von Fibroblasten steigern, sondern auch altersähnliche Veränderungen rückgängig machen kann, die durch hohen Zucker ausgelöst werden. Bei diabetischen Ratten wurden standardisierte Hautwunden angelegt und alle paar Tage aFGF um das verletzte Gebiet injiziert. Im Vergleich zu unbehandelten diabetischen Tieren zeigten aFGF-behandelte Ratten eine schnellere Verkleinerung der Wundfläche, eine bessere Wiederherstellung des darunterliegenden Gewebes und niedrigere Werte von Markern, die zelluläre Alterung anzeigen. In parallelen Laborversuchen mit einer Maus-Fibroblasten-Zelllinie, die sehr hohem Glukose ausgesetzt war, stellte aFGF die Teilungs- und Wanderungsfähigkeit der Zellen wieder her — zwei Verhaltensweisen, die für das Verschließen einer Wunde wesentlich sind.
Reduzierung des oxidativen Stresses in den Zellen
Hoher Blutzucker bewirkt mehr, als Zellen nur mit zusätzlichem Brennstoff zu überfluten: Er fördert auch die Überproduktion reaktiver Sauerstoffspezies, instabiler Moleküle, die Proteine, Fette und DNA schädigen. Dieser oxidative Stress ist ein wichtiger Auslöser dafür, dass Fibroblasten seneszent werden. Die Forschenden maßen in ihrem Zellmodell mehrere gängige Indikatoren dieses Stresses, darunter schädliche Abbauprodukte und die Aktivität der zelleigenen Antioxidans-Enzyme. Unter hohem Glukosegehalt zeigten Fibroblasten mehr Schäden und schwächere antioxidative Abwehr. Nach Zugabe von aFGF verschob sich das Gleichgewicht: Schädliche Marker sanken und schützende Enzyme wurden aktiver. Dies deutet darauf hin, dass aFGF hilft, ein gesünderes inneres Milieu wiederherzustellen, wodurch Fibroblasten weniger wahrscheinlich in einen dauerhaft gealterten Zustand abgleiten.
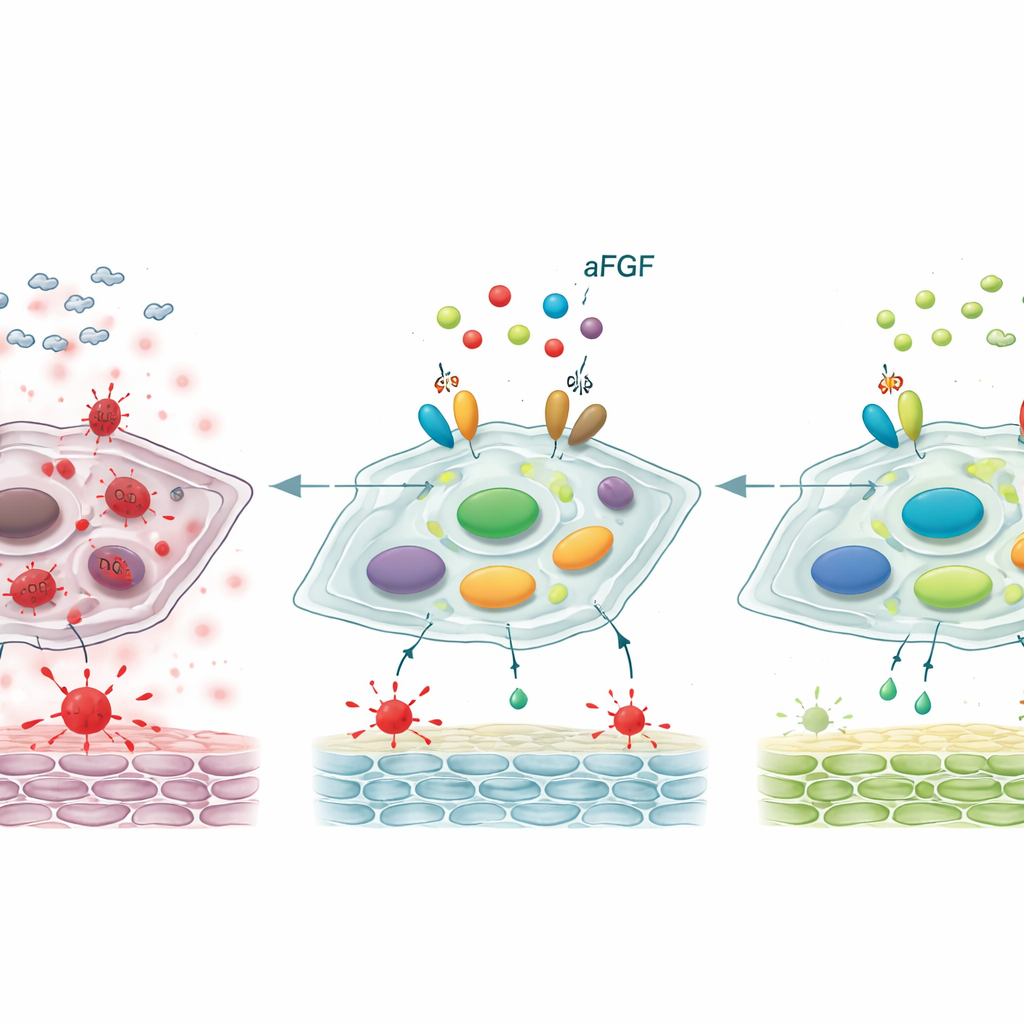
Zurücksetzen eines wichtigen Kontrollschalters
Auf molekularer Ebene untersuchten die Wissenschaftler eine Steuerachse, die zwei Proteine umfasst — SIRT1 und STAT3 — die gemeinsam beeinflussen, ob Fibroblasten jugendlich bleiben oder seneszent werden. In diabetischen Wunden und in Zellen, die mit hohem Glukose behandelt wurden, waren die Spiegel von SIRT1, einem Beschützer, der mit Stressresistenz assoziiert ist, reduziert, während die aktivierte Form von STAT3 — ein Treiber von Alterungs- und entzündlichem Verhalten — erhöht war. Die Behandlung mit aFGF kehrte dieses Muster um: SIRT1 stieg und aktiviertes STAT3 nahm ab. Als das Team SIRT1 mit einem spezifischen Inhibitor blockierte, verlor aFGF weitgehend seine Fähigkeit, oxidativen Stress zu reduzieren, Altersmarker zu dämpfen und die Wundheilung bei Ratten zu beschleunigen. Dies deutet darauf hin, dass die vorteilhaften Effekte von aFGF stark davon abhängen, SIRT1 wieder zu aktivieren, das seinerseits STAT3 und das schädliche Alterungsprogramm in Schach hält.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass aFGF mehr bewirkt als nur das Anregen von Zellwachstum. Es scheint überarbeitete Fibroblasten in diabetischen Wunden aus einem destruktiven Alterungszyklus zu retten, den oxidativen Stress zu lindern und einen wichtigen molekularen Schalter zurückzusetzen, sodass diese Zellen wieder am Wiederaufbau des Gewebes mitwirken können. Obwohl die Arbeit an Ratten und in Kulturen durchgeführt wurde und reale diabetische Wunden noch komplexer sind als die hier verwendeten Modelle, weisen die Resultate auf aFGF als vielversprechenden Kandidaten für künftige Therapien hin. Falls ähnliche Vorteile beim Menschen bestätigt werden, könnte eine gezielte aFGF-Therapie eines Tages chronischen diabetischen Geschwüren helfen, schneller zu heilen, Schmerzen und Infektionsrisiko zu verringern und die Wahrscheinlichkeit schwerer Komplikationen zu senken.
Zitation: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Schlüsselwörter: Heilung diabetischer Wunden, Fibroblastenalterung, oxidativer Stress, Wachstumsfaktortherapie, SIRT1 STAT3 Signalweg