Clear Sky Science · de
Radiomische Merkmale und Karotisstenose bei Parodontitis: eine zweistufige Bootstrap- und multimodale Machine-Learning-Studie
Warum Ihr Zahnfleisch etwas über Ihr Herz verraten könnte
Die meisten von uns sehen Zahnaufnahmen primär als Mittel, Karies zu erkennen oder Implantate zu planen. Diese Studie legt nahe, dass sie auch Hinweise auf die Gesundheit der Halsarterien liefern könnten, die das Gehirn versorgen. Indem sie verborgene Muster in routinemäßigen 3D-Zahnscans von Menschen mit Zahnfleischerkrankung auswerten, zeigen die Forschenden, dass es möglich sein könnte, Personen zu identifizieren, die ein erhöhtes Risiko für gefährliche Gefäßverengungen haben — und das lange bevor ein Schlaganfall eintritt.
Versteckte Warnsignale im Mund
Parodontitis ist eine chronische Entzündung, die langsam die Gewebe zerstört, die unsere Zähne stützen. In den letzten zehn Jahren haben zahlreiche Studien einen Zusammenhang mit Herzinfarkten und Schlaganfällen gezeigt und angedeutet, dass entzündetes Zahnfleisch und erkrankte Blutgefäße zwei Seiten derselben Problematik sein könnten. Dennoch fehlen Ärzten noch einfache, praktikable Werkzeuge, um aus den Patienten mit Parodontitis diejenigen herauszufiltern, die im Stillen eine Verengung der Halsschlagader entwickeln — eine Hauptursache für ischämische Schlaganfälle. Die Autoren fragten, ob die in Zahnarztpraxen bereits verwendeten 3D-Cone-Beam-CT-Scans subtile strukturelle Hinweise enthalten könnten, die diesen versteckten Gefäßschaden widerspiegeln.
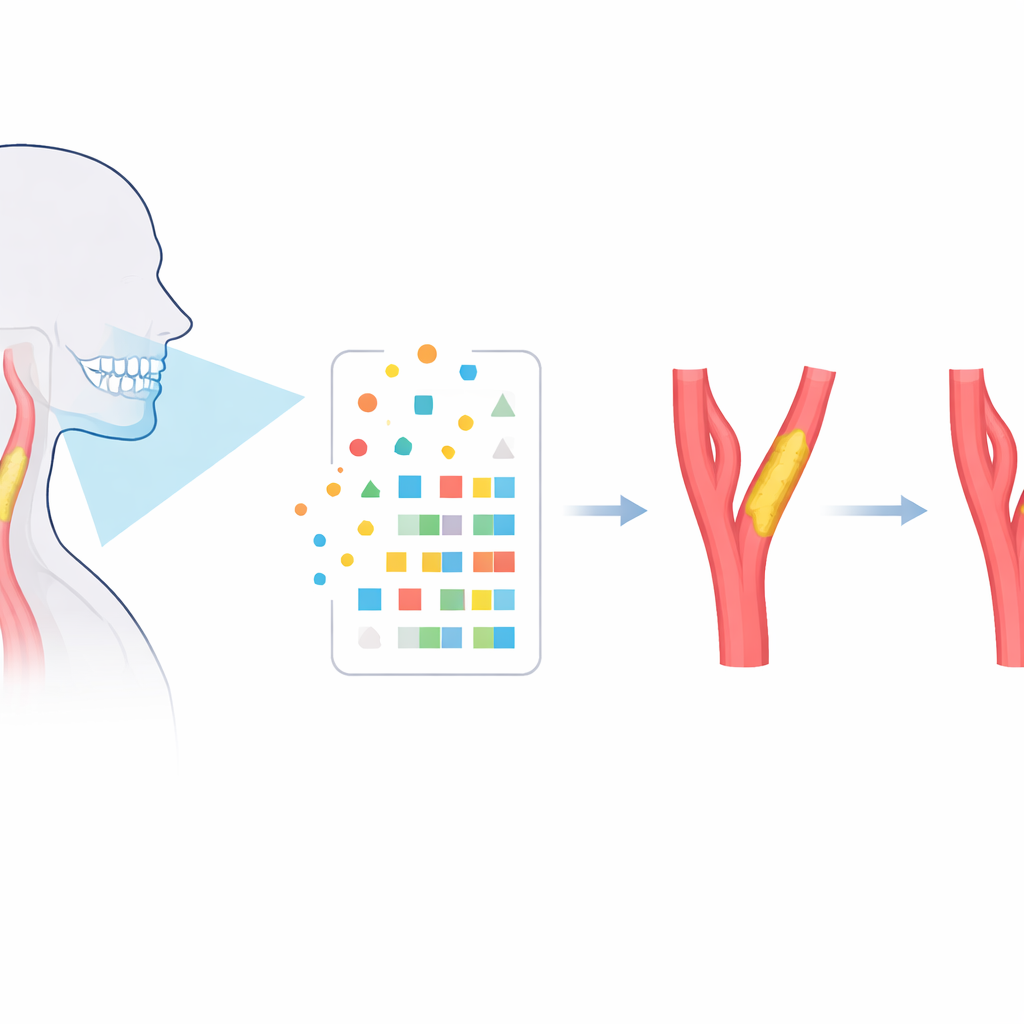
Zahnscans in messbare Muster verwandeln
Das Team analysierte Cone-Beam-CT-Scans von 279 Erwachsenen, die an einem großen Krankenhaus behandelt wurden: 168 hatten sowohl Parodontitis als auch eine Verengung der Halsschlagader, während 111 nur Parodontitis hatten. Für jede Person markierten Fachleute sorgfältig die Ober- und Unterkieferbereiche, die die Zähne und den stützenden Knochen umfassen. Mittels Radiomics — einer Technik, die medizinische Bilder in zahlreiche numerische Beschreibungen übersetzt — extrahierten sie 206 Merkmale pro Scan. Dazu gehörten einfache Messgrößen wie die Gesamthelligkeit ebenso wie Form- und Texturmuster, die mit bloßem Auge nicht zu erkennen sind, aber widerspiegeln können, wie Entzündung und Knochenumbau den Kiefer im Laufe der Zeit verändert haben.
Maschinen beibringen, gefährdete Patienten zu erkennen
Da in der Studie mehr Patienten mit erkrankten Arterien als gesunden Verhältnissen vertreten waren, verwendeten die Forschenden eine Daten-Ausgleichsmethode namens SMOTE, um ein ausgewogeneres Trainingsset für ihre Algorithmen zu schaffen. Anschließend wendeten sie einen sorgfältigen zweistufigen statistischen Prozess an, um die 206 radiomischen Merkmale zu sichten. Zuerst resampelten sie wiederholt die Daten und nutzten Korrelationsprüfungen sowie ein regularisiertes Regressionsverfahren, um redundante oder schwache Signale auszusondern. Merkmale, die dieses Auswahlverfahren wiederholt überstanden, gelangten in eine zweite Phase, in der wiederholte logistische Regressionsläufe die stabilste Kombination auswählten. Am Ende blieben 20 Schlüsselmerkmale übrig — bezüglich Kieferform, Intensitätsverteilung und feinkörniger Textur — die zusammen am besten zwischen Patienten mit und ohne Karotisstenose unterschieden.
Wie gut die Modelle arbeiteten
Mit diesen 20 Merkmalen bauten und verglichen die Forschenden drei gängige Machine-Learning-Modelle: logistische Regression, Support Vector Machines und Random Forests. Mithilfe einer Fünffach-Cross-Validation — einer Methode, die die Leistung an bisher ungesehenen Daten testet — ergab sich, dass das Random-Forest-Modell am besten abschnitt. Es trennte Hochrisiko- von Niedrigrisiko-Patienten mit einer Fläche unter der Kurve (AUC) von 0,892 korrekt, zeigte eine sehr hohe Sensitivität (es erkannte etwa 96 % der Patienten mit Gefäßverengung) und eine moderate Spezifität (etwa 71 % derjenigen ohne Verengung wurden korrekt beruhigt). Zusätzliche Prüfungen zeigten, dass seine Wahrscheinlichkeitsabschätzungen einigermaßen realitätsnah waren und dass es über einen breiten Bereich von Entscheidungsgrenzen hinweg Ärzten einen größeren Netto-Nutzen bieten würde als die einfacheren Modelle oder die Strategie, alle Patienten mit Gefäßuntersuchungen zu screenen.
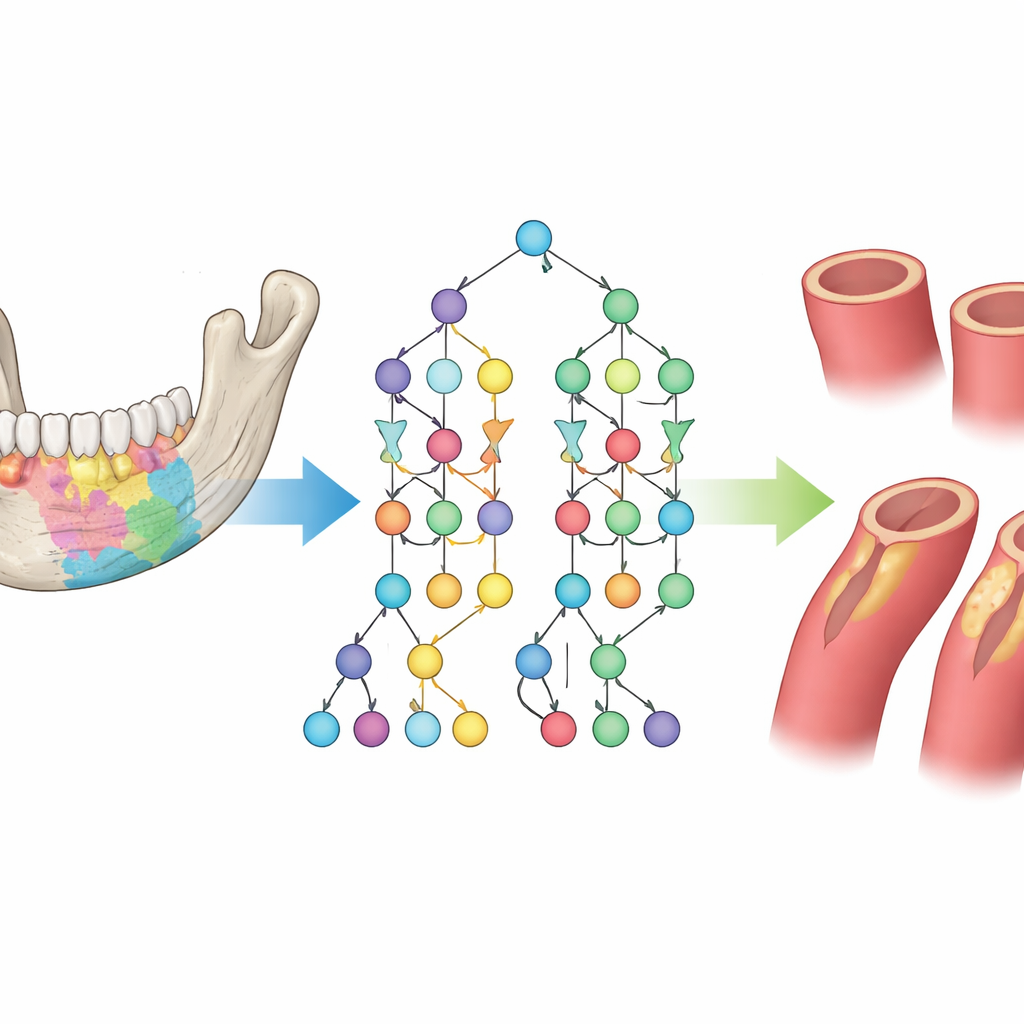
Was das für die tägliche Versorgung bedeuten könnte
Die Ergebnisse deuten darauf hin, dass ein einziger Kieferscan, der aus zahnmedizinischen Gründen aufgenommen wurde, eines Tages auch als Frühwarnsystem für Schlaganfallrisiken dienen könnte — besonders bei Patienten mit chronischer Zahnfleischerkrankung. Da Cone-Beam-CT in zahnärztlichen und oralchirurgischen Praxen bereits weit verbreitet ist, könnte ein solcher Ansatz viele Menschen ohne zusätzliche Aufnahmen, Nadeln oder Zeitaufwand screenen und nur diejenigen, die als höheres Risiko eingestuft werden, an vaskuläre Ultraschalluntersuchungen oder andere Herz‑und-Gefäß-Tests weiterleiten.
Wo uns die Befunde jetzt zurücklassen
Diese Arbeit erhebt nicht den Anspruch, dass Zahnärzte heute Arterienerkrankungen allein aus Röntgenaufnahmen diagnostizieren können. Die Studie wurde an einem Zentrum durchgeführt, stützte sich teilweise auf synthetische Daten zur Ausbalancierung der Fälle und wurde noch nicht in anderen Kliniken oder mit anderen Scannern validiert. Dennoch bietet sie einen Machbarkeitsnachweis: Subtile Muster in den Knochen um unsere Zähne scheinen das zu spiegeln, was in den Halsschlagadern geschieht, die das Gehirn versorgen. Wenn diese Ergebnisse bestätigt und verfeinert werden, könnten solche Modelle helfen, die Mundgesundheit enger in das gesamte kardiovaskuläre Screening einzubeziehen und einen Zahnarztbesuch zur Chance machen, nicht nur unser Lächeln, sondern auch Gehirn und Herz zu schützen.
Zitation: Zhang, M., Cai, J., Cao, Q. et al. Radiomic features and carotid stenosis in periodontitis a two stage bootstrap and multimodal machine learning study. Sci Rep 16, 8177 (2026). https://doi.org/10.1038/s41598-026-38463-1
Schlüsselwörter: Parodontitis, Karotidatherosklerose, Radiomics, Machine Learning, frühes Schlaganfallrisiko