Clear Sky Science · de
In silico-Entdeckung eines multi‑target Inhibitors aus Naturstoffen für die Therapie der Huntington‑Krankheit
Ein neuer Blick auf eine verheerende Gehirnkrankheit
Die Huntington‑Krankheit ist eine seltene, aber verheerende Erkrankung des Gehirns, die den Betroffenen nach und nach Bewegung, Denkvermögen und Selbstständigkeit raubt. Die heutigen Medikamente können einige Symptome lindern, doch sie stoppen oder kehren die Krankheit nicht um. Diese Studie untersucht einen neuen, computerbasierten Weg zur Suche nach Therapien: das gezielte Auffinden einer einzelnen natürlichen Verbindung, die mehrere Schwachstellen im Krankheitsprozess gleichzeitig angreift — ein Ansatz, der wirksamer sein könnte als Mittel, die nur auf ein einziges Ziel gerichtet sind.
Warum Huntington so schwer zu behandeln ist
Die Huntington‑Krankheit wird durch ein fehlerhaftes Gen verursacht, das zum allmählichen Abbau von Nervenzellen führt, meist beginnend im mittleren Lebensalter. Anfangs fallen oft subtile Stimmungsschwankungen, kleine unwillkürliche Bewegungen oder leichte Probleme bei Planung und Konzentration auf. Innerhalb von 10 bis 12 Jahren kann sich dies zu schweren Bewegungsstörungen, Sprachverlust, Demenz und vollständiger Pflegebedürftigkeit entwickeln. Wissenschaftler wissen, dass in den Gehirnzellen bei Huntington viele Prozesse fehlreguliert sind — die Energieproduktion versagt, schädliche Proteine verklumpen und die chemische Kommunikation zwischen Zellen wird toxisch. Weil so viele Signalwege gleichzeitig gestört sind, hatte die „ein Protein, ein Arzneistoff“-Strategie Schwierigkeiten, echte Durchbrüche zu erzielen.
Drei kritische Druckpunkte im Gehirn
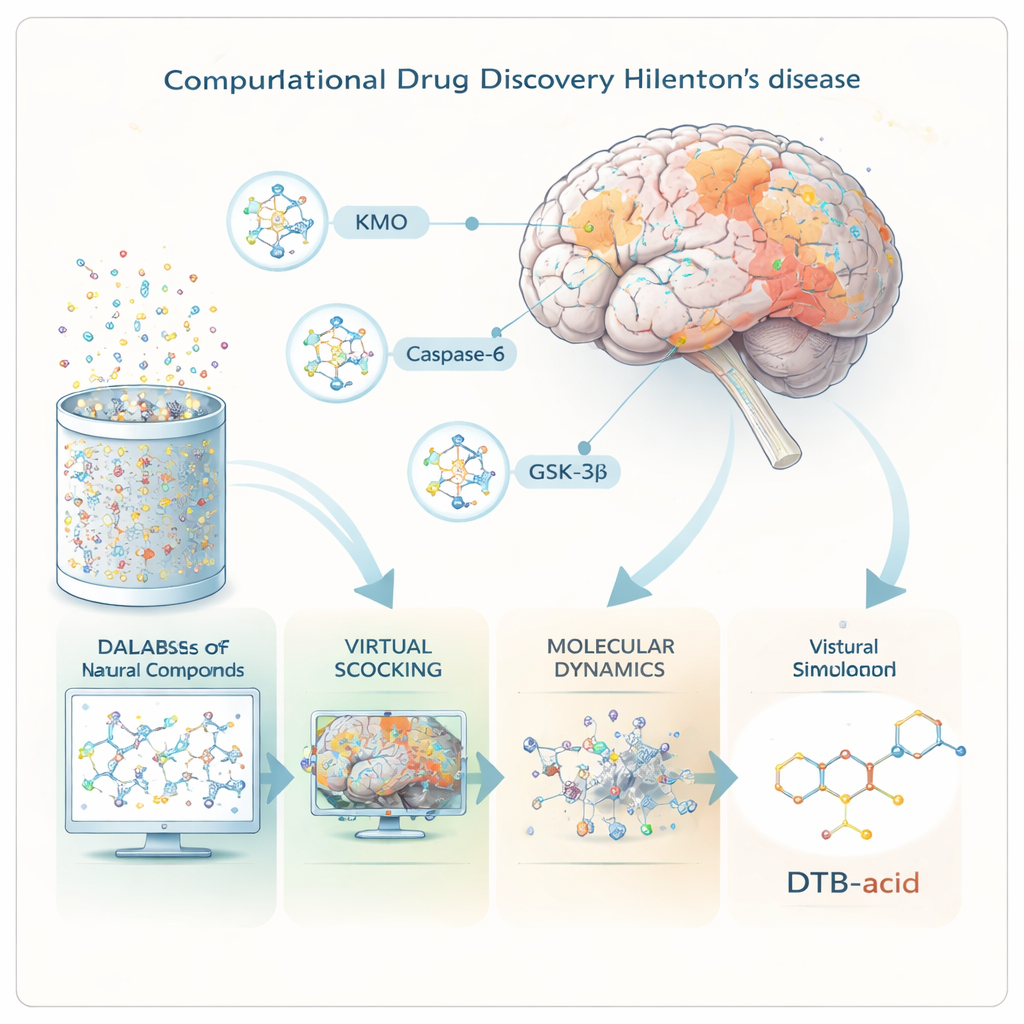
Die Forschenden konzentrierten sich auf drei Proteine, die an Schlüsselstellen der Huntington‑Pathologie stehen. Das erste, KMO, steuert den Abbau der Aminosäure Tryptophan in entweder toxische oder schützende Nebenprodukte; wenn dieses Gleichgewicht zugunsten der Toxine kippt, leiden die Gehirnzellen. Das zweite, Caspase‑6, zerschneidet das mutierte Huntingtin‑Protein in kleinere, hochtoxische Fragmente, die sich früh in der Erkrankung anreichern. Das dritte, GSK‑3β, ist ein Signalkinase, die mit abnormen Proteinverflechtungen und Zelltod bei mehreren Hirnerkrankungen in Verbindung gebracht wird. Indem sie eine einzige Verbindung suchten, die die schädliche Aktivität aller drei zugleich drosseln kann, hoffte das Team, eine Therapie zu entwerfen, die besser zur Komplexität der Krankheit passt.
Durchforstung des Naturstoff‑Archivs mit Supercomputern
Statt Chemikalien in Reagenzgläsern zu mischen, arbeiteten die Wissenschaftler vollständig „in silico“ und nutzten fortschrittliche Software, um das Verhalten von Molekülen zu modellieren. Sie begannen mit mehr als 695.000 Naturstoffen aus einer öffentlichen Datenbank und bereiteten jedes davon in dreidimensionaler Form vor. Leistungsfähige virtuelle Screening‑Tools sagten dann voraus, welche Verbindungen wahrscheinlich die Blut‑Hirn‑Schranke passieren, sich wie echte Arzneistoffe im Körper verhalten und größere Sicherheitsprobleme vermeiden. Nur etwa 60.000 überstanden diese Filter und wurden, wiederum rechnerisch, darauf getestet, wie passgenau sie in die Bindungstaschen der drei Zielproteine passen könnten.
Ein herausragendes Molekül: DTB‑Acid
Aus dieser enormen Suche stieg ein Molekül — genannt DTB‑acid, ein natürliches Alkaloid verwandt mit Matrinsäure — an die Spitze. Detaillierte Docking‑Studien zeigten, dass DTB‑acid in allen drei Proteinen starke, gut platzierte Kontakte ausbilden kann. Anschließend führten die Forschenden lange Molekulardynamik‑Simulationen durch, die nachahmen, wie Atome sich im Wasser über die Zeit bewegen, um zu prüfen, ob die Verbindung im Bindungszentrum stabil bleibt oder wegdriften würde. Über 100 Milliardenstel Sekunden simulierte Bewegung blieben die Protein‑Arzneimittel‑Komplexe stabil. Zusätzliche Energieberechnungen deuteten darauf hin, dass die Bindung an KMO besonders stark ist, während eine separate Analyse der Wassermoleküle in den Bindungsstellen zeigte, dass auch die Wechselwirkungen mit GSK‑3β thermodynamisch günstig sind.
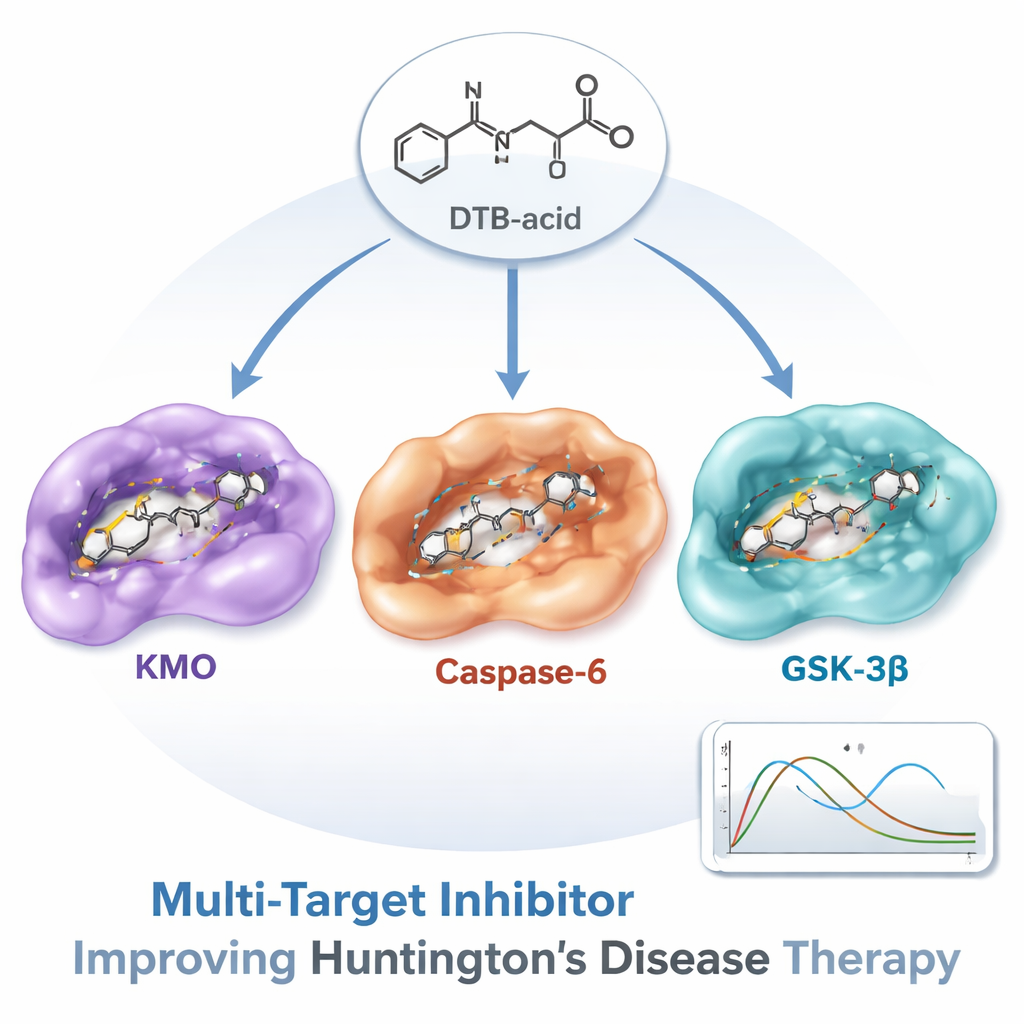
Vom Computer‑Treffer zur zukünftigen Medizin
Natürlich ist ein am Bildschirm vielversprechend erscheinendes Molekül nur ein erster Schritt. Die Autorinnen und Autoren betonen, dass DTB‑acid noch in Zellen und Tiermodellen getestet werden muss, um zu bestätigen, dass es das Gehirn erreicht, die beabsichtigten Ziele trifft und tatsächlich Neuronen schützt, ohne schädliche Nebenwirkungen. Dennoch zeigt diese Arbeit einen leistungsfähigen, effizienten Weg zur Entdeckung von Multi‑Target‑Medikamenten für komplexe Hirnerkrankungen. Für Nicht‑Spezialisten ist die Kernbotschaft: Anstatt Huntington mit einer Reihe separater, eng fokussierter Medikamente zu behandeln, könnte es möglich sein, eine sorgfältig zugeschnittene Verbindung wie DTB‑acid zu entwickeln, die mehrere Treiber der Schädigung gleichzeitig angreift — und damit neue Hoffnung bietet, den Verlauf dieser unerbittlichen Erkrankung zu verlangsamen oder zu verändern.
Zitation: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Schlüsselwörter: Huntington‑Krankheit, Multi‑Target‑Medikament, computergestützte Wirkstoffforschung, Naturstoffe, Neurodegeneration