Clear Sky Science · de
Integrierte Multi-Datensatz-Screenings zur Vorhersage der Prognose und Identifizierung von Immuntherapie-Genzielen bei Patienten mit hepatozellulärem Karzinom
Warum das für Menschen mit Leberkrebs wichtig ist
Das hepatozelluläre Karzinom, die häufigste Form von primärem Leberkrebs, fordert jährlich Hunderttausende Todesopfer. Viele Patientinnen und Patienten mit gleichem Krankheitsstadium sprechen sehr unterschiedlich auf Therapien an, insbesondere auf moderne Immuntherapien, die das körpereigene Immunsystem aktivieren sollen. Diese Studie stellt eine einfache, aber zentrale Frage: Lassen sich Tumoren anhand ihres Genaktivitätsprofils wie ein Fingerabdruck lesen, um vorherzusagen, wer eine schlechte Prognose hat, wer auf immunbasierte Medikamente anspricht und welche Gene potenzielle neue Therapieziele sind?
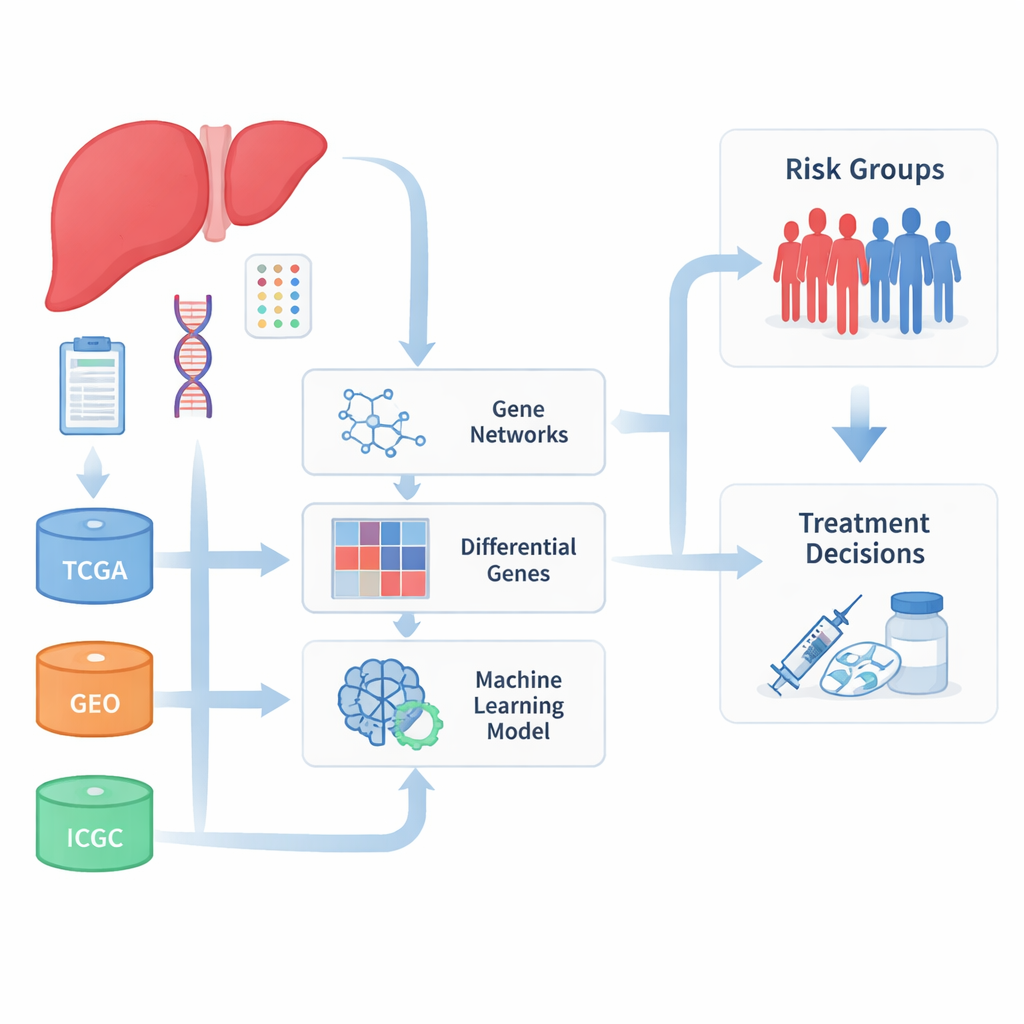
Verschiedene Datensätze zusammenführen
Die Forschenden begannen damit, große Sammlungen von Leberkrebsproben aus mehreren internationalen Datenbanken zusammenzuführen, die Tumorgenaktivität und klinische Ergebnisse dokumentieren. Durch die Kombination von Daten aus The Cancer Genome Atlas, dem International Cancer Genome Consortium und mehreren Studien des Gene Expression Omnibus stellten sie eine deutlich größere und vielfältigere Patientenkohorte zusammen, als es ein einzelnes Krankenhaus oder Projekt ermöglichen könnte. Da diese Datensätze in unterschiedlichen Laboren und mit verschiedenen Methoden erzeugt wurden, investierte das Team zunächst erhebliche Anstrengungen, um technische Unterschiede zu korrigieren, damit echte biologische Signale und nicht Laborrauschen die Ergebnisse bestimmten.
Gene finden, die mit dem Verlauf verknüpft sind
Mit bereinigten Daten suchte das Team nach Genclustern, die tendenziell gemeinsam an- und abgeschaltet werden und gleichzeitig mit dem klinischen Verlauf der Patienten korrelieren. Mit einem netzwerkartigen Ansatz gruppierten sie Tausende von Genen in Module und konzentrierten sich auf jene Module, die am stärksten mit Tumorverhalten und Überleben verbunden waren. Außerdem verglichen sie Tumoren mit nicht-tumorösem Gewebe, um Gene zu identifizieren, die in Krebs deutlich stärker oder schwächer aktiv sind. Die Überlappung dieser beiden Perspektiven ergab eine Liste von 93 Genen, die sowohl im Leberkrebs verändert als auch eng mit wichtigen Krankheitsmerkmalen verknüpft sind, viele davon beteiligt an der Arzneimittelverarbeitung und dem Umgang mit toxischen Stoffen in der Leber.
Entwicklung eines Zehn‑Gen-Risikoscores
Um diese Genlisten in etwas zu überführen, das Ärzte später verwenden könnten, wandten die Autorinnen und Autoren maschinelles Lernen an. Sie testeten mehr als hundert Kombinationen von Merkmalsauswahl- und Überlebensvorhersagealgorithmen und bewerteten sie danach, wie genau sie Patientengruppen mit besserer oder schlechterer Prognose in mehreren unabhängigen Kohorten trennen konnten. Aus dieser umfangreichen Suche destillierten sie eine kompakte Signatur von zehn Genen, die zusammen einen Risikoscore bilden. Patienten mit hohen Scores wiesen konsistent kürzere Gesamt-, krankheitsfreie und progressionsfreie Überlebenszeiten auf, sowohl in den Primärdatensätzen als auch in externen Validierungsgruppen. Unter diesen Genen hob sich TYMS als starker Indikator für schlechte Prognose hervor, während APOL3 und FBXO2 mit günstigeren Verläufen assoziiert waren.
Hinweise aus der immunologischen Nachbarschaft des Tumors
Die Studie ging über die reine Vorhersage hinaus und fragte, warum diese Gene relevant sind. Mithilfe mehrerer rechnerischer Werkzeuge schätzte das Team ab, welche Immunzelltypen in jedem Tumor vorhanden sind und wie stark der Zehn‑Gen-Score mit dieser immunologischen Landschaft zusammenhängt. Hochrisiko-Tumoren zeigten tendenziell Immunmuster und Genveränderungen, die mit mehr Mutationen und mit Merkmalen der Immunflucht verbunden sind, einschließlich Verknüpfungen zu bekannten Checkpoint-Molekülen wie PD‑1 und CTLA‑4. Sie untersuchten zudem tatsächliche Mutationsprofile und fanden, dass Hochrisiko-Tumoren häufiger Veränderungen in klassischen Krebs-Treibern wie TP53 aufwiesen. Schließlich bestätigten Bluttests von Patientinnen, Patienten und gesunden Freiwilligen, dass TYMS erhöht und FBXO2 reduziert ist bei Menschen mit Leberkrebs, was die Annahme stützt, dass diese Gene biologisch aktiv in der Erkrankung sind und nicht nur statistische Artefakte.
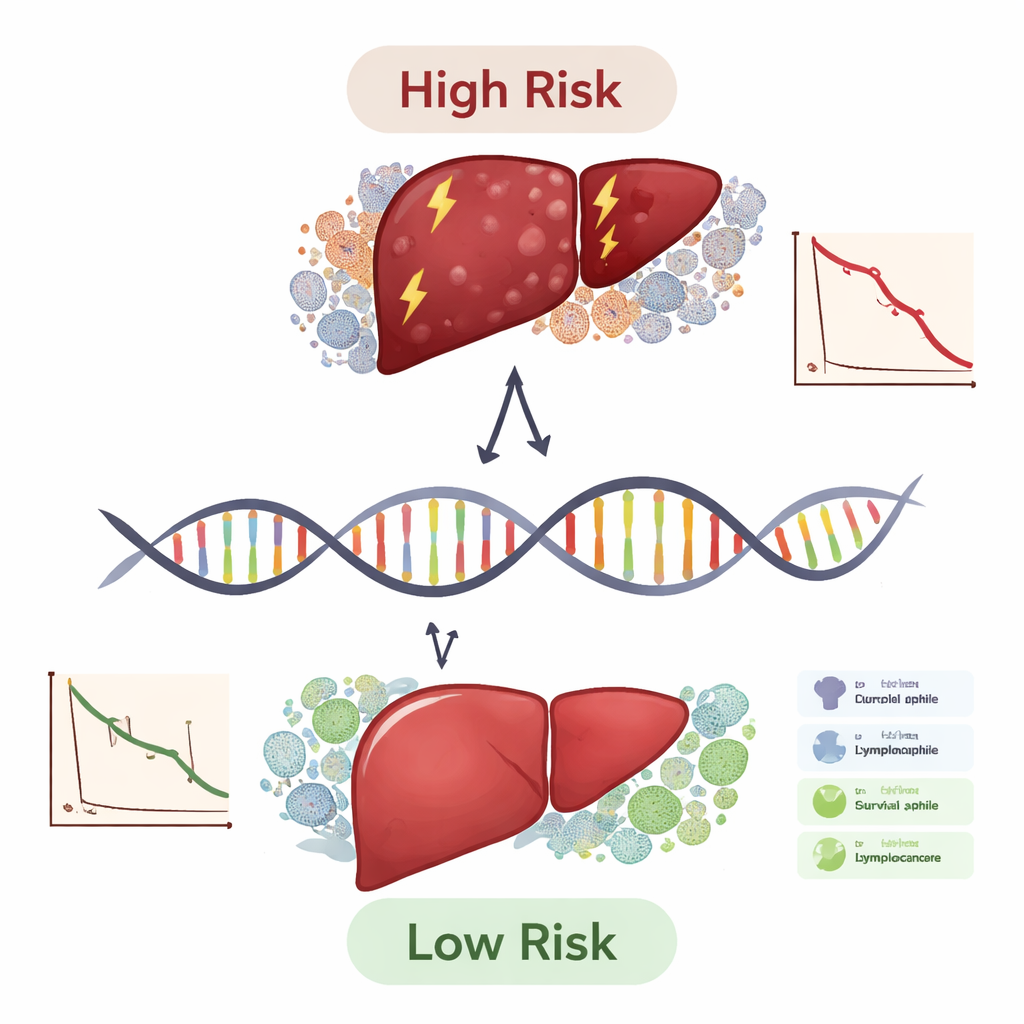
Was das für Patientinnen, Patienten und Ärztinnen und Ärzte bedeutet
Praktisch betrachtet liefert diese Arbeit einen Fahrplan, wie ein kleines Genpanel genutzt werden könnte, um Leberkrebspatienten in Risikogruppen einzuteilen und Hinweise zu geben, wer vermutlich am meisten von immunbasierten Therapien profitiert. Der Zehn‑Gen-Score ist noch kein klinisch einsetzbarer Test, erwies sich jedoch als besser als alleinige Standard-Stagingsysteme und blieb in verschiedenen Patientensubgruppen nützlich. So wie Cholesterinwerte die Prävention von Herzerkrankungen leiten, könnte ein solches Genpanel eines Tages Onkologen helfen, für Hochrisiko-Patienten aggressivere Therapien zu wählen, Niedrigrisikopatienten vor unnötigen Nebenwirkungen zu bewahren und Arzneimittelentwickler auf neue Ziele wie TYMS, APOL3 und FBXO2 zu lenken. Größere prospektive Studien und Laborversuche werden nötig sein, doch diese integrierte Analyse ist ein bedeutender Schritt hin zu einer stärker personalisierten, biologisch fundierten Versorgung bei Leberkrebs.
Zitation: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Schlüsselwörter: hepatozelluläres Karzinom, Gensignatur, Immuntherapie, Prognose, Tumormikroumgebung