Clear Sky Science · de
Anwendungsanalyse der transfizierten Zellmethode zum Nachweis von AChR-Antikörpern bei MG-Patienten
Warum das für Menschen mit Muskelschwäche wichtig ist
Myasthenia gravis ist eine Erkrankung, bei der das körpereigene Abwehrsystem die Kontaktstellen angreift, an denen Nerven mit Muskeln kommunizieren, was zu herabhängenden Augenlidern, Problemen beim Kauen und allgemeiner Erschöpfung führt. Ärztinnen und Ärzte stützen sich auf Bluttests, die nach diesen fehlgeleiteten Antikörpern suchen, doch die heute verwendeten Tests übersehen einen beträchtlichen Teil der Betroffenen. Diese Studie untersucht eine neuere, zellbasierte Methode, um diese Antikörper zuverlässiger zu erkennen — mit möglicher Folge einer früheren Diagnose und einer besseren Orientierung für die Behandlung.
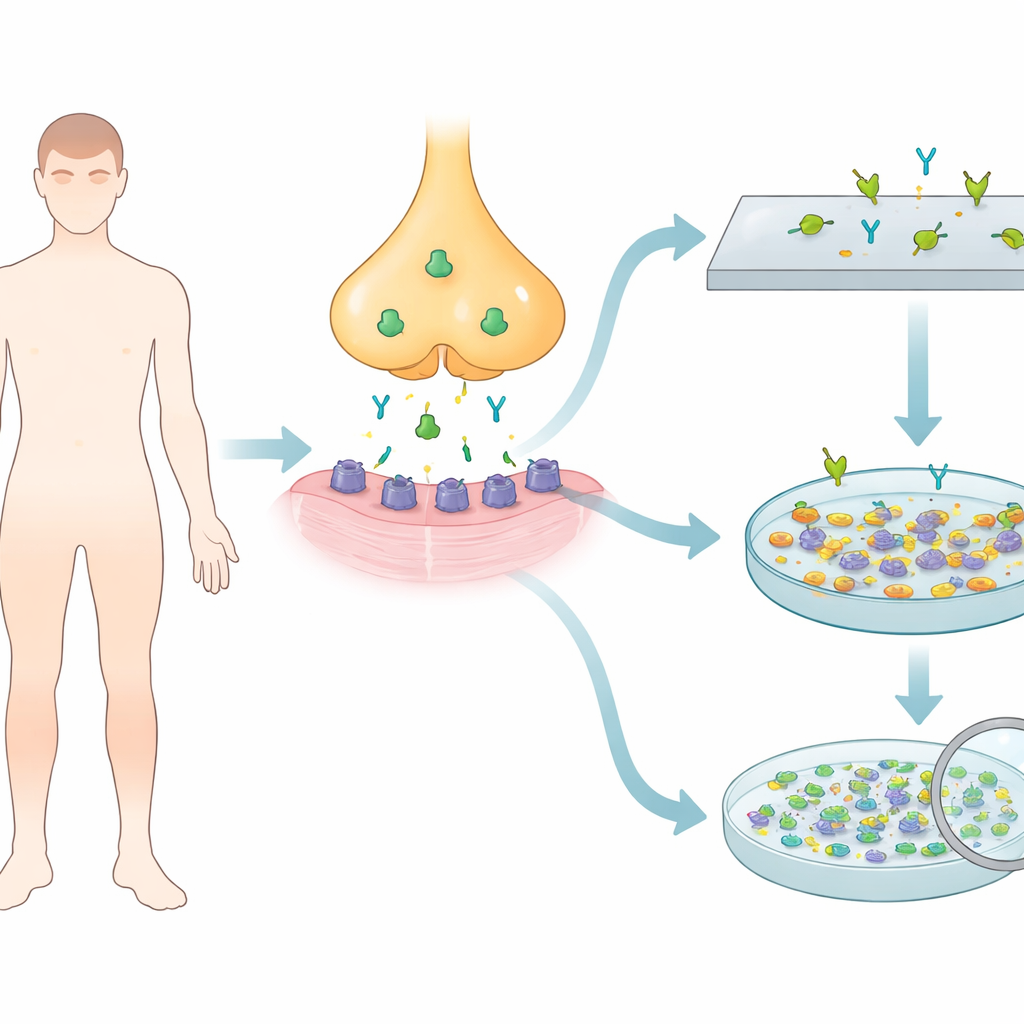
Ein versteckter Angriff an der Schnittstelle zwischen Nerv und Muskel
Bei Myasthenia gravis richtet sich das Immunsystem gegen ein Schlüsselprotein, den Acetylcholinrezeptor, der wie ein Tor wirkt und Nervenimpulse in Muskelbewegungen umsetzt. Die meisten Patientinnen und Patienten mit generalisierter Erkrankung und viele mit ausschließlich okulären Symptomen tragen Antikörper gegen diesen Rezeptor im Blut. Dennoch testen bis zu die Hälfte der Personen mit nur Augenbetroffenheit und etwa 10–15 Prozent derjenigen mit weiter verbreiteter Schwäche negativ in Standard-Bluttests. Ein plausibler Grund ist, dass manche Antikörper nur schwach an den Rezeptor binden und so konventionelle Tests, die gereinigte oder vereinfachte Proteinformen verwenden, umgehen.
Gewöhnliche Zellen in empfindliche Testplattformen verwandeln
Die Forschenden wollten ein hausinternes, zellbasiertes Testverfahren mithilfe einer in Laboren häufig verwendeten menschlichen Zelllinie entwickeln. Sie schrieben genetische Anweisungen für verschiedene Kombinationen von Rezeptorbausteinen — adulte Form, fetale Form und eine Mischung aus beiden — sowie ein Hilfsprotein, das Rezeptoren an der Zelloberfläche bündelt. Diese gentechnisch veränderten Zellen wurden auf winzigen Glasplättchen gezüchtet und fixiert, sodass sie als gebrauchsfertige Testobjekte gelagert werden konnten. Bei Zugabe von verdünntem Patientenserum binden vorhandene Antikörper an diese gebündelten Proteine und lassen sich mit einem fluoreszierenden Sekundärantikörper unter dem Mikroskop sichtbar machen.
Die beste Kombination finden, um mehr Antikörper zu erfassen
Das Team stellte zuerst fest, dass Zellen, die nur eine einzelne Rezeptoruntereinheit exprimierten, kein Signal zeigten, selbst wenn sie mit 48 Proben getestet wurden, die in einem kommerziellen Test positiv waren. Das deutet darauf hin, dass Patientenantikörper die dreidimensionale Struktur des Rezeptors auf der Zelloberfläche erkennen und nicht isolierte Teile, die noch im Zellinneren sitzen. Im Gegensatz dazu zeigten Zellen, die mit vollständigen adulten oder fetalen Rezeptorkombinationen konstruiert waren, klare Fluoreszenzsignale bei positiven Seren und blieben bei Kontrollen ohne Befund dunkel. Die stärksten und häufigsten Signale traten auf, wenn Zellen eine Mischung aus beiden, adulten und fetalen Rezeptorformen zusammen exprimierten — besonders bei Proben mit niedrigerer Antikörperlast. In einer Gruppe von 24 sorgfältig ausgewählten pädiatrischen und erwachsenen Patientinnen und Patienten lieferte dieser „Komplettmix“-Slide in etwa zwei Dritteln der Fälle mittelstarke bis starke Signale und übertraf damit deutlich die ausschließlich adulten oder fetalen Präsentationen.
Direkter Vergleich mit einem Standard-Bluttest
Um ihr zellbasiertes Verfahren mit einem weit verbreiteten Enzymimmunassay (ELISA) zu vergleichen, testeten die Forschenden 85 Myasthenia-gravis-Patientinnen und -Patienten mit beiden Methoden. Der ELISA detektierte Rezeptorantikörper bei etwa 68 Prozent der Patienten, während der zellbasierte Assay sie bei mehr als 75 Prozent nachwies. Insgesamt stimmten die beiden Tests gut überein — das statistische Übereinstimmungsmaß (Kappa) war hoch — dennoch gab es acht Patientinnen und Patienten mit widersprüchlichen Ergebnissen. Als zur Klärung ein Radioimmunassay, der als Referenzmethode gilt, hinzugezogen wurde, stimmte er in sechs der acht Fälle mit dem zellbasierten Test überein. Dieses Muster deutet darauf hin, dass der zellbasierte Test einige niedrigaffine Antikörper erfassen kann, die der ELISA übersieht, ohne dabei an Spezifität einzubüßen.
Was das für Patientinnen, Patienten und Ärztinnen und Ärzte bedeutet
Indem gewöhnliche Laborzellen dichte, altersgemischte Varianten des Acetylcholinrezeptors auf ihrer Oberfläche zeigten, entwickelte diese Studie einen empfindlicheren Suchscheinwerfer für krankheitsverursachende Antikörper bei Myasthenia gravis. Der neue Assay arbeitet insgesamt mindestens so zuverlässig wie bestehende kommerzielle Tests und könnte besser geeignet sein, schwer nachweisbare Antikörper zu erfassen — insbesondere bei Patientinnen und Patienten mit niedrigen Antikörperspiegeln oder komplexeren Antikörperprofilen. Größere, multizentrische Studien und Verfeinerungen mit lebenden Zellen sind zwar noch notwendig, bevor eine breite Anwendung sinnvoll ist, doch diese Arbeit skizziert einen praktikablen Weg zu präziseren Bluttests, die Ärztinnen und Ärzten helfen können, Diagnosen früher zu bestätigen, die Krankheit genauer zu überwachen und Behandlungen besser auf die Betroffenen abzustimmen.
Zitation: Liu, W., Xia, Z., Hu, J. et al. Application analysis of transfected cell method for detecting AChR antibodies in MG patients. Sci Rep 16, 8130 (2026). https://doi.org/10.1038/s41598-026-38414-w
Schlüsselwörter: Myasthenia gravis, Acetylcholinrezeptor-Antikörper, Zellbasierter Test, Autoimmunerkrankung des neuromuskulären Systems, Diagnostische Sensitivität